Статтю опубліковано на с. 59-64
Вступ
Гострий панкреатит (ГП) є одним із найбільш тяжких, найскладніших, прогностично несприятливих та часто життєво небезпечних гострих захворювань органів черевної порожнини [1–3].
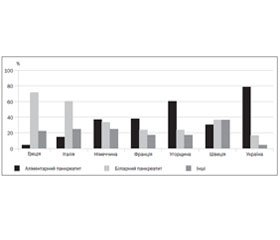
Останніми роками спостерігається помітна тенденція до збільшення кількості хворих на гострий панкреатит та його ускладнення, що зумовлено не тільки зростанням захворюваності, але й покращенням діагностики. У країнах Центральної Європи [1] захворюваність на ГП (за останні десять років) коливається у межах 10–40 випадків на 100 000 населення, причому захворюваність на біліарний панкреатит становить 40–65 %, а панкреатит, зумовлений зловживанням алкоголем, — 30–40 % (рис. 1).
Слід також відзначити, що кількість хворих на ГП залишається стабільно високою і не має тенденції до зниження, а лікування супроводжується тривалим перебуванням хворих на лікарняному ліжку і значними фінансовими витратами [3–5]. Серед широкого кола питань раціонального патогенетично обумовленого медикаментозного лікування, особливо в перші години від моменту надходження хворого, домінуюче місце займають два основні напрямки — нівелювання або повне купірування больового синдрому та стабілізація вітальних функцій (основних параметрів водно-електролітного обміну та гемодинамічних показників) шляхом адекватної інфузійної терапії [4–7].
З огляду на вищевказане опрацювання нових підходів до гемодинамічної стабілізації стану хворих на ГП шляхом оптимізації стартової інфузійної терапії заслуговує на безсумнівний науковий і практичний інтерес.
Мета дослідження — оцінити клінічну ефективність (вплив на мікроциркуляторні порушення) та роль перфузійних розчинів у комплексному хірургічному лікуванні хворих із ГП на ранньому етапі лікування.
Матеріали і методи
Проведено проспективний аналіз результатів лікування вибіркової групи пацієнтів із ГП (30 осіб), які перебували в міському спеціалізованому панкреатологічному центрі на базі клініки загальної хірургії Львівського національного медичного університету імені Данила Галицького у 2015–2016 рр. Вік пацієнтів — від 42 до 61 року (середній вік — 54,1 ± 5,8 року). Жінок було 12 (40 %), чоловіків — 18 (60 %). Діагноз захворювання встановлювався на підставі оцінки результатів клінічних, лабораторно-біохімічних, променевих (ультрасонографія, комп’ютерна томографія, рентгенографія) та інструментальних (фіброгастродуоденоскопія, відеолапароскопія) методів дослідження. Тривалість захворювання на момент госпіталізації становила від двох до чотирьох діб, у більшості пацієнтів (26; 86,7 %) — дві доби, причому в 4 випадках (13,3 %) відзначався швидкопрогресуючий розвиток захворювання.
За етіологічним чинником ГП етанольного генезу констатовано в 15 хворих (50 %), біліарного — також у 15 пацієнтів (50 %). Співвідношення чоловіки : жінки — 18 : 12, за генезом захворювання: етанольний панкреатит — 14 : 1, біліарний — 4 : 11 відповідно.
Згідно з дефініцією класифікації Атланта (2012) [6], легкий перебіг захворювання констатовано у 8 (26,66 %), середньої тяжкості — у 20 (66,67 %) і тяжкий ГП — у 2 (6,67 %) пацієнтів.
Ступінь тяжкості стану пацієнтів оцінювався з урахуванням загальноклінічних та лабораторних критеріїв (вираженість больового синдрому, блювання, тахікардія > 100–120 за хвилину, рівні артеріального тиску (АТ), систолічного АТ (САТ), діастолічного АТ (ДАТ) і центрального венозного тиску (ЦВТ), добовий діурез, об’єм циркулюючої крові, наявність ознак поліорганної недостатності).
Стратифікацію тяжкості перебігу панкреатиту проводили з урахуванням таких ознак: вік > 50 років; виражений абдомінальний больовий синдром, стійкий до анальгетичної терапії; тахікардія > 120 за 1 хв; САТ < 100 мм рт.ст.; кількість лейкоцитів периферійной крові > 15 • 109/л; рівень глюкози в крові > 10 ммоль/л; коефіцієнт АСТ/АЛТ < 1; непрямий білірубін > 60 мкмоль/л; креатинін крові > 110 мкмоль/л.
З метою стабілізації стану в перші години від моменту надходження всім пацієнтам проводилась базова медикаментозна терапія відповідно до затверджених стандартів та протоколів надання невідкладної медичної допомоги хворим із гострим панкреатитом [2] та опрацьованих у клініці локальних протоколів ведення хворих на ГП.
Усіх пацієнтів за принципом «сліпого конверта» було розподілено на дві групи, які були репрезентативними за статтю та тяжкістю домінуючої патології. До основної групи віднесено 16 хворих, у яких лікувальна програма поряд із базовою медикаментозно-інфузійною терапією включала додаткове введення перфузійного розчину Гекотон зі швидкістю інфузії 5 мл/кг/год (350–400 мл/год, об’ємом 400–800 мл/добу).
Порівняльна група об’єднувала 14 пацієнтів, компенсація гіповолемічних порушень у яких забезпечувалася призначенням базової інфузійної терапії в загальному об’ємі до 2,5 літра.
Оскільки програма інфузійної підтримки у хворих на ГП на фоні форсованого діурезу розрахована на введення понад 2–3 л розчинів, додавання колоїдного компонента вважалося доцільним (ідеальне співвідношення кристалоїдів і колоїдів становить 3 : 1).
У 15 пацієнтів (93,75 %) основної групи і 12 (85,7 %) — групи порівняння комплексна інтенсивна консервативна інфузійно-медикаментозна терапія мала позитивний ефект і сприяла стабілізації стану хворого. У двох пацієнтів (6,7 %) із тяжким перебігом захворювання у зв’язку з прогресуванням ГП і розвитком місцевих гнійно-некротичних ускладнень у вигляді парапанкреатиту/параколіту було здійснено хірургічне втручання з використанням міні-інвазивних (інтервенційна сонографія і відеолапароскопія), традиційних лапаротомних хірургічних технологій, а також з їх поєднанням.
Відповідно до дизайну дослідження спостереження за пацієнтами (з оцінкою загального стану хворих та аналізом лабораторних показників) проводилось у три етапи: I — оцінка початкового стану хворого при надходженні у 2-ге хірургічне відділення (міський панкреатологічний центр); II — через 6 годин після початку інфузійної терапії; III — 2-га доба стаціонарного лікування.
Загальний стан хворих та ефективність проведеного комплексного лікування оцінювали з використанням лабораторних, інструментальних та апаратних методів динамічного моніторингу. Особлива увага приділялась контролю за стабілізацією вітальних функцій (АТ, частота серцевих скорочень (ЧСС), ЦВТ, погодинний діурез, сатурація кисню (SрO2), добовий діурез).
Як критерій гемодинамічної стабілізації стану хворого, а також наявності вірогідних даних про ступінь вираженості ішемії органів та систем і відновлення адекватної перфузії тканин та мікроциркуляції використовували вивчення характеру моторно-евакуаторної функції шлунково-кишкового тракту (ШКТ) та її змін у процесі інфузійної терапії. Для отримання вірогідних результатів було використано метод електроміографії (із застосуванням приладу «ЭГЭГ-01м», Росія), який забезпечує графічний контроль з комп’ютерним аналізом скорочень різних відділів ШКТ. Дослідження проводили відповідно до вимог етичного комітету. Статистичну обробку отриманих результатів здійснювали за допомогою пакета програм MS Excel 2010. Дані наведені у вигляді M ± m. Статистично вірогідним вважали значення p < 0,05.
Результати досліджень та їх обговорення
Загальний добовий розрахований обсяг інфузійної терапії становив 80 мл/кг на добу в добовому об’ємі 3800 ± 200 мл у кореляційній залежності від стану хворого на момент госпіталізації.
У 21 пацієнта (70 %) при первинному фізикальному огляді було відзначено коливання рівнів АТ із тенденцією до зниження (127,5 ± 6,9 мм рт.ст. (основна група) і 125,5 ± 6,0 мм рт.ст. (група порівняння)) та тахікардію (104 ± 11 уд/хв і 108 ± 9 уд/ хв відповідно). Зниження гемодинамічних показників (АТ) у поєднанні з даними об’єктивного клінічного огляду (сухість слизових та шкіри, зниження тургору підшкірної клітковини та шкірної складки) свідчило про наявність гіповолемії. Погодинний діурез у 18 пацієнтів (60 %) був значно знижений, аж до анурії в 9 пацієнтів (30 %). Явища прихованої гіповолемії та дегідратації у пацієнтів обох груп супроводжувалися проявами гемоконцентрації (середній рівень гематокриту крові 48,6 ± 3,8 і 49,4 ± 2,4 відповідно) та зниженням значень ЦВТ — 51,9 ± 4,8 мм рт.ст. в основній групі і 47,6 ± 5,9 мм рт.ст. — у групі порівняння.
Результати клінічних спостережень та проведений моніторинг лабораторних досліджень дозволили у 86,7 % хворих констатувати вірогідні ознаки дегідратації, зменшення тканинної перфузії з ішемією спланхнічної зони, які були підтверджені ультрасонографічним (УЗД) обстеженням (збільшення розмірів підшлункової залози, ознаки постперфузійного пошкодження з виникненням парапанкреатичних тканинних набряків, венозного стазу та порушення мікроциркуляції).
Проведення медикаментозної корекції на ранньому етапі лікування хворих із ГП дозволило адекватно відкоригувати описані вихідні порушення в переважної більшості пацієнтів (24; 80 %), проте якісний характер лікування залежав від компонентності проведеної інфузійної терапії. В обох групах уже впродовж першої доби спостерігалася стійка фіксація показників центральної гемодинаміки на нормальних значеннях з їх утриманням протягом усього терміну спостереження. Однак клінічні показники системної гемодинаміки в основній групі стабілізувались значно швидше (р < 0,05), ніж у групі порівняння (табл. 1)
Повноцінна інфузійна терапія, проведена в перші години від моменту госпіталізації пацієнтів у поєднанні з адекватним знеболюванням хворих, дозволила стабілізувати пацієнтів, що у першу чергу було підтверджено вірогідним (p < 0,05) зниженням частоти серцевих скорочень, а швидкий і тривалий волемічний ефект спряв покращенню мікроциркуляції та оксигенації (SpO2).
За даними табл. 2 ми можемо відзначити більш виражену динаміку зменшення ЧСС у хворих основної групи (із 104 ± 11 уд/хв до 82 ± 12 уд/ хв) на противагу групі порівняння (108 ± 9 уд/хв і 89 ± 11 уд/хв). Слід також відзначити, що тенденція до зниження частоти серцевих скорочень була більш виражена у хворих із гострим біліарним панкреатитом (група порівняння) і незалежно від генезу захворювання у пацієнтів основної групи, що опосередковано вказувало на більш швидке нівелювання інтоксикації.
Загалом комплексна інфузійна терапія з внутрішньовенним введенням волюмокоректорів у поєднанні з адекватним купіруванням больового синдрому дозволила досягти позитивного клінічного результату та стабілізації стану впродовж першої доби в 13 пацієнтів (86,7 %) основної групи, в той час як подібний ефект у групі порівняння виявлявся лише в 11 осіб (73,3 %).
Використання багатокомпонентного колоїдно-гіперосмолярного розчину Гекотон (основна група) сприяло відновленню адекватних водних просторів організму вже впродовж першої доби стаціонарного лікування. На фоні фізіологічних рівнів електролітів, нормальних значень осмолярності плазми впродовж усього періоду клінічного спостереження за станом хворих рідинний баланс організму відповідав фізіологічному. Це збігалося зі зниженням гематокриту до 44,5 ± 2,1 у чоловіків та 39,6 ± 2,1 у жінок на 2-гу добу спостереження і відновленням до нормальних показників коагулограми на 3-тю добу дослідження. Погодинний діурез збільшувався до 0,8 мл/кг/год без медикаментозної стимуляції. Ознаки дегідратації були відсутні. За даними УЗД-моніторингу, на п’яту добу в 9 пацієнтів (56,3 %) основної групи відзначено покращення ультрасонографічної картини в ділянці підшлункової залози (зменшення розмірів головки й тіла залози, відсутність парапанкреатичного набряку).
На противагу пацієнтам основної групи станом на 2-гу добу спостереження у хворих групи порівняння рівень гематокриту залишався підвищеним: 47,8 ± 4,6 — у чоловіків та 44,7 ± 3,8 — у жінок. За результатами спостережень у пацієнтів із групи порівняння паралельно було констатовано, що при застосуванні стандартної (базової) інфузійної терапії були стабільні показники центральної та системної гемодинаміки, однак відзначалися прояви помірного локального інтерстиціального набряку. За даними УЗД-обстежень, на 5-ту добу лікування відсутність парапанкреатичного набряку та зменшення розмірів підшлункової залози відзначено лише у 6 хворих (42,8 %).
Загалом слід вказати, що проведена інфузійна терапія сприяла стабілізації АТ у більшості пацієнтів уже через дві-три години від її початку. Однак в основній групі (на фоні інфузії Гекотону) на 2-гу добу тенденція до стабілізації гемодинамічних показників (зниження ЧСС — 104 ± 11 уд/хв vs 82 ± 12 уд/хв; САТ і ДАТ на рівні 134,2 ± 5,1/81,3 ± 11,7 мм рт.ст. відповідно) була більш виражена, ніж у групі порівняння (ЧСС — 108 ± 9 уд/хв vs 89 ± 11 уд/хв; САТ і ДАТ 139,2 ± 4,0/86,0 ± 14,5 мм рт.ст. відповідно).
Наведені результати спостережень дозволяють стверджувати, що інтенсивна терапія (ІТ) у хворих основної групи (з додаванням гідроксіетилкрохмалю) сприяла оптимізації кровообігу та забезпечувала стабілізацію АТ у поєднанні з мікроциркулярним компонентом, у той час як базова ІТ забезпечувала відновлення лише АТ та венозної частини мікроциркуляторного русла. Даний висновок підтверджували й результати, отримані при визначенні ступеня сатурації (через 6 годин від моменту завершення інфузійної терапії). У хворих основної групи показник SpO2 становив 97,3 ± 4,2 %, у той час як хворих із групи порівняння — 94,2 ± 3,8 %.
/63.jpg)
Заслуговують на увагу також результати проведених електроміографічних досліджень з оцінкою особливостей, стану та характеру моторно-евакуаторної функції кишкового тракту у хворих обох груп та моніторингу рентгенологічної картини. Проведені скринінгові спостереження показали, що в пацієнтів як основної, так і групи спостереження на момент надходження перистальтичні хвилі шлунка та дванадцятипалої кишки мали хаотичний, дискоординований характер без чіткої послідовності та ритму м’язових скорочень, які не піддавалися числовому аналізу (рис. 2). Однак вже через 1,5–2 години після закінчення інфузійної терапії у хворих основної групи спостерігалося упорядкування перистальтичних м’язових скорочень з їх кількісним зростанням (до 3–4 на хвилину), більше вираженою амплітудою, що свідчило про покращення пропульсивної здатності тонкої кишки (рис. 3).
З третьої доби до комплексу медикаментозної терапії було додано препарати з прокінетичними властивостями, які на фоні інфузійної терапії сприяли повноцінному відновленню пасажу в 75 % хворих основної групи (рис. 4).
У хворих з групи порівняння, незважаючи на активне використання прокінетиків, аналогічних результатів відновлення пропульсивної здатності кишечника вдалося досягти лише на 4–5-ту добу (тривалість затримки у відновленні перистальтики — 28–36 год).
Вірогідних відмінностей за результатами електроміографічних обстежень пропульсивної здатності кишечника в пацієнтів обох груп на 5–6-ту добу лікування виявлено не було (р < 0,05).
Отже, додавання до інфузійної терапії багатокомпонентного полііонного колоїдно-гіперосмолярного розчину Гекотон® відповідно до методики малооб’ємної ресусцитації (small-volume resuscitation) у хворих із ГП супроводжувалося позитивним ефектом, який визначався зниженням ЧСС, відновленням адекватного ступеня сатурації та покращенням пропульсивної здатності кишечника, що і визначає доцільність використання даного препарату в клінічній практиці.
Висновки
1. Проведення повноцінної медикаментозної терапії з компонентом інфузійної терапії у хворих з гострим панкреатитом на ранньому етапі лікування є клінічно доцільним і патогенетично обґрунтованим.
2. Корекція гіповолемічних порушень із включенням перфузійних розчинів гідроксіетилкрохмалю сприяє стабілізації стану пацієнтів, має виражений позитивний мікроциркулярний ефект та забезпечує раннє відновлення перистальтики у даного контингенту хворих.
/64.jpg)

/60.jpg)
/61.jpg)
/62.jpg)
/63.jpg)