Резюме
У статті описано основні причини порушення функції діафрагми, клінічне значення її дисфункції. До дослідження включено 8 пацієнтів віком 1–3 роки з дихальною недостатністю (досліджувана група) та 10 пацієнтів аналогічного віку без ознак дихальної недостатності (контрольна група). Наведено власні результати ультразвукового дослідження діафрагми при проведенні механічної вентиляції легень у режимах PCV, P-SIMV та при спонтанному диханні через 2 год після екстубації в досліджуваній групі пацієнтів. Вивчено такі показники, як товщина правого та лівого куполів діафрагми, фракція їх стоншення, амплітуда рухів під час дихання, а також наявність десинхронізації при проведенні механічної вентиляції легень. Установлено, що в пацієнтів досліджуваної групи правий купол діафрагми під час вдиху мав вірогідно меншу товщину порівняно з аналогічним показником у контрольній групі пацієнтів, що становила 4,60 ± 0,15 мм при механічній вентиляції легень у режимі PCV, 4,40 ± 0,11 мм — у режимі P-SIMV та 4,50 ± 0,06 мм — при спонтанному диханні порівняно з 5,90 ± 0,21 мм у контрольній групі. Товщина лівого купола діафрагми при вдиху в пацієнтів досліджуваної групи була більшою на всіх етапах проведення механічної вентиляції легень порівняно з контрольною групою пацієнтів та становила 5,10 ± 0,17 мм у режимі PCV, зменшувалася до 4,00 ± 0,12 мм у режимі P-SIMV та до 4,00 ± 0,12 мм під час спонтанного дихання порівняно з 3,40 ± 0,04 мм у контрольній групі пацієнтів. Отже, у дітей із дихальною недостатністю відмічаються дисфункція правого купола діафрагми, а також порушення релаксації лівого купола діафрагми при збереженій його скоротливій здатності.
В статье описаны основные причины нарушения функции диафрагмы, клиническое значение ее дисфункции. В исследования нами были включены 8 пациентов с дыхательной недостаточностью (исследуемая группа) и 10 пациентов такого же возраста без признаков дыхательной недостаточности (контрольная группа). Приведены собственные результаты ультразвукового исследования диафрагмы при проведении механической вентиляции легких в режимах PCV, P-SIMV и при спонтанном дыхании через 2 ч после экстубации в исследуемой группе пациентов. Изучены такие показатели, как толщина правого и левого куполов диафрагмы, фракция их истончения, амплитуда движений при дыхании, а также наличие десинхронизации при проведении механической вентиляции легких. Установлено, что у пациентов исследуемой группы правый купол диафрагмы во время вдоха имел достоверно меньшую толщину по сравнению с аналогичным показателем в контрольной группе пациентов, которая составляла 4,60 ± 0,15 мм при механической вентиляции легких в режиме PCV, 4,40 ± 0,11 мм — в режиме P-SIMV и 4,50 ± 0,06 мм — при спонтанном дыхании по сравнению с 5,90 ± 0,21 мм в контрольной группе. Толщина левого купола диафрагмы на вдохе у пациентов исследуемой группы была больше на всех этапах проведения механической вентиляции легких по сравнению с контрольной группой пациентов и составила 5,10 ± 0,17 мм в режиме PCV, уменьшалась до 4, 00 ± 0,12 мм в режиме P-SIMV и до 4,00 ± 0,12 мм при спонтанном дыхании по сравнению с 3,40 ± 0,04 мм в контрольной группе пациентов. Итак, у детей с дыхательной недостаточностью отмечаются дисфункция правого купола диафрагмы, а также нарушение релаксации левого купола диафрагмы при сохраненной его сократительной способности.
Introduction. Acute respiratory failure is accompanied by excessive work of breathing muscles. During the decompensation of acute respiratory failure, a patient will have the violation of the delivery of oxygen and elimination of carbon dioxide. The main causes of respiratory failure can be lung damage with worsening transport of gases through the alveolar-capillary membrane and the violations of various parts of the nervous system with impaired regulation of respiration. One of the main respiratory muscles, performing over 50 % work of the respiratory system, is the diaphragm. Therefore, the detection of diaphragm dysfunction is a necessary component of diagnostics that helps modify the treatment of patients with respiratory failure. Materials and methods. In our study we included 8 patients with respiratory failure (study group) and 10 patients, who had no respiratory failure (control group). We performed the ultrasound examination of the diaphragm during mechanical ventilation in the modes PCV, P-SIMV and during spontaneous breathing 2 hours late after weaning from mechanical ventilation in study group patients and during spontaneous breathing in control group. We studied such parameters as the thickness of the right and left hemidiaphragm, a fraction of thickness, range of diaphragm motion during breathing and the presence of desynchronization during mechanical ventilation. Results. Patients of both groups did not differ significantly by the age, but the average weight of patients in the study group was significantly lower than in the control group. In 75 % of patients in the study group, we identified body weight deficit from 10 to 30 %. We found that in patients of the study group thickness of the right hemidiaphragm during inspiration in all modes of mechanical ventilation was significantly less compared to the same parameter in the control group patients and were 4.60 ± 0.15 mm during PCV mode; 4.40 ± 0.11 mm during P-SIMV mode, 4.50 ± 0.06 mm during spontaneous breathing and 5.90 ± 0.21 mm in the control group patients. The thickness of the left hemidiaphragm during inspiration in patients of the study group was greater at all stages of mechanical ventilation compared with the control group of patients and was 5.10 ± 0.17 mm during PCV mode, decreased to 4.00 ± 0.12 mm during P-SIMV mode and was 4.00 ± 0.12 mm during spontaneous breathing and 3.40 ± 0.04 mm in the control group patients. Thickness fraction of right hemidiaphragm in patients of the study group was significantly lower compared with this indicator in the control group of patients and was 0.25 ± 0.04 during the mechanical ventilation in PCV mode, 0.29 ± 0.02 in P-SIMV mode and 0.38 ± 0.05 during spontaneous breathing versus 0.50 ± 0.08 in control group. Thickness fraction of left hemidiaphragm in patients of the study group had no significant differences in comparison to the control group of patients, but this index showed a better contractility of the left hemidiaphragm compared with right hemidiaphragm during the mechanical ventilation in PCV and P-SIMV modes in study group patients. The frequency of desynchronization between the patient and the machine of mechanical ventilation was highest during the mechanical ventilation in PCV mode and in the most cases it can be reduced with the correction of inspiratory time or the ratio between inspiration and expiration under ultrasound control. This method gives us the opportunity to avoid excessive sedation of patients and makes possible daily assessment for the beginning of the weaning from mechanical ventilation. Conclusions. In children with respiratory failure, there are the dysfunction of the right hemidiaphragm and relaxation dysfunction of the left hemidiaphragm without violating its contractile ability. We suggest using techniques that monitor diaphragm muscle function to confirm a physiologically acceptable level of diaphragm contractility and allow the clinician to optimize ventilator settings in order to improve patient-ventilator interaction.
Статтю опубліковано на с. 73-77
Вступ
Частою причиною розвитку дихальної недостатності в дітей є гострі захворювання нижніх дихальних шляхів, до яких належать і пневмонії. За даними ВООЗ, в Україні кількість випадків смерті дітей від гострих захворювань нижніх дихальних шляхів упродовж останніх 15 років зменшилася практично втричі та станом на 2015 рік становила для дітей від 1 до 59 міс. 0,5 випадку на 1000 дітей, народжених живими, що в 2,5 раза перевищує аналогічний показник для США, у віковій групі 0–4 роки — 0,8 випадку, що в 4 рази вище, ніж у США у 2015 році, тоді як кількість випадків смерті дітей від ВІЛ/СНІДу в Україні в обох вікових групах у 2015 році становить лише 0,2 випадку на 1000 дітей, народжених живими (у США жодна дитина не померла у 2015 році внаслідок цієї причини) [9]. Тому добра спланованість надання допомоги та наявність сучасних алгоритмів діагностики й інтенсивної терапії могли б покращати результати лікування такої категорії дітей.
Гостра дихальна недостатність супроводжується надмірною роботою дихальних м’язів, а при декомпенсації стану пацієнта — порушенням доставки кисню та елімінації вуглекислого газу. Причинами розвитку дихальної недостатності можуть бути як ушкодження паренхіми легень із порушенням транспорту газів через альвеоло-капілярну мембрану, так і порушення різних ланок регуляції роботи системи органів дихання. Одним з основних дихальних м’язів, що виконує понад 50 % роботи системи дихання, є діафрагма. Зважаючи на це, виявлення діафрагмальної дисфункції є необхідною складовою діагностики, що допоможе модифікувати лікування пацієнтів із дихальною недостатністю.
Мета дослідження: вивчити дані літератури про методи оцінки функції діафрагми і роль її дисфункції в маніфестації та персистенції дихальної недостатності і дослідити функцію діафрагми в дітей при паренхіматозній дихальній недостатності.
Матеріали та методи
До дослідження включено 8 дітей віком від 1 до 3 років із гострою дихальною недостатністю, які потребували проведення механічної вентиляції легень (МВЛ) (досліджувана група пацієнтів). Контрольну групу становили 10 дітей від 1 до 3 років без патології системи органів дихання. Усі пацієнти перебували на лікуванні у комунальному закладі «Львівська обласна дитяча клінічна лікарня «ОХМАТДИТ» з 01.04.2016 р. по 01.09.2016 р.
Функцію діафрагми вивчали при ультразвуковому дослідженні (УЗД) за допомогою визначення її товщини під час вдиху та на видиху, амплітуди рухів, фракції стоншення. Візуалізацію діафрагми в досліджуваній групі пацієнтів проводили впродовж здійснення МВЛ на етапах примусової, примусово-допоміжної вентиляції, а також під час спонтанного дихання через 2 год після екстубації, у контрольній групі пацієнтів — під час тесту спонтанного дихання в положенні пацієнта на спині. УЗД виконували в М-режимі, використовуючи ультразвукове вікно печінки чи селезінки. Наявність діафрагмальної дисфункції констатували за вертикальними рухами діафрагми менше 10 мм чи парадоксальними її рухами впродовж МВЛ, при зниженні фракції стоншення менше 30 %.
Результати та обговорення
У здорових осіб екскурсія діафрагми зазвичай є асиметричною і має більшу амплітуду зліва, у нормі відмінності з обох сторін становлять менше 50 % [6]. Дисфункція діафрагми розвивається у 29–80 % пацієнтів, які потребують проведення МВЛ понад 48 год, та часто залишається непідтвердженою [1, 2]. Такі пацієнти мають вірогідно довший загальний час проведення та час відлучення від МВЛ, а також вищу частоту повторного відлучення [2], що підвищує терміни перебування пацієнта у відділі інтенсивної терапії та збільшує витрати коштів на його лікування [4].
Установлено, що низька діафрагмальна активність пов’язана з високими параметрами підтримки при МВЛ та асоціюється з атрофією та дисфункцією діафрагми [7]. Отже, порушення функціонування діафрагми може бути як первинною причиною розвитку дихальної недостатності, так і її наслідком. Необхідно пам’ятати, що м’язи, що беруть участь у процесі дихання, — це лише органи-ефектори, а уражатися можуть і центральна нервова система, і діафрагмальний нерв, і мотонейрони, і нейром’язові синапси. Дистрофія м’язових волокон діафрагми здебільшого є вторинним процесом, котрому сприяє як нутритивний дефіцит, так і довготривала відсутність функціонування діафрагми, що часто пов’язують із використанням міорелаксантів, ушкодженням діафрагмальних нервів або кількох сегментів шийного відділу хребта на рівні C1–C5. Ожиріння, травма, ателектази, запалення нижніх часток легень, плевральний випіт, асцит тощо також впливають на кінетику діафрагми [6].
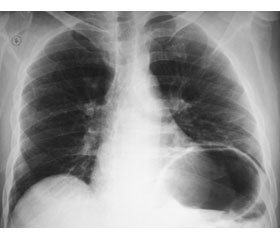
Верифікувати діафрагмальну дисфункцію можна при поєднанні клінічних симптомів (диспное, що більше маніфестує в положенні на спині, труднощі відлучення від оксигенотерапії та від МВЛ, елевація купола діафрагми на рентгенографії органів грудної клітки, непояснювальний респіраторний дистрес, парадоксальне дихання або епізоди повторних пневмоній чи повторюваного унілатерального колапсу легені) та інструментальних даних, що свідчать про порушення функціонування діафрагми [6, 8].
Схематичну будову, топографію діафрагми та її товщину можна вивчити за допомогою даних рентгенографії, комп’ютерної, магнітно-резонансної томографії, проте майже всі ці методики передбачають транспортування пацієнта в радіологічне відділення та балансування між користю діагностики та безпекою для пацієнта. Функцію діафрагми вивчають під час магнітної стимуляції діафрагмальних нервів (за змінами тиску в ендотрахеальній трубці), при визначенні максимального інспіраторного тиску під час спроби спонтанного вдиху та ультрасонографічно за допомогою визначення фракції стоншення діафрагми [1]. Слід визнати, що визначення максимальної сили вдиху та видиху потребує доброї кооперації з пацієнтом. Високі показники цих тисків (зокрема, тиску під час спонтанного вдиху понад 11 см водного стовпа) виключають клінічно значиму дисфункцію дихальних м’язів, проте низькі показники не є специфічними щодо причин їх розвитку та можуть свідчити про погану техніку вимірювання або відсутність кооперації з пацієнтом [7].
Специфічним показником скоротливої здатності діафрагми є трансдіафрагмальний тиск, що можна розрахувати як різницю між тиском у шлунку та в стравоході (Pdi = Pga – Pes). Його використовують для ретельного моніторингу функції діафрагми в пацієнтів із складним відлученням від МВЛ [7]. Тиск у стравоході (Pes) відображає плевральний тиск і може бути використаний для обчислення сумарно роботи, що виконується дихальними м’язами. Золотим стандартом для оцінювання нейрон-респіраторного драйву є діафрагмальна електроміографія У режимі МВЛ NAVA використовується пролонгований моніторинг електроміографічних сигналів. Таким чином, діафрагмальна електроміографія може бути використана для моніторингу навантаження на дихальні м’язи та взаємодії між вентилятором і пацієнтом.
Ультразвукове дослідження стає все більш популярним інструментом для визначення функції діафрагми. Якщо в міжреберному доступі візуалізується зменшення каудальної амплітуди рухів діафрагми під час дихання без допоміжної підтримки, то це вказує на слабкість діафрагми, а її парадоксальні рухи — на парез діафрагми. Діафрагмальна атрофія може бути визначена за допомогою вимірювання товщини діафрагми по середній аксилярній лінії на рівні правого купола діафрагми, а фракція стоншення діафрагми під час вдиху вказує на її здатність до скорочення. Атрофію діафрагми також можна визначити за допомогою комп’ютерної томографії, проте це більш громіздкий метод порівняно з УЗД. У пацієнтів із діафрагмальною атрофією наявна і діафрагмальна дисфункція, а в незначної частини цих пацієнтів товщина діафрагми зростає впродовж проведення МВЛ, що також може бути пов’язано з дисфункцією діафрагми [5].
Корисним може бути УЗД діафрагми при проблемі асинхронізації пацієнта та вентилятора. Найбільш точними та надійними для виявлення асинхронізації є сигнали, що отримані за допомогою езофагеального катетера (за змінами тиску чи електроміограмою). Вивчення езофагеальних сигналів, що відображають електричну активність діафрагми та/або тиск у стравоході, нещодавно дозволило описати обернений тригеринг — вид асинхронізації, коли механічна інсуфляція свіжого газу тригерує повторювані діафрагмальні скорочення. Асинхронізація між пацієнтом та апаратом МВЛ призводить до подовження часу МВЛ, а також часу відлучення. Погана синхронізація часто може провокувати фазові проблеми та призводити до порушення між нейроіндукованим вдихом та часом видиху, а також інсуфляцією апаратом свіжої дихальної суміші та самостійним видихом пацієнта. Така асинхронізація може відбуватися, коли респіраторний драйв пацієнта залишається ще відносно високим (найчастіше при гострій дихальній недостатності). У табл. 1 наведено одну з класифікацій тригерування та циклінгу.
Недостатній циклінг призводить до зростання роботи дихання, асинхронізація — до порушень сну. Крім того, подвійний тригеринг може призводити до надходження вдвічі більшого обсягу дихальної суміші та індукувати перерозтягнення легень і розвиток волюмотравми. Зростання індексу асинхронізації, якщо вона не піддається коригуванню, призводить до підвищення термінів госпіталізації у відділення анестезіології й інтенсивної терапії та госпітальної летальності. Приліжкова діагностика асинхронізації на сьогодні полягає у визначенні трансдіафрагмального тиску, електроміограми з діафрагми, графічного моніторингу тиску в дихальних шляхах та потоку дихальної суміші, автоматизованого програмного забезпечення, що аналізуватиме криві дихання. Проте інспіраторні зусилля пацієнта можна вивчати і за допомогою показників фракції стоншення діафрагми (УЗД), а також неінвазивним методом верифікувати асинхронізацію пацієнта та вентилятора [3]. Методика УЗД є приліжковою, не потребує транспортування пацієнта до радіологічного відділення, може бути виконана багатократно впродовж тривалого часу лікарем інтенсивної терапії.
При обстеженні пацієнтів обох груп ми отримали такі результати: пацієнти досліджуваної та конт–рольної груп вірогідно не відрізнялися за віком, проте середня маса тіла пацієнтів досліджуваної групи була вірогідно нижчою за аналогічний показник у контрольній групі пацієнтів (табл. 2) і становила 10,1 ± 1,1 та 13,1 ± 1,2 кг відповідно. Відтак у 75 % пацієнтів досліджуваної групи виявлено дефіцит маси тіла від 10 до 30 %.
Рівень поліорганної дисфункції в пацієнтів досліджуваної групи оцінювали за шкалою P-MODS, та вона становила 4,2 ± 1,1 бала в досліджуваній групі пацієнтів на етапі МВЛ у режимі PCV; 3,1 ± 0,8 бала (p > 0,05 порівняно з етапом МВЛ у режимі PCV) — на етапі МВЛ у режимі P-SIMV; 1,3 ± 0,3 бала (p ≤ 0,05 порівняно з етапом МВЛ у режимі PCV) — на етапі спонтанного дихання.
/73-77/75-1.jpg)
Вивчаючи функцію діафрагми (табл. 3), ми встановили, що в пацієнтів досліджуваної групи правий купол діафрагми під час вдиху мав вірогідно меншу товщину порівняно з аналогічним показником у контрольній групі пацієнтів, а також вірогідно не відрізнявся за товщиною впродовж усього періоду проведення МВЛ та при спонтанному диханні, і вона становила 4,60 ± 0,15 мм при МВЛ у режимі PCV, 4,40 ± 0,11 мм — при МВЛ у режимі P-SIMV та 4,50 ± 0,06 мм — при спонтанному диханні після екстубації пацієнтів порівняно з 5,90 ± 0,21 мм у контрольній групі пацієнтів. Порівнюючи товщину правого купола діафрагми під час видиху в пацієнтів досліджуваної та контрольної груп, необхідно відмітити, що при МВЛ у режимах PCV та P-SIMV вона залишалася нижчою порівняно з показниками в конт–рольній групі пацієнтів і становила 3,10 ± 0,23 мм та 3,40 ± 0,14 мм відповідно, тоді як при спонтанному диханні пацієнтів досліджуваної групи товщина правого купола діафрагми вірогідно не відрізнялася від такого ж показника в контрольній групі пацієнтів і становила 3,60 ± 0,11 мм та 3,80 ± 0,14 мм відповідно.
/73-77/76-1.jpg)
При порівнянні товщини лівого купола діафрагми простежується така закономірність: під час вдиху в пацієнтів досліджуваної групи він мав більшу товщину на всіх етапах проведення МВЛ порівняно з контрольною групою пацієнтів, що становила 5,10 ± 0,17 мм при МВЛ у режимі PCV, зменшувалася до 4,00 ± 0,12 мм при МВЛ у режимі P-SIMV та до 4,00 ± 0,12 при спонтанному диханні після екстубації порівняно з 3,40 ± 0,04 мм у контрольній групі пацієнтів. А при видиху лівий купол діафрагми мав вірогідно більшу товщину лише при МВЛ у режимі PCV, що становила 3,50 ± 0,12 мм порівняно з 3,10 ± 0,05 мм у контрольній групі пацієнтів (табл. 3).
Показники амплітуди рухів правого та лівого куполів діафрагми в пацієнтів досліджуваної групи залишалися низькими порівняно з контрольною групою пацієнтів і становили відповідно: для правого купола — від 11,2 ± 1,3 мм при МВЛ у режимі PCV та 14,1 ± 1,8 мм при МВЛ у режимі P-SIMV до 13,8 ± 1,6 мм при спонтанному диханні після екстубації порівняно з 16,3 ± 2,1 мм у контрольній групі; для лівого купола діафрагми даний показник був відносно низьким, що можна трактувати як маркер дисфункції діафрагми (табл. 3).
Фракція стоншення правого купола діафрагми в пацієнтів досліджуваної групи була вірогідно нижчою порівняно з даним показником у контрольній групі аж до етапу спонтанного дихання та становила відповідно 0,25 ± 0,04 при проведенні МВЛ у режимі PCV, 0,29 ± 0,02 — при проведенні МВЛ у режимі P-SIMV та 0,38 ± 0,05 — при спонтанному диханні порівняно з 0,50 ± 0,08 у контрольній групі. Фракція стоншення лівого купола діафрагми мала невірогідні відмінності порівняно з контрольною групою пацієнтів, проте цей показник демонстрував кращу скоротливу здатність лівого купола діафрагми порівняно з правим куполом при МВЛ у режимах PCV і P-SIMV.
Найбільша частота десинхронізацій при МВЛ спостерігалася на етапі проведення МВЛ у режимі PCV і усувалася здебільшого корекцією часу вдиху та співвідношення часу вдиху і видиху під УЗ-контролем, що дозволяло уникнути надмірної седації пацієнтів та зробити можливим щоденну оцінку можливостей початку відлучення від МВЛ (табл. 3).
Висновки
Дослідження функції діафрагми за допомогою УЗД дозволяє швидко, неінвазивно та динамічно оцінювати її роботу як одного з основних м’язів системи органів дихання. У всіх пацієнтів із нашого дослідження, які потребували проведення МВЛ, наявні дисфункція правого купола діафрагми, а також порушення релаксації лівого купола діафрагми при збереженій його скоротливій здатності. Робота лівого купола діафрагми вірогідно може робити значний внесок у компенсаторні можливості системи органів дихання при її дисфункції. Ми пропонуємо використовувати в клінічній практиці ті методи визначення функції діафрагмального м’яза, що дозволять лікарю якомога фізіологічніше забезпечувати взаємодію між пацієнтом та апаратом МВЛ, а також прогнозувати ступінь готовності пацієнта дихати самостійно.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів при підготовці даної статті.

/73-77/75-1.jpg)
/73-77/76-1.jpg)