Резюме
Метою роботи було дослідити можливий зв’язок клініко-анамнестичних, інструментальних та лабораторних показників з відновленням функції правого шлуночка (ПШ) за даними 2D-спекл-трекінг-ультразвукової ехокардіографії (2D-СТ-ЕхоКГ) у хворих на гостру тромбоемболію легеневої артерії (ТЕЛА) в динаміці лікування. Матеріали та методи. Обстежені 104 хворі на гостру ТЕЛА. Усім хворим проводили 2D-СТ-ЕхоКГ, показники оцінені в першу добу перебування в стаціонарі та через 3 місяці антикоагулянтної терапії (АКТ), що була призначена при госпіталізації методом конвертів: ривароксабан або варфарин. Резидуальна дисфункція правого шлуночка (ДфПШ) після АКТ встановлена за даними 2D-СТ-ЕхоКГ як сегментарна фракція викиду апікального ПШ сегмента, менша за 65 %, та показник глобальної поздовжньої деформації вільної стінки ПШ, менший за –18,5 %. Результати. Після проведеної АКТ усі обстежені хворі були розподілені на дві групи: до І групи увійшло 13 (12,5 %) хворих із виявленою резидуальною ДфПШ, ІІ групу становив 91 (87,5 %) пацієнт із повним відновленням функції ПШ. Встановлено, що у хворих І групи вірогідно частіше зустрічалися цукровий діабет 2-го типу (р = 0,04) та хронічна серцева або дихальна недостатність (р = 0,03), відмічене збільшення рівнів тропоніну І (р = 0,05), креатиніну (р = 0,009) та фібриногену (р = 0,05), а також зниження швидкості клубочкової фільтрації (р = 0,02) до рівня менше від 60 мл/хв/1,73 м2. Серед пацієнтів ІІ групи вірогідно частіше зустрічались особи, які отримували ривароксабан (р = 0,007), а в І групі хворих — варфарин (р = 0,006). Медіана строку від епізоду ТЕЛА до початку АКТ становила 9,0 доби у ІІ групі та 20,0 доби в І групі, р = 0,03. Висновки. Через три місяці АКТ у 12,5 % хворих на гостру ТЕЛА за даними 2D-CT-ЕхоКГ зберігається резидуальна ДфПШ. Це порушення, за даними регресійного аналізу, на 62,6 % обумовлене наявністю таких чинників, як використання варфарину, строк до початку лікування понад 9 діб, наявність цукрового діабету 2-го типу та зниження швидкості клубочкової фільтрації до рівня менше від 60 мл/хв/1,73 м2.
Целью работы было исследовать возможную связь клинико-анамнестических, инструментальных и лабораторных показателей с восстановлением функции правого желудочка (ПЖ) по данным 2D-спекл-трекинг-ультразвуковой эхокардиографии (2D-СТ-ЭхоКГ) у больных острой тромбоэмболией легочной артерии (ТЭЛА) в динамике лечения. Материалы и методы. Обследованы 104 больных с острой ТЭЛА. Всем больным проводили 2D-СТ-ЭхоКГ, показатели оценены в первые сутки пребывания в стационаре и через 3 месяца антикоагулянтной терапии (АКТ), которая была назначена при госпитализации методом конвертов: ривароксабан или варфарин. После проведения АКТ резидуальная дисфункция правого желудочка (ДфПЖ) была верифицирована по данным 2D-СТ-ЭхоКГ как сегментарная фракция выброса апикального ПЖ сегмента меньше 65 % и показатель глобальной продольной деформации свободной стенки ПЖ меньше –18,5 %. Результаты. После проведенной АКТ все обследованные больные были разделены на две группы: в I группу вошли 13 (12,5 %) больных с выявленной резидуальной ДфПЖ, II группу составил 91 (87,5 %) пациент с полным восстановлением функции ПЖ. Установлено, что в I группе достоверно чаще встречались сахарный диабет 2-го типа (р = 0,04) и хроническая сердечная или дыхательная недостаточность (р = 0,03), отмечено повышение уровней тропонина I (р = 0,05), креатинина (р = 0,009) и фибриногена (р = 0,05), а также снижение скорости клубочковой фильтрации (р = 0,02) до уровня менее 60 мл/мин/1,73 м2. Среди пациентов II группы достоверно чаще встречались лица, получавшие ривароксабан (р = 0,007), а в I группе больных — варфарин (р = 0,006). Медиана срока от эпизода ТЭЛА до начала АКТ составила 9,0 суток во II группе и 20,0 суток в первой группе, р = 0,03. Выводы. Через три месяца АКТ у 12,5 % больных с острой ТЭЛА по данным 2D-CT-ЭхоКГ сохраняется резидуальная ДфПЖ. Это нарушение, по данным регрессионного анализа, на 62,6 % обусловлено наличием таких факторов, как использование варфарина, срок до начала лечения больше 9 суток, наличие сахарного диабета 2-го типа и уменьшение скорости клубочковой фильтрации до уровня менее 60 мл/мин/1,73 м2.
Background. The purpose was to investigate the possible relation between anamnestic, instrumental and laboratory indicators and restoration of right ventricular (RV) function according to 2D speckle tracking echocardiography (2D STE) in patients with acute pulmonary embolism (PE) in the dynamics of treatment. Materials and methods. The study involved 104 patients with acute PE. All patients were examined using 2D STE, indicators were assessed on the first day of hospital stay and after 3 months of anticoagulant therapy (ACT), which was prescribed during hospitalization by envelope method: rivaroxaban or warfarin. After ACT and according to 2D-STE, residual RV dysfunction has been determined as a segmental ejection fraction of the apical RV segment less than 65 %, and the global longitudinal strain of the free RV wall is less than 18.5 %. Results. After ACT, all the examined patients were divided into two groups: group I included 13 (12.5 %) persons with residual RV dysfunction, group II consisted of 91 (87.5 %) patients with complete restoration of RV function. It was found that type 2 diabetes mellitus (p = 0.04) and chronic cardiac or respiratory failure (p = 0.03) were significantly more likely in the group I; an increase in troponin I (p = 0.05), creatinine (p = 0.009) and fibrinogen (p = 0.05) levels were noted, as well as a decrease in the glomerular filtration rate (p = 0.02) to less than 60 ml/min/1.73 m2. Among patients in group II, significantly more persons received rivaroxaban (p = 0.007), and in the group I — warfarin (p = 0.006). The median of the period from the PE episode to the ACT initiation was 9.0 days in second group and 20.0 days in the first group, p = 0.03. Conclusions. After three months of ACT, residual RV dysfunction remains in 12.5 % of patients with acute PE according to 2D STE. According to the regression analysis, in 62.6 % of cases this failure was determined by the presence of such factors, as warfarin therapy, the treatment start date more than 9 days, the presence of type 2 diabetes mellitus and a decrease in the glomerular filtration rate to less than 60 ml/min/1.73 m2.
Вступ
Дисфункція правого шлуночка (ДфПШ) у хворих на гостру тромбоемболію легеневих артерій (ТЕЛА), за даними міжнародних регістрів ICOPER та MAPPED, є найбільш значимим предиктором внутрішньогоспітальної летальності та одним із найвагоміших факторів, що впливають на короткостроковий та віддалений прогноз [7, 10]. Слід підкреслити, що, за даними регістру ICOPER, застосування такого методу лікування, як тромболітична терапія (ТЛТ), не мало впливу як на частоту рецидивів емболії, так і на зниження 90-денної летальності навіть у пацієнтів високого ризику ранньої смерті від ТЕЛА [7].
Порушення гемодинаміки при ТЕЛА пов’язані як із механічною обтурацією легеневих судин тромбоемболами, так і з потужним вазоспазмом унаслідок вивільнення тромбоксану А2 та серотоніну [17]. Перевантаження правого шлуночка (ПШ) об’ємом призводить до його дилатації з короткочасним збільшенням скорочувальної здатності за рахунок механізму Франка — Старлінга, а також унаслідок іно- та хронотропної стимуляції [14]. Непрекондиційований ПШ на тлі підвищеної потреби в кисні та зниження градієнта коронарної перфузії дуже швидко декомпенсується з розвитком ДфПШ [14].
Вивільнення нейрогормональних медіаторів та активація запального процесу також розглядаються як провідні причини, що призводять до ДфПШ [17, 20]. В експериментальній моделі ТЕЛА показано, що експресія прозапальних генів (підвищення концентрації цитокін-індукованого хемоатрактанту нейтрофілів-1 та циклооксигенази-2) визначається вже через 6 годин після початку захворювання, через 12 годин значно підвищується активація молекул адгезії (селектин Е та молекули міжклітинної адгезії) [20]. Цей процес, поряд із прозапальною експресією цитокінів (інтерлейкін-6, інтерлейкін-8 і білок хемоатрактанту моноцитів-1) фібробластами, лімфоцитами та ендотеліальними клітинами, обумовлює трансендотеліальну міграцію фібробластів, сприяє їх диференціації в міофібробласти та проліферації гладком’язових клітин ендотелію, що сприяє патологічному ремоделюванню не тільки легеневих артеріол, але й венозних легеневих судин, призводить до прогресування запалення, вазоспазму та фіброзу [8, 15, 21].
Ультразвукова 2D-спекл-трекінг-ехокардіогра–фія (2D-CT-ЕхоКГ) є перспективним методом кількісної оцінки посегментарної скорочуваності ПШ. Цей метод дозволяє об’єктивізувати ДфПШ, що є важливим для стратифікації ризику та визначення тактики лікування при першому контакті з хворим, а також дає змогу оцінити ступінь відновлення функціонального стану ПШ та ефективність антикоагулянтної терапії (АКТ) [6, 11]. Найбільш інформативними показниками 2D-СТ-ЕхоКГ щодо встановлення ДфПШ у хворих на гостру ТЕЛА є сегментарна фракція викиду апікального правошлуночкового сегмента (сегментарна ФВ АПшС), менша за 65 % (чутливість 64,9 %, специфічність 100 %, р < 0,0001), та показник глобальної правошлуночкової поздовжньої деформації вільної стінки правого шлуночка (глобальний стрейн ПШ), менший за –18,5 % (чутливість 72,5 % та специфічність 85,7 %, р < 0,0001) [19].
Метою роботи було дослідити можливий зв’язок клініко-анамнестичних, інструментальних та лабораторних показників із відновленням функції правого шлуночка за даними 2D-СТ-ЕхоКГ у хворих на гостру ТЕЛА в динаміці лікування.
Матеріали та методи
Обстежені 104 хворі, середній вік яких становив 62,9 ± 13,5 року, які послідовно були госпіталізовані до КЗОЗ «Харківська міська клінічна лікарня № 8» з 1 вересня 2014 року по 1 квітня 2016 року з діагнозом гострої ТЕЛА, що була верифікована за допомогою мультиспіральної комп’ютерної томографічної ангіографії легеневих артерій (МКТ ангіографія ЛА). Загальна характеристика обстежених хворих наведена в табл. 1.
Окрім проведення загальноклінічного обстеження, усім хворим оцінювали клінічну вірогідність ТЕЛА за переглянутим Женевським алгоритмом (оригінальна версія) [13], проводили стратифікацію раннього ризику смерті від ТЕЛА [1] та давали оцінку прогнозу хворого за шкалою індексу тяжкості ТЕЛА PESI (оригінальна версія) [4].
Визначення в крові маркера пошкодження міокарда тропоніну І проводилося імунохемілюмінесцентним методом за допомогою аналізатора Tosoh AIA2000 (Японія). Визначення рівня креатиніну проводили кінетичним методом за допомогою автоматичного біохімічного аналізатора ABX Pentra 400 (Horiba ABX, Франція), визначали швидкість клубочкової фільтрації (ШКФ) розрахунковим методом за формулою MDRD [16]. Рівень фібриногену визначали коагулометричним методом за допомогою автоматичного біохімічного аналізатора Sysmex CA 1500 (Японія). Визначення рівня тромбоцитів проводили методом потокової цитофлуориметрії з використанням лазерних напівпровідників і гідродинамічного фокусування за допомогою автоматичного гематологічного аналізатора ABX Pentra DF 120 (Horiba ABX, Франція). Вищенаведені лабораторні показники були оцінені в першу добу перебування в стаціонарі. Міжнародне нормалізоване відношення (МНВ) визначали з використанням тромбопластину (Thromboplastin-SI, Human, Австрія) з міжнародним індексом чутливості (МІЧ) 1,1 (за паспортом) на автоматичному коагулометрі Sysmex CA 1500 (Японія). Розрахунок МНВ проводили зведенням у степінь МІЧ відношення протромбінового часу (ПТЧ) пацієнта до ПТЧ контрольної плазми (Control Plasma Normal, Lot 17675).
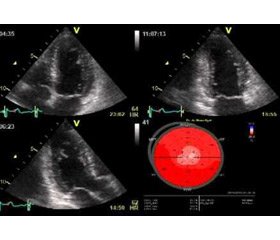
Усім хворим виконували ЕхоКГ на апараті Acuson X2000 (Siemens, Німеччина) з використанням датчика з частотою ультразвуку 3,0 МГц за стандартним протоколом. Вимірювали розміри лівого та правого передсердя, кінцевий систолічний та діастолічний розмір лівого шлуночка, розміри ПШ, фракцію викиду (ФВ) лівого шлуночка за Сімпсоном. Також визначали середній тиск у легеневій артерії за відношенням часу прискорення кровотоку у вихідному тракті ПШ до часу вигнання крові з ПШ [6, 11]. Усім хворим проводили 2D-спекл-трекінг-ехокардіографію за допомогою Syngo® Velocity Vector Imaging™ Technology на апараті ACUSON X2000 (Siemens, Німеччина). Проводили оцінювання сегментарної ФВ АПшС та розраховували глобальний стрейн ПШ. Показники ЕхоКГ та 2D-CT-ЕхоКГ були оцінені в першу добу перебування в стаціонарі та через 3 місяці АКТ.
МКТ ангіографію ЛА проводили в строки від декількох годин до 14 діб до включення хворих у дане дослідження на комплексі Somatom Definition AS 64 (Siemens, Німеччина) за стандартним протоколом із використанням внутрішньовенного контрастування томогексолом-350, 50 мл. Наявність ТЕЛА за даними МКТ ангіографії ЛА визначали за знаходженням дефектів контрастування, що частково та/або повністю перекривали просвіт бодай однієї з гілок легеневої артерії. Проводили кількісну оцінку розмірів легеневого стовбура та легеневих артерій та визначали характер поширення ураження гілок легеневих артерій [9].
При госпіталізації хворих на ТЕЛА антикоагулянту терапію призначали методом конвертів: ривароксабан отримали 57 (54,8 %) пацієнтів, варфарин — 47 (45,2 %) хворих. Ривароксабан призначали 15 мг двічі на добу протягом 21 дня, потім 20 мг на добу. Титрування дози варфарину проводили на тлі призначення еноксапарину в дозі 1 мг/кг двічі на добу до досягнення цільового значення міжнародного нормалізованого відношення протягом двох діб поспіль. За необхідності (швидкість клубочкової фільтрації менше ніж 40 мл/хв/1,73 м2 та вік старше за 75 років) доза еноксапарину була скоригована. Згідно з рекомендаціями ESC 2014 пацієнтам з ТЕЛА високого ризику ранньої смерті провели тромболітичну терапію (ТЛТ) у 45 (42,3 %) випадках [1]. У 34 (75,6 %) хворих тромболітичним агентом була стрептокіназа, в 11 (24,4 %) застосували актилізе, 9 (20 %) пацієнтам тромболітик вводили двічі. До початку терапії ривароксабаном за означеною вище схемою після проведеної ТЛТ хворі отримували еноксапарин протягом 5 діб. Варфарин на тлі введення еноксапарину був призначений на другу добу після ТЛТ. Пацієнтам, яким не проводилася ТЛТ, одразу призначали або ривароксабан, або варфарин на тлі введення еноксапарину. Тривалість антикоагулянтної терапій щонайменше становила 3 місяці, середня тривалість — 4,2 ± 1,9 місяця. Пацієнтам, які приймали варфарин, МНВ визначали не рідше від одного разу на 2 тижні, частка утримання показника в межах терапевтичного діапазону становила 81,9 %. У всіх пацієнтів проводили розрахунок комплаєнсу як відсотка фактично прийнятого препарату до розрахованої належної кількості, що становив у І групі 94,8 %, а у ІІ — 96,4 %.
Залежно від результатів 2D-CT-ЕхоКГ, що були отримані через три місяці АКТ, обстежені нами хворі були розподілені на дві групи: до І групи ввійшло 13 (12,5 %) хворих, у яких сегментарна ФВ АПшС була меншою за 65 % та показник глобального стрейну ПШ був менший за –18,5 %, що було визначене як наявність резидуальної ДфПШ. До ІІ групи ввійшов 91 (87,5 %) пацієнт, у них на тлі терапії відбулося повне відновлення функції ПШ, про що свідчили показник сегментарної ФВ АПшС, більший за 65 %, і/або показник глобального стрейну ПШ, більший за –18,5 %. Слід зазначити, що обидві групи за всіма показниками внутрішньосерцевої гемодинаміки, які оцінювалися під час госпіталізації за даними ЕхоКГ, були статистично порівнянними.
Статистичну обробку отриманих даних проводили з використанням пакета статистичних програм Statistica 10.0 (StatSoft Inc., США), Microsoft Office Exсel 2013. Оскільки при попередньому аналізі кількісних ознак відхилень від нормального розподілу не виявлено, вони подані у вигляді «середнє ± стандартне відхилення» (М ± σ), для порівняння середніх двох вибірок використовували Mann — Whitney U-test. Міжгрупові відмінності якісних ознак оцінювали з використанням критерію χ2 Пірсона з поправкою Йетса для малих вибірок. Для усіх видів аналізу відмінності вважали статистично значимими при р < 0,05. Для виявлення зв’язку між показниками, що вивчали, проводили багатофакторний регресійний аналіз та розраховували стандартизовані регресійні коефіцієнти бета та звичайні регресійні коефіцієнти В, які дозволяють порівняти відносний внесок кожної незалежної змінної в передбачення залежної змінної. Коефіцієнти регресії вважали статистично значимими при р < 0,05.
Результати
При проведенні порівняльного аналізу встановлено, що хворі І групи, у яких через три місяці АКТ за даними 2D-CT-ЕхоКГ була наявна резидуальна ДфПШ, вірогідно частіше страждали від цукрового діабету 2-го типу, ніж пацієнти ІІ групи: 4 (30,7 %) проти 9 (9,9 %), χ2 = 4,12; р = 0,04. Також у І групі вірогідно частіше, ніж у ІІ групі, зустрічався такий фактор ризику виникнення венозного тромбоемболізму, як хронічна серцева або дихальна недостатність: 6 (45,8 %) проти 16 (17,6 %), χ2 = 4,25; р = 0,03 (табл. 2). За іншими клініко-анамнестичними показниками, що оцінювались, обстежені групи хворих були статистично порівнянними (табл. 2).
/93-1.jpg)
Як показали результати проведеного лабораторного обстеження, у І групі рівень тропоніну І у першу добу після госпіталізації становив 0,06 ± 0,01 мг/мл та був вірогідно вищим, ніж у ІІ групі — 0,04 ± 0,02 нг/мл, р = 0,05. Отримані нами дані збігаються з даними метааналізу, у якому підвищення рівня тропоніну відмічалось у 50 % хворих на ТЕЛА та свідчило про наявність пошкодження міокарда ПШ, асоціювалось з наявністю ДфПШ та погіршенням прогнозу навіть у пацієнтів зі стабільною гемодинамікою [12].
Середній рівень креатиніну (табл. 3) у І групі порівняно з ІІ був вірогідно вищим та становив 131,6 ± 29,3 мкмоль/л проти 102,0 ± 33,7 мкмоль/л, р = 0,009. У групі пацієнтів з наявністю резидуальної ДфПШ середній рівень ШКФ, розрахованої за формулою MDRD, був вірогідно нижчим, ніж у пацієнтів ІІ групи: 42,8 ± 14,2 мл/хв/1,73 м2 проти 62,3 ± 20,9 мл/хв/1,73 м2, р = 0,01. У хворих із рівнем ШКФ, меншим за 60 мл/хв/1,73 м2, середній показник у І групі становив 36,4 ± 9,4 мл/хв/1,73 м2 та був вірогідно нижчим, ніж у ІІ групі, — 43,3 ± 11,2 мл/хв/1,73 м2, р = 0,02, але відмінностей між групами встановлено не було: 9 (69,2 %) у І групі проти 56 (61,5 %) у ІІ, χ2 = 0,29, р = 0,6. Отримані нами дані узгоджуються з результатами дослідження B. Altınsoy та співавт., у якому доведена наявність зв’язку між порушенням функції нирок та короткостроковим прогнозом у хворих на ТЕЛА та запропоновано використовувати ШКФ як додатковий прогностичний маркер у пацієнтів помірного ризику [3].
Також, як показали результати лабораторного обстеження, вірогідно вищим у І групі, ніж у ІІ групі хворих, був рівень фібриногену: 3,8 ± 2,6 г/л проти 3,4 ± 1,5 г/л, р = 0,05. Подібні дані були отримані в проспективному спостереженні М. Bohacekova et al., у якому були виділені фактори ризику розвитку хронічної посттромбоемболічної легеневої гіпертензії, зокрема збільшення рівнів фібриногену та фактора фон Віллебранда, зниження рівня тромбоцитів зі збільшенням їх середнього об’єму та спонтанна агрегація тромбоцитів [4].
Установлено, що час від епізоду ТЕЛА до початку АКТ у ІІ групі хворих, у яких через три місяці лікування, за даними 2D-CT-ЕхоКГ, відбулося повне відновлення функції ПШ, становив 11,45 ± 9,60 доби та був вірогідно меншим, ніж у І групі — 18,3 ± 11,0 доби, р = 0,03 (табл. 4). Для показника терміну госпіталізації хворих на ТЕЛА була розрахована медіана для обох груп, що становила 9,0 [3,0–14,0] доби у ІІ групі та 20,0 [10,0–30,0] доби в І групі. Серед проаналізованих нами вірогідних причин щодо затримки початку АКТ було звернення хворих після 9-ї доби (9 (69,2 %) осіб у І групі проти 31 (34,0 %) у ІІ групі, χ2 = 4,5, р = 0,02) та об’єктивні діагностичні труднощі (4 (30,7 %) особи в І групі проти 5 (5,5 %) у ІІ групі, χ2 = 6,2, р = 0,01).
/94-1.jpg)
При проведенні порівняльного аналізу встановлено, що в І групі хворих вірогідно частіше, ніж у ІІ, зустрічалися пацієнти, яким було призначено варфарин: 9 (69,2 %) проти 22 (24,2 %), χ2 = 7,54; р = 0,006. Серед пацієнтів, у яких через три місяці лікування відбулося, за даними 2D-CT-ЕхоКГ, повне відновлення функції ПШ, вірогідно частіше зустрічались особи, які отримували ривароксабан: 69 (75,8 %) проти 4 (30,8 %) у групі пацієнтів з наявністю резидуальної ДфПШ, χ2 = 7,14; р = 0,007 (табл. 4). Найбільш вірогідним поясненням отриманих нами результатів може бути наявність у ривароксабану плейотропних ефектів, зокрема протизапального. В експериментальних роботах C.T. Esmon, Q. Zhou et al. та Р. Zuo et al. доведено, що активований фактор Х (FXa), прямим інгібітором якого є ривароксабан, також діє як потужний індуктор прозапальної експресії цитокінів клітинами ендотелію через рецептори, що активуються протеазами, 2-го типу (protease-activated receptor, PAR-2) [6, 21, 22]. Це призводить до проліферації ендотеліальних гладком’язових клітин та сприяє патологічному ремоделюванню легеневих артеріол та венул, –обумовлює прогресування запалення та фіброзу [8, 15, 21]. Особливістю механізму дії антагоністів вітаміну К, до яких належить варфарин, є утворення біологічно неактивної форми PIVKA-FXa, що не може адекватно продовжити каскад згортання крові, але зберігає здатність активувати PAR-2. На відміну від варфарину ривароксабан повністю інактивує FXa, що припиняє як перетворення протромбіну в тромбін, так і FXa-обумовлену активацію PAR-2 [18]. У пацієнтів, що отримують варфарин, забезпечується антикоагулянтний ефект, але синтезований PIVKA-FXa зберігає здатність активувати PAR-2, що запускає прозапальний каскад, на той час як у пацієнтів, які отримують прямий пероральний інгібітор FХа, пригнічується як коагуляція, так і активація PAR-2. Таким чином реалізується плейотропний протизапальний ефект ривароксабану, який може пояснити більш ефективне відновлення скорочувальної функції правого шлуночка.
З метою виявлення незалежних чинників, що можуть впливати на відновлення функції ПШ у хворих на ТЕЛА, нами був проведений покроковий регресійний аналіз (табл. 5). Отримана вірогідна регресійна модель (p < 0,05), згідно з якою відносний внесок щодо наявності резидуальної ДфПШ у обстежених хворих на ТЕЛА таких показників, як використання як антикоагулянтного агента варфарину, становить 17,7 % (р = 0,05), затримка початку АКТ більше ніж на 9 діб (за розрахованою медіаною) від епізоду ТЕЛА — 16,7 % (р = 0,05), наявність цукрового діабету 2-го типу — 15,1 % (р = 0,02) та швидкість клубочкової фільтрації менше за 60 мл/хв/1,73 м2 — 13,1 % (р = 0,05).
/95-1.jpg)
Отже, згідно з результатами нашого дослідження, у 12,5 % хворих на гостру ТЕЛА через три місяці антикоагулянтної терапії за даними 2D-CT-ЕхоКГ зберігається дисфункція правого шлуночка. У цій групі хворих вірогідно частіше зустрічалися цукровий діабет 2-го типу та хронічна серцева або дихальна недостатність, відмічалось збільшення рівнів тропоніну І, креатинину та фібриногену, а також зниження швидкості клубочкової фільтрації до рівня менше ніж 60 мл/хв/1,73 м2.
З огляду на отримані дані регресійного аналізу більш ефективною щодо відновлення функції правого шлуночка у хворих на гостру ТЕЛА є антикоагулянтна терапія з використанням прямого інгібітору активованого фактора Х ривароксабану, особливо за наявності у хворих цукрового діабету 2-го типу, зниження швидкості клубочкової фільтрації до рівня менше ніж 60 мл/хв/1,73 м2 та при затримці початку антикоагулянтної терапії більше ніж на 9 діб.
Висновки
1. Доведено, що через три місяці антикоагулянтної терапії у 12,5 % хворих на гостру тромбоемболію легеневої артерії за даними 2D-CT-ЕхоКГ зберігається дисфункція правого шлуночка.
2. За даними регресійного аналізу, у хворих на гостру тромбоемболію легеневої артерії через 3 місяці проведення антикоагулянтної терапії резидуальна дисфункція правого шлуночка на 62,6 % обумовлена такими чинниками, як використання варфарину, строк до початку лікування понад 9 діб, наявність цукрового діабету 2-го типу та зниження швидкості клубочкової фільтрації до рівня менше від 60 мл/хв/1,73 м2.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів при підготовці даної статті.
Автор висловлює велику вдячність завідувачці кафедри кардіології та функціональної діагностики ХМАПО, д.м.н., професору, заслуженому діячу науки та техніки України Вірі Йосипівні Целуйко, професору кафедри кардіології та функціональної діагностики ХМАПО, д.м.н. Ларисі Миколаївні Яковлевій та доценту кафедри кардіології та функціональної діагностики ХМАПО, к.м.н. Костянтину Юліановичу Кіношенко.
Список литературы
1. Целуйко В.Й. та ін. Діагностичні можливості 2D-спекл-трекінг ехокардіографії щодо оцінки функції правого шлуночка у хворих на гостру тромбоемболію легеневої артерії / Целуйко В.Й., Яковлева Л.Н., Кіношенко К.Ю., Сухова С.М. // Серце і судини. — 2017. — № 1. — С. 26-32.
2. 2014 ESC Guidelines on the diagnosis and management of acute pulmonary embolism. The Task Force for the Diagnosis and Management of Acute Pulmonary Embolism of the Euro–pean Socie–ty of Cardiology // European Heart Journal. — 2014, Vol. 35 — № 43. — Р. 3033-3073 doi:10.1093/eurheartj/ehu283.
3. Altınsoy B. et al. Prognostic Value of Renal Dysfunction Indicators in Normotensive Patients with Acute Pulmonary Embolism / Altınsoy B., Öz İ.İ., Örnek T., Erboy F., Tanrıverdi H., Uygur F., Altintas N., Atalay F., Tor M.M. // Clinical and applied thrombosis hemostasis. — 26 Mar 2016. doi:10.1177/1076029616637440.
4. Bohacekova M. et al. Risk factors detection in chronic thromboembolic pulmonary hypertension, a tool for risk quantification? / Bohacekova M., Kaldararova M., Valkovicova T., Remkova A., Vesely J., Simkova I. // Bratislava Medical Journal. — 2016. — Vol. 117, № 10. — Р. 577-582. doi:10.4149/bll_2016_112
5. Donze J. et al. Prospective validation of the Pulmonary Embolism Severity Index. A clinical prognostic model for pulmonary embolism / Donzé J., Le Gal G., Fine M.J., Roy P.M., Sanchez O., Verschuren F., Cornuz J., Meyer G., Perrier A., Righini M., Aujesky D. // Journal of Thrombosis and Haemostasis. — 2008. — Vol. 100, № 5. — P. 943-948. doi:10.1160/TH08-05-0285
6. Esmon C.T. Targeting factor Xa and thrombin: impact on coagulation and beyond // Journal of Thrombosis and Haemostasis. — 2014. — Vol. 111. — Р. 625-633. doi:10.1160/TH13-09-0730
7. Feigenbaum H. Echocardiography. — Lippincott Williams & Wilkins, 2012. — 785 р. ISBN/ISSN: 9780781795579
8. Goldhaber S.Z., Visani L., De Rosa M. Acute pulmonary embolism: clinical outcomes in the International Cooperative Pulmonary Embolism Registry (ICOPER) // Lancet. — 1999. — Vol. 353, № 9162. — Р. 1386-9.
9. Goto M. et al. Rivaroxaban, a factor Xa inhibitor, induces the secondary prevention of cardiovascular events after myocardial ischemia reperfusion injury in mice / Goto M., Miura S., Suematsu Y., Idemoto Y., Takata K., Imaizumi S., Uehara Y., Saku K. // International Journal of Cardiology. — 2016. — Vol. 220 — Р. 602-607. doi: 10.10.2016.06.212.
10. Hofer М. CT Teaching Manual: A Systematic Approach to CT Reading. 4th edition. — MEDIDAK Publishing GmbH, 2013. — Р. 367.
11. Kasper W. et al. Management Strategies and Determinants of Outcome in Acute Major Pulmonary Embolism: Results of a Multicenter Registry / Kasper W., Konstantinides S., Geibel А., Olschewski М., Heinrich F., Grosser K.D., Rauber K., Iversen S., Redecker M., Kienast J. // J. Am. Coll. Cardiol. — 1997. — Vol. 30, № 5. — Р. 1165-1171. doi:10.1016/S0735-1097(97)00319-7.
12. Kossaify A. Echocardiographic Assessment of the Right Ventricle, from the Conventional Approach to Speckle Tracking and Three-Dimensional Imaging, and Insights into the «Right Way» to Explore the Forgotten Chamber // Journal Clinical Me–dicine Insights: Cardiology. — 2015. — Vol. 9. — P. 65-75. doi: 10.4137/cmc.s27462.
13. Lankeit M. et al. Predictive value of the high-sensitivity troponin T assay and the simplified pulmonary embolism severity index in hemodynamically stable patients with acute pulmonary embolism: a prospective validation study / Lankeit M., Jimenez D., Kostrubiec M., Dellas C., Hasenfuss G., Pruszczyk P., Konstantinides S. // Circulation. — 2011. — Vol. 124, № 24. — Р. 2716-2724. doi: 10.1161/circulationaha.111.051177.
14. Le Gal G. et al. Prediction of pulmonary embolism in the emergency department: the revised Geneva score / Le Gal G., Righini M., Roy P.M., Sanchez O., Aujesky D., Bounameaux H., Perrier A. // Annals of Internal Medicine. — 2006. — Vol. 144, № 3. — P. 165-171. doi:10.7326/0003-4819-144-3-200602070-00004.
15. Marcus J.T. et al. Interventricular mechanical asynchrony in pulmonary arterial hypertension: left-to-right delay in peak shortening is related to right ventricular overload and left ventricular underfilling / Marcus J.T., Gan C.T., Zwanenburg J.J., Boonstra A., Allaart C.P., Gotte M.J., Vonk-Noordegraaf A. // Journal of the American College of Cardiology. — 2008. — Vol. 51, № 7. — Р. 750-757. doi: 10.1016/j.jacc.2007.10.041.
16. Rosenkranz A.C., Schrör K., Rauch B.H. Direct inhibitors of thrombin and factor Xa attenuate clot-induced mitogenesis and inflammatory gene expression in human vascular smooth muscle cells // Journal of Thrombosis and Haemostasis. — 2011. — Vol. 106, № 3. — Р. 561-562. doi: 10.1160/TH11-04-0275.
17. Schück O. et al. A new method to estimate glomerular filtration rate based on serum concentration of creatinine, urea and albumin (MDRD, Modification of Diet in Renal Disease) / Schück O., Smrcková J., Teplan V., Stávek P., Skibová J., Stol–lová M. // Vnitr̆ní lékar̆ství. — 2004. — Vol. 50, № 7. — P. 507-509. PMID: 15323257.
18. Smulders Y.M. Pathophysiology and treatment of haemodynamic instability in acute pulmonary embolism: the pivotal role of pulmonary vasoconstriction // Cardiovascular Research. — 2000. — Vol. 48, № 1. — Р. 23-33. doi: 10.1016/S0008-6363(00)00168-1.
19. Spronk H., de Jong A.M., Crijns H.J. Pleiotropic effects of factor Xa and thrombin: what to expect from novel anticoagulants // Cardiovascular Research. — 2014. — Vol. 101. — Р. 344-351. doi:10.1093/cvr/cvt343.
20. Watts J.A. et al. Proinflammatory events in right ventricular damage during pulmonary embolism: effects of treatment with ketorolac in rats / Watts J.A., Gellar M.A., Stuart L.K., Obraztsova M., Kline J.A. // Journal of Cardiovascular Pharmacology. — 2009. — Vol. 54, № 3. — Р. 246-252. doi: 10.1097/fjc.0b013e3181b2b699.
21. Zhou Q., Bea F., Preusch М. Evaluation of Plaque Stability of Advanced Atherosclerotic Lesions in Apo E-Deficient Mice after Treatment with the Oral Factor Xa Inhibitor Rivaroxaban // Mediators of Inflammation. — 2011. — Vol. 2011. — Art. ID 432080, 9 p. doi: 10.1155/2011/432080.
22. Zuo P., Zuo Z., Wang X. Factor Xa induces pro-inflammatory cytokine expression in RAW 264.7 macrophages via protease-activated receptor-2 activation // American Journal of Translational Research. — 2015. — Vol. 7, № 11. — Р. 2326-2334. doi: 10.1943-8141/ajtr0014456.

/92-1.jpg)
/93-1.jpg)
/94-1.jpg)
/95-1.jpg)