Резюме
Актуальність. Неспецифічний біль у спині — найчастіша скарга після невеликих травм і гострих респіраторних захворювань та провідна причина обмеження фізичної активності пацієнтів молодше 45 років. Це захворювання продовжує залишатися соціально значущою медичною проблемою внаслідок як тривалої непрацездатності цієї групи пацієнтів, так і високої вартості лікування. Мета: оцінити ефективність епідуральної інфільтрації місцевими анестетиками і глюкокортикостероїдами при неспецифічному болі в спині, пов’язаному з дегенеративно-дистрофічним ураженням різних відділів хребта, та визначити її вплив на покращання якості життя таких хворих. Матеріали та методи. Проаналізовані результати лікування 71 пацієнта віком від 36 до 74 років, які перебували в Центрі лікування болю та неврологічному відділенні КЗОЗ «Харківська обласна клінічна лікарня — Центр екстреної медичної допомоги та медицини катастроф» із 2016 по 2017 рік із приводу хронічного неспецифічного болю в спині. Пацієнти були розподілені на 2 групи: основну — 38 осіб, яким як монотерапію епідурально вводили розчин глюкокортикостероїду та місцевого анестетика, та контрольну — 33 пацієнти, яким проводили стандартне консервативне лікування. Результати. У результаті проведеної терапії пацієнти відчували зменшення болю в спині, покращання загального самопочуття та якості життя. Однак через 6 тижнів після лікування рівень болю в групі пацієнтів, які отримувала епідуральні ін’єкції, був нижчим у 1,7 раза порівняно зі стандартною терапією. Покращання життєдіяльності та загального функціонування в два рази порівняно з результатами до лікування спостерігалось в основній групі через 3 тижні після початку терапії, у той час як пацієнти контрольної групи не досягли такого результату навіть через 6 місяців після лікування. Висновки. Проведене дослідження показало доцільність використання епідуральних ін’єкцій розчину глюкокортикоїду та місцевого анестетика в пацієнтів із хронічним неспецифічним болем у спині в моделюванні больового синдрому.
Актуальность. Неспецифическая боль в спине — наиболее частая жалоба после небольших травм и острых респираторных заболеваний и ведущая причина ограничения физической активности пациентов моложе 45 лет. Это заболевание продолжает оставаться социально значимой медицинской проблемой вследствие как длительной нетрудоспособности этой группы пациентов, так и высокой стоимости лечения. Цель: оценить эффективность эпидуральной инфильтрации местными анестетиками и глюкокортикостероидами при неспецифической боли в спине, связанной с дегенеративно-дистрофическим поражением различных отделов позвоночника, и определить ее влияние на улучшение качества жизни таких больных. Материалы и методы. Проанализированы результаты лечения 71 пациента в возрасте от 36 до 74 лет, находившихся в Центре лечения боли и неврологическом отделении КУЗ «Харьковская областная клиническая больница — Центр экстренной медицинской помощи и медицины катастроф» с 2016 по 2017 год по поводу хронической неспецифической боли в спине. Пациенты были разделены на 2 группы: основную — 38 человек, которым в качестве монотерапии эпидурально вводили раствор глюкокортикостероида и местного анестетика, и контрольную — 33 пациента, которым проводили стандартное консервативное лечение. Результаты. В результате проведенной терапии пациенты чувствовали уменьшение боли в спине, улучшение общего самочувствия и качества жизни. Однако через 6 недель после лечения уровень боли в группе пациентов, получавшей эпидуральные инъекции, был ниже в 1,7 раза по сравнению с контрольной группой. Улучшение жизнедеятельности и общего функционирования в два раза по сравнению с результатами до лечения наблюдалось в основной группе через 3 недели после начала терапии, в то время как пациенты контрольной группы не достигли такого результата даже через 6 месяцев после лечения. Выводы. Проведенное исследование показало целесообразность использования эпидуральных инъекций раствора глюкокортикостероида и местного анестетика у пациентов с хронической неспецифической болью в спине в моделировании болевого синдрома.
Background. Chronic nonspecific back pain is a common and cost-intensive musculoskeletal syndrome in young working-age people around the world. The aim of research was to evaluate the effectiveness of epidural injection of local anesthetics and steroids in patients with nonspecific back pain associated with degenerative-dystrophic lesions of various parts of the spine and to determine its effect on improving the quality of life of these patients. Materials and methods. The results of treatment were analyzed in 71 patients aged 36 to 74 years, who underwent treatment for chronic nonspecific back pain at the Center for Pain Management and neurology department of Municipal Healthcare Institution “Regional Clinical Hospital — Center for Emergency Medical Care and Disaster Medicine” from 2016 to 2017. Patients were divided into 2 groups: the main group — 38 people, who received epidural steroids and local anesthetic solution as a monotherapy, and 33 patients with standard conservative treatment. Results. As a result of the therapy, patients reported reduced back pain, improved overall well-being and quality of life. However, pain level in main group was 1.7 times lower compared to the controls 6 weeks after treatment. The improvement in vital activity and overall functioning was twice as good compared with the results before the treatment in the main group, but patients of the control group did not achieve this result even 6 months after the treatment. Conclusions. Based on the study results we concluded that the epidural injections of steroid solution and local anesthetic in patients with chronic nonspecific back pain can be used when modeling pain syndrome. The positive dynamics according to questionnaires and scales confirmed active restoration of neurological status, ability to self-service and the quality of life of patients.
Вступ
Неспецифічний біль у спині (НБС) виникає в людей будь-якого віку і є провідним фактором втрати працездатності у всьому світі, тому медичну і соціальну значимість цієї патології тяжко переоцінити [1, 2]. Поширеність НБС у країнах Західної Європи і США сягає 45–80 %, причому хронічні болі відчувають 10–30 % населення, а за медичною допомогою звертаються тільки 5 % хворих [2–4]. Відомо, що загальні витрати на лікування НБС в три рази перевищують вартість лікування онкологічних хворих, а в рейтингу причин тимчасової непрацездатності він займає 2-ге місце [5].
Причин виникнення болю в спині безліч. Насамперед їх можна розподілити на вертеброгенні (грижа міжхребцевого диска, спондилоартроз, спондильоз, спондилолістез, стеноз хребетного каналу, остеопороз та ін.) та невертеброгенні (міофасціальний синдром, розтягнення зв’язок і м’язів, фіброміалгія та ін.) [6]. Зрозуміло, що тільки ефективна багатокомпонентна допомога пацієнтам із НБС може повною мірою сприяти одужанню, але, на нашу думку, першочергово пацієнти потребують адекватного знеболювання для покращання якості життя незалежно від етіологічних факторів, що викликали цей симптомокомплекс.
НБС у контексті сучасної патогенетичної класифікації болю можна віднести до змішаного типу [6–8]. Центральна частина міжхребцевого диска містить велику кількість фосфоліпази А2 (ФА2), що ферментує арахідонову кислоту, у результаті чого утворюються такі медіатори болю, як простагландини та лейкотрієни. При взаємодії з ноцицепторами фіброзного кільця міжхребцевого диска, задньої поздовжньої зв’язки, твердої мозкової оболонки вони забезпечують ноцицептивний компонент НБС [9]. Також існують дані, згідно з якими запальні медіатори наявні в підвищених концентраціях у грижі і в дегенеративно змінених міжхребцевих дисках [10]. Простагландини, що, зі свого боку, також є похідними арахідонової кислоти, відповідають за загострення болю шляхом сенсибілізації периферичних ноцицепторів. Крім цього, у результаті ущемлення корінця з сенсорних волокон, що оточують задній ріг спинного мозку, можуть вивільнятися нейрогенні медіатори болю, такі як субстанція Р, вазоактивний інтестинальний пептид і пептид, що регулюється кальцитоніновим геном, які викликають формування нейропатичного компонента болю [11, 12]. Змішаний характер больового синдрому, недостатня ефективність лікування болю в гострий період можуть вважатися основними факторами хронізації больового синдрому [8, 10]. Таким чином, важливо, ураховуючи патофізіологічні механізми розвитку НБС, максимально ефективно ліквідувати больовий синдром на ранніх стадіях хвороби, знижуючи ймовірність переходу синдрому в хронічну форму.
Згідно з уніфікованим клінічним протоколом МОЗ України № 311 від 25.04.2012 р. № 311 для контролю хронічного больового синдрому використовуються нестероїдні протизапальні та протиревматичні засоби. У США епідуральні ін’єкції є одним із найбільш поширених методів менеджменту хронічного болю в спині і нижніх кінцівках [2, 6, 12]. Арсенал препаратів для епідуральних блокад зростає з кожним роком, але найбільше привертають увагу публікації про ефективність епідурального введення розчинів глюкокортикостероїдів (ГКС) та місцевих анестетиків (МА) [13]. В основі аналгетичного ефекту ГКС лежить їх здатність пригнічувати фермент ФА2, що перериває місцеві запальні реакції, у результаті зменшуються набряк і защемлення нервових волокон [7, 13]. Разом із тим ГКС, введені в епідуральний простір, можуть пригнічувати біль за допомогою їх здатності припиняти ектопічні імпульси з пошкодженого нерва і знижувати провідність в інтактних немієлінізованих волокнах типу C [14]. Епідуральна ін’єкція МА може збільшити приплив крові до ішемізованого нерва і, подібно до ГКС, уповільнити або зупинити ноцицептивну передачу [10, 15]. Крім того, розчин місцевого анестетика може справляти аналгетичний ефект шляхом вимивання прозапальних цитокінів і сприяти адгезіолізису рубцевої тканини [7]. Незважаючи на усі переваги даного методу лікування, у літературі недостатньо даних, що б підтверджували ефективність епідурального введення ГКС та МА при неспецифічному болі в спині.
Мета роботи: визначити ефективність епідурального введення розчину ГКС та МА у пацієнтів із хронічним неспецифічним болем у спині і оцінити його вплив на покращання якості життя таких хворих.
Матеріали та методи
До проспективного когортного дослідження було включено 71 пацієнта віком від 36 до 74 років із хронічним НБС, які перебували в Центрі лікування болю та неврологічному відділенні КЗОЗ «Харківська обласна клінічна лікарня — Центр екстреної медичної допомоги та медицини катастроф» із 2016 по 2017 рік. Усіх хворих було розподілено на 2 групи: основну, до неї увійшло 38 осіб (22 жінки та 16 чоловіків, середній вік — 51,44 ± 8,77 року), які як лікування отримали лише курс епідуральних ін’єкцій, та контрольну — 33 пацієнти (21 жінка та 12 чоловіків, середній вік — 53,08 ± 7,46 року), які отримали стандартну для цієї патології терапію. При аналізі даних виявлено, що досліджувані групи пацієнтів вірогідно не відрізняються за віковими, антропометричними параметрами та фізичним станом.
Обстеження починалося з клінічного огляду, за результатами якого проводився відбір пацієнтів згідно з критеріями включення та виключення.
Критеріями включення були: вік понад 18 і менше 75 років; біль у спині з іррадіацією або без такої; інтенсивність болю за візуально-аналоговою шкалою (ВАШ) — 4 бали і більше; тривалість болю — 3 місяці та більше; підписання інформованої згоди на участь у дослідженні; фізичний статус — ІІ–ІІІ клас за АSА; доведений зв’язок больового синдрому з патологією міжхребцевого диска (магнітно-резонансна, комп’ютерна томографія); відсутність протипоказань до пункції епідурального простору; значне обмеження рухової активності і погіршення якості життя.
Критерії виключення: наявність тяжкої соматичної патології; перелом хребта в анамнезі; онкологічні хвороби; інфекційний процес у стадії загострення.
Інтенсивність больового синдрому та його вплив на життя оцінювали перед першою блокадою, безпосередньо після неї, через 3 тижні, 6 тижнів і через 6 місяців. Кратність курсу ін’єкцій і необхідність проведення повторних курсів блокад визначали з огляду на особливості клінічної симптоматики і дані інструментального обстеження кожного конкретного пацієнта. Термін спостереження становив від 2 до 6 місяців.
Оцінку больового синдрому проводили за допомогою ВАШ. При використанні ВАШ пацієнту пропонували висловити суб’єктивне відчуття болю. Шкала проградуйована від 0 до 10, де 0 — відсутність болю, 10 — максимально сильний біль, що коли-небудь відчував пацієнт.
Також із метою оцінки якості терапії використовували опитувальник Освестрі. Він дає можливість у балах оцінити вплив болю на самообслуговування, сон, суспільне життя, переміщення в просторі, спроможність піднімати важкі предмети, тривалий час стояти і сидіти. Опитувальник містить 10 розділів, в кожному з яких 6 пунктів. Хворий позначає в кожному розділі тільки один пункт, що найбільш відповідає його стану. Лікар залежно від порядкового номера квадратика (1–6) проставляє бали (0–5). Індекс відповідей дорівнює сумі балів десяти відповідей, помножених на 2. Максимальна кількість балів — 50, а максимальний відсоток дорівнює 100.
Методика епідуральної ін’єкції. На початку маніпуляції виконували катетеризацію периферичної вени, весь час здійснювали моніторинг артеріального тиску, частоти серцевих скорочень, сатурації. У положенні пацієнта на животі на рентгенпрозорому столі проводили триразову обробку операційного поля 70% розчином етанолу. Існує декілька різновидів епідуральної блокади, але ми віддаємо перевагу інтерламінарному методу, оскільки він дозволяє проводити сегментарну блокаду в проблемному сегменті. Рівень пункції епідурального простору залежав від ураженого сегмента хребта — від L5 до Th12 при залученні попереково-крижового відділу хребта та від С5 до Th1 при болю в шийному відділі. Пункцію епідурального простору виконували голкою для епідуральної анестезії із зрізом типу Туохі діаметром 18G в асептичних умовах із дотриманням принципів сегментарності після інфільтрації шкіри, підшкірної клітковини і міжостистої зв’язки 2% розчином лідокаїну, як зображено на рис. 1.
/82-1.jpg)
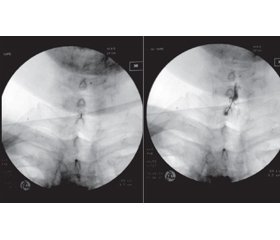
За допомогою цієї голки вводили контраст Visipaque 1 мл під контролем електронно-оптичного перетворювача. Рентген-контроль поширення контрасту дозволяв точно ідентифікувати епідуральний простір (рис. 2). Після візуалізації в епідуральний простір вводили розчин бупівакаїну 5 мг/мл в об’ємі 1 мл із додаванням 1 мл кеналогу 40. Із ГКС ми віддаємо перевагу препарату кеналог 40, до складу якого входить тріамцинолон ацетонід, що, блокуючи ФА2, забезпечує швидку і пролонговану протизапальну і болезаспокійливу дію та має найбільш виражений деструктивний вплив на грижі. Після ін’єкції пацієнтів укладали на 15 хв на хвору сторону, що дозволяло фіксуватися лікувальній суміші на ураженому корінці.
/82-2.jpg)
Статистична обробка отриманих даних проводилася в такий спосіб: спочатку перевірялась відповідність ряду даних вибірки нормальному закону розподілу за допомогою критерію Шапіро — Уїлка. Для порівнянь застосовувався параметричний t-критерій Стьюдента або непараметричний критерій Манна — Уїтні. Побудова порівняння якісних ознак проводилася за допомогою точного критерію χ2 із включенням критерію Макнемара. Розрахунки здійснювалися на персональному комп’ютері за допомогою пакета програм Microsoft Office та Statistica 7.0. Відмінності вважали вірогідними при р < 0,05.
Результати та обговорення
У результаті проведеної терапії пацієнти відчували зменшення болю в спині, покращання загального самопочуття та якості життя. Так, при аналізі показників інтенсивності болю за ВАШ було виявлено вірогідне зниження показників: через тиждень після лікування в пацієнтів основної групи інтенсивність болю знизалась на 57,6 % порівняно зі зниженням на 29,5 % серед хворих контрольної групи. Така тенденція зберігалась протягом усього періоду спостереження. Через 6 тижнів рівень болю в групі, що отримувала епідуральні ін’єкції, був нижчим в 1,7 раза порівняно зі стандартною терапією.
За допомогою опитувальника Освестрі визначали порушення життєдіяльності пацієнтів до та після лікування. У результаті дослідження було виявлено вірогідне зниження балів серед опитуваних усіх груп після курсу призначеного лікування. Однак у пацієнтів основної групи визначали покращання життєдіяльності в два рази порівняно з результатами до лікування вже з 3-го тижня, тобто після 2-ї блокади, тоді як пацієнти контрольної групи не досягли такого результату навіть через 6 місяців після лікування.
Висновки
Проведене дослідження показало доцільність використання епідуральних інфільтрацій розчину глюкокортикоїду та місцевого анестетику в пацієнтів із хронічним неспецифічним болем у спині в моделюванні больового синдрому та його ефективність порівняно зі стандартною терапією.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Maher C. Non-specific low back pain / C. Maher, M. Underwood, R. Buchbinder // The Lancet. — 2017. — Т. 389. — № 10070. — С. 736-747.
2. Chatterjee R. The effect of low vitamin D on chronic non-specific low back pain: A systematic review / R. Chatterjee S. Hemmings, M.W. Laupheimer // International Musculoske–letal Medicine. — 2016. — Т. 38. — № 2. — С. 43-50.
3. Van Helvoirt H. et al. Transforaminal epidural steroid injections influence Mechanical Diagnosis and Therapy (MDT) pain response classification in candidates for lumbar herniated disc surgery // Journal of back and musculoskeletal rehabilitation. — 2016. — Т. 29. — №. 2. — С. 351-359.
4. Свиридова Н.К. Боль в нижней части спины // Междунар. неврол. журн. — 2016. — № 5(83). — С. 130-134.
5. Поворознюк В.В. Боль в нижней части спины. Распространенность, причины, механизмы развития и особенности диагностики // Боль. Суставы. Позвоночник. — 2011. — № 1. — С. 1.
6. Van Dongen J.M. et al. Patient versus general population health state valuations: a case study of non-specific low back pain // Quality of Life Research. — 2017. — С. 1-7.
7. Баринов А.Н. Боль в спине: новые технологии и старые предрассудки / А.Н. Баринов, К.А Махинов, Д.А Сергиенко // Фарматека. — 2016. — № 7.
8. Goubert D. et al. Structural Changes of Lumbar Muscles in Non-specific Low Back Pain: A Systematic Review // Pain physician. — 2016. — Т. 19. — № 7. — С. 985.
9. Барыш А.Е. Современная методика инъекционного лечения вертеброгенной боли под контролем компьютерной томографии // Боль. Суставы. Позвоночник. — 2014. — № 1–2 (13–14). — С. 30-37.
10. Квасницкий Н.В. Эпидуральные инъекции стероидных препаратов в лечении корешкового синдрома, обусловленного дегенеративно-дистрофическим поражением позвоночника / Н.В. Квасницкий, А.Н. Квасницкий // Український нейрохірургічний журнал. — 2014. — № 4. — С. 55-60.
11. Данилов А.Б. Алгоритм диагностики и лечения боли в нижней части спины с точки зрения доказательной медицины // Нервные болезни. — 2010. — № 4. — С. 11-18.
12. Helm I.S. et al. Percutaneous adhesiolysis in the management of chronic low back pain in post lumbar surgery syndrome and spinal stenosis: a systematic review // Pain Physician. — 2012. — 15. — 435-462.
13. Manchikanti L., Pampati V., Falco J., Hirsch J. Growth of spinal interventional pain management techniques: analysis of utilization trends and Medicare expenditures 2000 to 2008 [published online ahead of print July 11, 2012] // Spine. — 2012.
14. Пятко В.Э. и др. Место эпидуральных блокад в лечении боли нижней части спины // Регионарная анестезия и лечение острой боли. — 2009. — № 1. — С. 25-27.
15. Kuijpers T. et al. A systematic review on the effectiveness of pharmacological interventions for chronic non specific low back pain // Eur. Spine J. — 2011. — 20. — Р. 40-50.

/82-1.jpg)
/82-2.jpg)
/83-1.jpg)