На сьогодні практично аксіомою є те, що прееклампсія — це патологія ендотелію. Причому до сьогодні залишається без відповіді питання: що відмічається в дебюті хвороби — артеріолодилатація чи артеріолоспазм? Ще в 1989 році J.N. Roberts et al. висунули гіпотезу про те, що провокуючими факторами виникнення/розвитку прееклампсії є вільні жирні кислоти, ліпопротеїди, пероксиди ліпідів, кахектин, продукти деградації фібриногену і фрагменти мікроворсинок синцитіотрофобласту, що потрапили в кровотік. Головною й єдиною проблемою в розвитку прееклампсії є плацента.
Тромботична мікрооангіопатія (ТМА) характеризується пошкодженням міросудинного русла різних органів, тромбоцитопенією і гемолітичною анемією. Вагітність вважається одним із найважливіших тригерів розвитку ТМА. Під час вагітності, з одного боку, виникає підвищення рівня фактора фон Віллебранда (vWF), ймовірно, під дією естрогенів, а з іншого — зниження активності ферменту ADAVNS 13, ймовірно, під дією підвищеного його споживання, основна роль якого полягає в руйнуванні мультимерів vWF. Фізіологічна роль vWF полягає в забезпеченні адгезії тромбоцитів до субендотеліального матриксу при пошкодженні судини і гемодинамічному стресі. При високому рівні vWF і/або низькій активності ферменту ADAVNS 13 виникають ТМА, порушення мікроциркуляції в різних органах, насамперед у нирках, печінці, кишках тощо (табл. 1).
У більшості шкал оцінки тяжкості стану хворого та тяжкості поліорганної дисфункції як маркерів печінкової дисфукнції оцінюють рівень білірубіну й активність трансаміназ. Відразу виникає питання: а як же бути з такими функціями (чи дисфункціями) печінки, як синтетична, детоксикаційна та ін.? Ураховуючи поліфункціональність печінки, дати чітке визначення гострої печінкової дисфункції (ГПечД) є вкрай складним завдання. Говорячи про ГПечД, слід оцінити всі функції печінки (табл. 2), виділивши найбільш виражені, і тоді скласти алгоритм дій.
Для оцінки тяжкості ГПечД є декілька шкал, але всі вони мають як переваги, так і недоліки (табл. 3).
Однією з найтяжчих проблем, що виникає під час ускладнення вагітності, є печінкова –дисфункція (табл. 4). Навіть під час вагітності, що перебігає –фізіологічно, у 3–8 % жінок виникають функціональні зміни печінки: знижується рівень альбуміну (у 1,5 раза), антитромбіну III, протеїнів С і S, гаптоглобіну, підвищується рівень лужної фосфатази (у 2–4 рази), фібриногену, α1-, α2-, β-глобулінів, церулоплазміну, трансферину (в 1,5 раза), жовчних кислот (у 3 рази), тригліцеридів (у 3 рази) та холестерину (у 1,5 раза).
Тяжкість діагностики ГПечД у вагітних зумовлена, по-перше, поліфункціональністю печінки, а по-друге — особливістю функціонального стану вагітної, наявністю особливої «норми» вагітної жінки (табл. 5).
Найбільш грізними причинами виникнення ГПечД під час вагітності є прееклампсія, HELLP-синдром, гостра жирова дистрофія печінки та холестатичний гепатоз вагітних.
HELLP-синдром
Термін HELLP-синдром запропонований L. Weinstein у 1982 році. HELLP-синдром: hemolysis — поява вільного гемоглобіну в плазмі крові та сечі; elevated Liver enzimes — підвищений рівень АСТ і АЛТ; low platelets — тромбоцитопенія.
Окрім того, виділяють парціальні форми: ELLP- та LP-синдром.
HELLP-синдром ускладнює вагітність у 0,5–0,9 % вагітних, а при тяжкій прееклампсії він зустрічається в 10–20 % випадків. Здебільшого він виникає під час вагітності (в 10 % — до 27-го тижня вагітності, в 50 % — в терміні вагітності 27–37 тижнів, а в 20 % — після 37-го тижня).
В 10–20 % випадків розвиток HELLP-синдрому на відміну від прееклампсії не супроводжується артеріальною гіпертензією. При вимірюванні АТ важливим є правильний підбір розмірів манжеток тонометрів. Так, при величині плеча стандартного розміру (менше 33 см) слід користуватися манжеткою стандартного розміру (12 × 23 см), при окружності плеча 33–41 см розмір манжетки має бути 15 × 33 см, а при окружності плеча більше 41 см — 18 × 36 см. При вимірюванні АТ манжетка манометра має знаходитися на рівні серця. В США АТ визначають у сидячому положенні, а в Англії — в лежачому положенні хворого на правому боці при боковому нахилі на 30°, при цьому манжетка манометра повинна знаходитися на рівні серця.
Надлишкова прибавка маси тіла та набряки в 50 % передують розвитку HELLP-синдрому.
Перинатальна летальність залишається дуже високою і сягає 34 %, а летальність жінок — 25 %.
Патогенез. Провідними механізмами розвитку HELLP-синдрому є порушення тонусу та проникності судин (вазоспазм/вазодилатація (?), підвищена проникність судин), активація нейтрофілів, дисбаланс про- та протизапальних цитокінів (підвищений рівень IL-10, -6, трансформуючого фактора росту β3 та зниження концентрації CCL18,CXCL5 та IL-6). Одночасно виникають відкладення фібрину і мікротромбування, збільшення активності інгібіторів активації плазміногену (РАІ-1).
Певне значення в розвитку HELLP-синдрому мають антифосфоліпідний синдром та інші варіанти тромбофілій, різні варіанти генетичних аномалій, які пов’язують із наявністю поліморфізму генів. Ці гени кодують компоненти системи ліпідного обміну (LPL, ApoE, LCYFD), антиоксидантного (EPHX, CYPIAI, SOD) та імунологічного захисту (HLA-G, TNF-α, IL-1, IL-10, CD14-рецептор, CTLA-4), системи гемостазу (FVL, MTHFR, протромбін, CBS, PAI-1, GP-111A, FX111, FXV11, фібриноген), плацентарних факторів (STOX1, SERPINA3, ACVR2, IGF-1, IGF-11), факторів, що регулюють тонус судин (AGT, ACE, ATIR, REN, PRCP, eNOS, ET-1, ER, F1t-1, ENG, VEGF, PIGF).
Діагностика. Згідно з критеріями Tennessee: рівень тромбоцитів менше 100 0009/л, АСТ > 70 ОД/л, ЛДГ > 600 ОД/л.
Згідно з критеріями Mississippi:
— I клас: тромбоцити < 50 0009/л, АСТ і АЛТ > 70 ОД/л, ЛДГ > 600 ОД/л;
— II клас: тромбоцити < 50 000—100 0009/л, АСТ і АЛТ > 70 ОД/л, ЛДГ > 600 ОД/л;
— III клас: тромбоцити < 100 000—150 0009/л, АСТ і АЛТ 40–70 ОД/л, ЛДГ > 600 ОД/л.
Клінічно вагітні відчувають біль у животі (внаслідок розтягнення капсули печінки та інтестинальної ішемії).
Відмічається високий рівень розчинних комплексів фібрин-мономіру як прояв ДВЗ-синдрому.
На фоні зниженого рівня гемоглобіну в 10 % вагітних та породіль виявляють гемоглобінемію та гемоглобінурію. Ранньою і специфічною ознакою внутрішньосудинного гемолізу є низький вміст гаптоглобіну (менше 1 г/л) та поява в мазку крові обломків еритроцитів — шизоцитів.
У біохімічному аналізі крові — підвищений рівень непрямого білірубіну та глутатіон-S-трансферази (GST-al або α-GSТ).
Одним із найважливіших предикторів і критеріїв тяжкості HELLP-синдрому є тромбоцитопенія, що корелює з геморагічними ускладненнями та тяжкістю ДВЗ-синдрому.
Важливо відрізнити внутрішньосудинний гемоліз від позасудинного. Останній виникає при фагоцитозі еритроцтів клітинами селезінки. При цьому в мазку крові видно сфероцити або мікросфероцити. Внутрішньосудинний гемоліз викликає руйнування еритроцитів внаслідок їх механічного пошкодження. Цей вид гемолізу є характерним для HELLP-синдрому. Для цього виду гемолізу характерні:
— зубчасті, зморщені, зруйновані еритроцити з різко окресленими краями;
— маленькі, неправильної форми фрагменти еритроцитів (зіркоподібні клітини) і шистоцити;
— поліхромазія;
— при втраті всього гемоглобіну в мазку крові видно «тіні» клітин.
У дослідженні PIERS (Preeclampsia Integrated Estimate of Risk) прогностичну значимість для негативного кінця хвороби для матері показують: біль у грудях, задишка, тромбоцитопенія, підвищений рівень АСТ і АЛТ, HELLP-синдром та гіперкреатинемія. Негативний перинатальний результат був пов’язаний з діастолічним АТ > 110 мм рт.ст. та відшаруванням плаценти (табл. 6).
Перинатальні ускладнення в дитини подано в табл. 7.
HELLP-синдром слід диференціювати з низкою патологічних станів.
Диференціальна діагностика
— Гестаційна тромбоцитопенія.
— Гостра жирова дистрофія печінки.
— Вірусний гепатит.
— Холангіт.
— Холецистит.
— Інфекція сечовивідних шляхів.
— Гастрит.
— Виразка шлунка.
— Гострий панкреатит.
— Імунна тромбоцитопенія.
— Дефіцит фолієвої кислоти.
— Системний червоний вовчак.
— Антифосфоліпідний синдром.
— Тромботична тромбоцитопенічна пурпура.
— Гемолітико-уремічний синдром.
Патоморфологія. У літературі сьогодні є чимало протиріч щодо характеру пошкодження печінки при HELLP-синдромі. Одні автори вважають класичним морфологічним варінтом пошкодження печінки при HELLP-синдромі перипортальний чи острівковий паренхіматозний некроз із депозитами фібрину в просвіті синусоїдних капілярів, а інші говорять про подібність морфологічних змін печінки при HELLP-синдромі і гострому жировому гепатозі вагітних та неможливість морфологічної диференціальної діагностики цих патологічних станів. На думку А.В. Кулікова і співавт. (2014), різниця морфологічних змін у печінці при HELLP-синдромі визначається його формою (повна чи часткова).
При повному HELLP-синдромі виявляють поширений гепатоцелюлярний некроз. Макроскопічно печінка збільшена в розмірах, світло-коричневого кольору, строката за рахунок множинних різнокаліберних субкапсульних і паренхіматозних джерел темно-коричневого кольору, що мають тенденцію до злиття.
При гістологічному дослідженні в печінковій паренхімі знаходять субкапсульні, центролобулярні, перипортальні та мультилобулярні джерела некрозу, крововиливів, масивні відкладення фібрину в синусоїдних капілярах, плазматичне просякнення стінок артеріол.
Характер морфологічних змін печінки при повному HELLP-синдромі подібний до змін печінки при еклампсії.
При повному HELLP-синдромі пошкоджуються також і нирки у вигляді гемоглобінурійного нефрозу внаслідок внутрішньосудинного гемолізу. У легенях виявляють мегакаріоцитоз (морфологічний маркер тромбоцитопенії).
При парціальному HELLP-синдромі (ELLP-синдромі) морфологічна картина печінки характеризується наявністю в цитоплазмі множинних гепатоцитів різної величини, жирових вакуолей.
Лікування. Патогенетичною тактикою лікування є розродження.
При терміні вагітності більше 34 тижнів потрібне термінове розродження. Вибір методу розродження визначається акушерською ситуацією.
При терміні вагітності 27–34 тижні та за відсутності загрозливої для життя ситуації (кровотеча, ДВЗ-синдром, прееклампсія/еклампсія) можливим є пролонгування вагітності до 48 год (стабілізація стану вагітної та підготовка легень плода кортико–стероїдами). Вибір методу розродження — операція кесаревого розтину.
При терміні вагітності менше 27 тижнів та за відсутності загрозливої для життя ситуації можливою є пролонгація вагітності до 48–72 год.
Однією з головних проблем, що виникає у вагітних із HELLP-синдромом, є дискоагулемія (табл. 8).
Кортикостероїди у жінок з HELLP-синдромом (бетамезон 12 мг/24 год, дексаметазон 6–10 мг через 12 год) не показали ефективності в запобіганні ускладненням зі сторони матері, за винятком зростання кількості тромбоцитів. Застосування кортикостероїдів зменшує частоту виникнення тяжкого респіраторного дистрес-синдрому у новонародженого. Кортикостероїди призначають при кількості тромбоцитів менше 50 тис. клітин.
Магнезіальна терапія. Магнію сульфат призначають при АТ > 160/110 мм рт.ст. болюсно 4 грами, а потім 1 г/год під контролем колінного рефлексу. Терапію треба продовжувати не менше як 48 год після розродження.
Корекція коагулопатії. У разі ускладнення HELLP-синдрому кровотечею чи ДВЗ-синдромом застосовують свіжозаморожену плазму (20–30 мл/кг маси тіла), кріопреципітат (при гіпофібриногенемії), рекомбінантний фактор VII, концентрат протромбінового комплексу. При розвитку коагулопатичної кровотечі потрібно застосовувати антифібринолітичну терапію (транексамова кислота — 10–15 мг/кг). Тромбоцитарну масу застосовують при кількості тромбоцитів менше 20 тис. клітин.
Інфузійна терапія. На сьогодні не існує єдиної думки як щодо кількості, так і щодо якісного складу інфузійної терапії при HELLP-синдромі. Усі сходяться на думці, що препаратами першого ряду мають бути збалансовані кристалоїдні препарати.
Лікування внутрішньосудинного гемолізу. Показано термінове проведення плазмаферезу. При збереженому темпі сечовиділення застосовують 4% гідрокарбонат натрію для корекції метаболічного ацидозу та запобігання утворенню солянокислого гематину в просвіті канальців нирок. Застосовуючи фуросемід (20–40 мг) та інфузійну терапію кристалоїдами, треба намагатися досягнути темпу сечовиділення до 100–150 мл/год.
При гострому пошкодженні нирок (І чи F за класифікацією RIFLE) обмежують темп інфузії до 300 мл та об’єм діурезу та застосовують технології нирково-замісної терапії.
Анестезіологічне забезпечення операції кесарева розтину. При коагулопатії (тромбоцити менше 100 тис. клітин; МНВ більше 1,5; фібриноген менше 1 г/л; АЧТЧ більше в 1,5 раза від норми) методом вибору анестезіологічного забезпечення операційного втручання є загальна анестезія (діазепам-кетаміново-фентанілова анестезія).
Гострий жировий гепатоз вагітних
У 1934 році Stander і Caddenа, в 1940 році H.L. Sheehan описали патологічний стан вагітних, який назвали «гостра жовта акушерська атрофія печінки», летальність при якій тоді становила 90–100 %.
ГЖГВ спостерігається з частотою 1 : 7000–1 : 13 000 вагітностей. Як правило, це ускладнення розвивається на 32–36-му тижні вагітності.
Летальність при ГЖГВ на сьогодні становить від 18 до 25 %, а перинатальна летальність сягає 23 %.
Етіологія та патогенез ГЖГВ до сьогодні не зовсім зрозумілі. До факторів ризику розвитку ГЖГВ відносять генетичний мітохондріальний дефект β-окислен–ня жирних кислот: дефіцит ферментів довгого ланцюга 3-гідроксіацил КоА-дегідрогенази (LCHAD) у плода — мутації G1528-CiE474Q. Також має значення обмін жирних кислот у плаценті. В гетерозиготної матері та гомозиготного плода це призводить до надлишкового надходження токсичних метаболітів жирних кислот від плода в кровотік матері та ураженню печінки. Звідси і виникає необхідність розродження як єдиного патогенетичного методу лікування.
Клініка. Клінічні прояви ГЖГВ є доволі різноманітними.
Клініко-лабораторні симптоми ГЖГВ:
— блювання;
— біль у животі;
— полідипсія і поліурія;
— енцефалопатія;
— підвищений рівень трансаміназ (у 3–10 раз вище від норми);
— гіпербілірубінемія;
— гіпоглікемія;
— підвищення сечової кислоти;
— ниркова дисфункція (креатинін > 170 мкмоь/л);
— гіперамоніємія (> 47 мкмоль/л);
— гіперлейкоцитоз (від 11 до 20–30 тис. кл/л);
— коагулопатія (протромбіновий час > 14 с; АЧТЧ > 34 с);
— асцит або гіперехогенна структура печінки при ультразвуковій діагностиці;
— мікровезикулярний стеатонекроз при біопсії печінки.
За наявності більше 5 перерахованих вище симптомів імовірність ГЖГВ дуже велика.
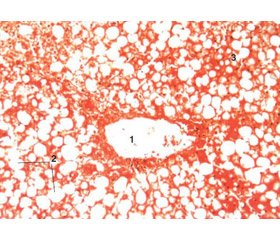
Патоморфологія. При макроскопічному дослідженні печінка яскраво-жовтого однорідного забарвлення. При мікроскопічному дослідженні гепатоцити набряклі, з різнокаліберними краплями жиру в цитоплазмі. Печінкова архітектоніка не порушена.
Морфологічною особливістю цієї патології є відсутність некрозу гепатоцитів і запалення строми (рис. 1).
Лікування. Інтенсивна терапія у вагітних із ГЖГВ має симптоматичний характер. Спосіб розродження визначається акушерською ситуацією.
Холестатичний гепатоз вагітних
У 80 % випадків ХГВ найчастіше розвивається після 30-го тижня вагітності. Однак є окремі повідомлення про розвиток ХГВ з 8-го тижня вагітності.
Частота виникнення ХГВ коливається від 1 : 1000 до 10 000 вагітних.
Етіологія та патогенез ХГВ на сьогодні є не зовсім зрозумілими. Причинами виникнення цього ускладнення вважаються ефект естрогенів і прогесторону, генетичні мутації транспортних білків у гепатобіліарній системі, які зв’язані з обміном жовчних кислот (АВСВ4 (MDR3), N591S, V444A, E279G, D482G, ABCC2, NR1114), низький рівень споживання селену, інфекції (гепатит, пієлонефрит), вживання антибіотиків, захворювання кишок.
Патоморфологія. При гістологічному дослідженні відмічають накопичення жовчного пігменту в гепатоцитах, розширення жовчних капілярів і міжчасточкових жовчних проток із переповненням їх жовчю та формуванням жовчних тромбів. У результаті тривалого застою жовчі можливі пошкодження гепатоцитів і розрив жовчних проток з утворенням «жовчних озер».
Клініка. Головними проявами є свербіж шкіри та помірні болі в животі. Перебіг ХГВ для матері регресує від 3–5 діб до 3–4 тижнів після пологів. Значно гірший вплив ХГВ має на плід. У зв’язку із збільшеним ризиком антенатальної загибелі плода частота передчасних пологів сягає 60 %.
Діагностика. Підвищений рівень лужної фосфатази, гаммаглутамілтранспептидази, помірне підвищення рівня білірубіну, АСТ, АЛТ, жовчних кислот.
Лікування. Основними препаратами є похідні урсодезоксихолієвої кислоти (8–15 мг/кг/24 год) протягом 1–4 тижнів.
Розродження вагітної проводять у термін вагітності 37–38 тижнів.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів при підготовці даної статті.

/12-1.jpg)
/13-1.jpg )
/15-1.jpg )
/15-2.jpg )
/16-1.jpg )