Актуальность
За практически вековой период использования антибиотиков человечество накопило достаточное количество научной информации об их рациональном применении. Конкретный антибактериальный препарат эффективен только в отношении определенных микроорганизмов, и назначаться он должен в определенных эффективных дозах в течение четко указанного периода.
Антибактериальные препараты относятся к наиболее широко назначаемым препаратам в отделениях интенсивной терапии. Не секрет, что в клинике современной интенсивной терапии остро стоит проблема антибиотикорезистентности. ВОЗ определила резистентность к антибиотикам как одну из трех наиболее серьезных угроз нового тысячелетия для здоровья человека [1, 2].
Устойчивость к карбапенемам у основной группы грамотрицательных бактерий — возбудителей внутрибольничных инфекций была и остается серьезной проблемой. Тяжелые нозокомиальные инфекции из-за мультилекарственной резистентности (МЛР) грамотрицательных бактерий обусловливают высокую заболеваемость и смертность [1, 3].
Особенно высок уровень внутренней резистентности ко многим классам антибиотиков у таких микроорганизмов, как Pseudomonas aeruginosa (PA) и Acinetobacter baumannii (AB) и видов Enterobacteriaceae, способных вызывать инфекционные осложнения, чрезвычайно трудно поддающиеся лечению, а новые антибиотики для борьбы против этих бактерий не будут доступны в течение многих лет [3, 4].
Возможным путем решения этой проблемы может стать либо синтез новых антибактериальных средств, либо оптимизация применения имеющихся препаратов [5].
Поскольку новых антибиотиков, которые бы находились в разработке и были способны обходить известный механизм МЛР у грамотрицательных бактерий, практически не существует, становится актуальным выбор эффективного антибиотика из имеющегося на данный момент арсенала [6, 7].
NDM-продуцирующие (фермент металло-бета-лактамаза из Нью-Дели) клинические изоляты МЛР-superbug (супербактерии) были зарегистрированы в более чем 20 странах на всех континентах [8]. Многие из этих МЛР-изолятов, продуцирующих NDM, восприимчивы только к полимиксинам. Уровень резистентности к полимиксинам в настоящее время относительно низок, однако резистентность в грамотрицательных патогенах может возникать in vitro, а также вследствие неоптимального использования [9].
И в этой ситуации полимиксины вновь могут стать альтернативой «без выбора» для лечения грам–отрицательных бактериальных инфекций с МЛР. Без новых антибиотиков полимиксины все чаще используются в качестве терапии последней линии [10, 11].
Полимиксины относятся к природным катионным полипептидным антибиотикам с молекулярной массой около 1000–1750 кДа, которые продуцируются спорообразующими почвенными бактериями Bacillus polymyxa Ross.
Полимиксины оказывают на микроорганизмы бактерицидное действие, обусловленное способностью препаратов нарушать целостность цитоплазматической мембраны микробной клетки, что влечет за собой ее лизис.
Полимиксин B впервые был представлен для клинического применения в 1947 году как продукт роста Bacillus polymyxa. Colistin (Колистин), также известный как полимиксин Е, был первым антибиотиком, обнаруженным в 1949 году в Японии, полученным из Bacillus polymyxa subsp., а затем в Европе в 1950 и в США в 1959 году [12].
Из 5 выделенных групп природных соединений только 2 используются в клинике — полимиксин В и полимиксин Е (Колистин).
В связи в вышесказанным на современном этапе в клинике интенсивной терапии для снижения антибиотикорезистентности и борьбы с МЛР-продуцирующими NDM-изолятами большой интерес представляет колистиметат натрия (Colisti–methate sodium) — метансульфонат колистина.
Физическая химия
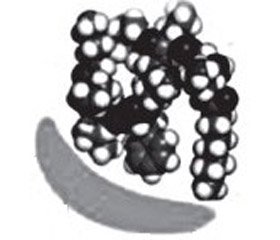
Чтобы понять механизмы антибактериальной активности полимиксинов и их резистентность, важно знать их химические структуры. Полимиксины имеют гидрофобную жирную кислотную группу и полярную группу из 5 немасштабированных амфипатических g-аминогрупп, благодаря которым возможна связь с мембранными мишенями бактерий. Единственная разница в структуре между полимиксином B и полимиксином E (Колистином) заключается в аминокислотных компонентах. Оба полимиксина представляют рацемическое соединение, которое содержит смесь D- и L-аминокислот, расположенных в виде циклического гептапептидного кольца с трипептидной боковой цепью, причем боковая цепь ковалентно связана с жирной кислотой через ацильную группу. Присутствие D-лейцина в молекуле Колистина отличает его от полимиксина B (рис. 1, 2) [6, 13].
/20-1.jpg )
Для парентеральных назначений Колистин представлен в виде натриевой соли метансульфоната колистина, который является неактивным пролекарством, подвергаясь гидролизу in vivo и in vitro, образует активную субстанцию. Каждый миллиграмм чистого колистинового основания в сульфате колистина и в колистиметате натрия эквивалентен 30 000 международных единиц и 12 500 единиц Колистина соответственно. Таким образом, термины colistin и colistimethate (рис. 3) не являются полными эквивалентами. Колистиметат натрия (CMS) менее эффективен и менее токсичен, чем сульфат колистина (табл. 1).
В настоящее время продолжается разработка различных составов полимиксинов для усиления их антимикробной активности при минимизации их токсических эффектов.
Механизм антибактериальной активности полимиксинов
Наружная мембрана бактерий представляет собой барьер для различных вредных веществ, включая многочисленные противомикробные средства [13]. Полимиксины оказывают антимикробное действие посредством прямого взаимодействия с липидным компонентом липидом А липополисахарида (LPS) внешнего слоя бактериальной клетки.
Модель данного воздействия, именуемая «самовозбуждаемое поглощение», указывает на то, что амфипатическая природа полимиксинов имеет решающее значение для обеспечения поглощения молекулы полимиксина через наружный мембранный барьер бактерий (рис. 4) [6, 13, 14].
Катионные молекулы Колистина конкурируют и вытесняют ионы Ca++ и Mg++, которые обычно стабилизируют молекулу липополисахарида наружной мембраны грамотрицательных бактерий. Являясь бактерицидными, они, нацеливаясь на клеточную стенку бактерий, нарушают проницаемость мембраны, что приводит к утечке внутриклеточных компонентов и в конечном итоге заканчивается гибелью клетки. Помимо этого, они также обладают антиэндотоксиновой активностью. Важным моментом является то, что бактерицидные и антиэндотоксиновые эффекты имеют выраженную дозозависимость [6].
В исследованиях также было показано, что полимиксины способны ингибировать альтернативную никотинамидадениндинуклеотиддегидрогеназу и малат: хиноноксидоредуктазу [14].
Отмечается также, что вышеописанные эффекты полимиксинов способствуют улучшению прохождения через бактериальную мембрану других гидрофильных антибиотиков, в частности карбопенемов, что усиливает суммарный антибактериальный эффект.
Полимиксины плохо абсорбируются из желудочно-кишечного тракта, зато хорошо накапливаются в печени, почках, мышцах, сердце и легких. Вследствие большой молекулярной массы тяжело проникают через гематоэнцефалический барьер (ГЭБ), однако в случае развития воспалительного процесса мозговых оболочек проницаемость ГЭБ резко возрастает [15].
Колистин и CMS в основном активны против грамотрицательных внутрибольничных изолятов с естественной восприимчивостью, таких как Enterobacteriaceae spp., неферментативные грамотрицательные бактерии P.aeruginosa и Acinetobacter spp. [13, 15], а также против Haemophilus influenzae, E.coli, Salmonella spp., Shigella spp., Klebsiella spp., Legionella pneumophila, Aeromonas spp., Citrobacter spp. и Bordetella pertussis. Виды Campylobacter неоднородны по восприимчивости к Колистину (табл. 2) [15].
Применение в интенсивной терапии
Сопротивляемость бактерий антибиотикам естественна и неизбежна. В 2013 году тогдашний директор центров по контролю и предотвращению заболеваний (CDC) Том Фриден сказал журналистам: «Если мы не будем вести себя осторожно, вскоре мы окажемся в постантибиотической эпохе». Все чаще врачи во всем мире сталкиваются с реальностью инфекций с грамотрицательными патогенами, которые устойчивы ко всем антибиотикам, кроме полимиксинов [4, 16]. В качестве яркого примера можно привести ситуацию с быстрым распространением NDM-1-продуцирующих Enterobacteriaceae (в основном K.pneumoniae и Escherichia coli) на Индийском полуострове с последующим распространением во многих странах. И в возникшей ситуации полимиксины становятся последней линией обороны против грамотрицательных супербактерий. Особенно остро эта проблема встает перед врачами отделений интенсивной терапии (ОИТ) при выборе стратегии назначения антибиотикотерапии пациентам с септическими состояниями, обусловленными внутригоспитальной суперинфекцией.
Частота инфекций, вызванных патогенными микроорганизмами, устойчивыми к β-лактаму, цефалоспоринам, аминогликозидам и хинолонам, резко возросла в последние годы. Распространенность таких резистентных штаммов в отделениях интенсивной терапии достигает 21,8 %. Например, смертность при инфекциях, вызванных A.baumannii, по сообщениям, составляет 52 % при бактериемии и от 23 до 73 % при пневмонии [16].
В интенсивной терапии для лечения серьезной системной грамотрицательной инфекции, включая организмы с МЛР, чтобы избежать ошибок при дозировке и введении, CMS следует назначать и вводить только с позиции активности колистинового основания (табл. 1).
Всасывание препарата через слизистую оболочку полости рта или желудочно-кишечного тракта не происходит. После парентерального введения Колистин связывается с белками крови примерно на 50 %. Около двух третей CMS в неизмененном состоянии элиминируется в основном почками в течение 24 часов.
Средняя эффективная дозировка у пациентов в ОИТ варьирует от 2,5 до 5,0 мг/кг/день при сохраненной нормальной функции почек и обычно назначается 2–4 раза в день.
В европейских странах для взрослых пациентов и детей старше 12 лет с нормальной функцией почек и массой тела более 60 кг режим дозирования рекомендован от 240 до 480 мг (3–6 миллионов МЕ) CMS в день в три приема. У пациентов с нормальной функцией почек и массой тела 60 кг или менее — 4–6 мг/кг (50 000–75 000 МЕ/кг) CMS в день, разделенные на три введения. Если в европейских руководствах по ведению пациентов с резистентной флорой верхняя граница рекомендованных доз при массе тела > 60 кг составляет 480 мг CMS, то в рекомендациях США максимальная доза составляет 800 мг CMS в день. При почечной дисфункции с уровнем креатинина 140–230 мкмоль/л рекомендуемая внутривенная доза Колистина для серьезных инфекций должна снижаться до 2 миллионов МЕ каждые 12 часов — 380 мг соответственно [16, 17].
У пациентов с почечной недостаточностью, которым требуется диализ, рекомендуемые внутривенные дозы CMS составляют от 2 до 3 мг/кг после каждого сеанса гемодиализа [16, 17] и 2 мг/кг в день во время проведения перитонеального диализа [17].
Также отмечено, что нефротоксичность и нейротоксичность препарата меньше, чем было опубликовано в прошлом. Это может быть связано с более высокой степенью очистки препаратов [17].
Daikos et al., изучая оптимальные режимы дозирования для достижения бактерицидного эффекта при МЛР грамотрицательной флоре, установили, что при концентрации в крови Колистина > 4 мкг/мл P.аeruginosa погибала практически в 100 % образцов, в то время как при концентрации < 4 мкг/мл в 40 % отобранного материала обнаруживался патогенный возбудитель. Для достижения этих концентраций требовалось назначение 9 млн МЕ каждые 24 часа [18].
Колистин, согласно данным ряда исследований о лечении пневмоний, вызванных грамотрицательными бактериями с МЛР (P.aeruginosa и Baumannii), также зарекомендовал себя как эффективный препарат выбора. Авторы описывают высокую выживаемость — 75,6 % при среднем режиме суточного дозирования 3,2 млн МЕ (256 мг) в виде ингаляций как дополнение к парентеральной терапии антибиотиками широкого спектра действия, такими как карбапенемы, пиперациллин/тазобактам и ампициллин/сульбактам. Следует также отметить, что терапия карбопенемами более 20 дней и CMS более 13 дней являлась независимым предиктором развития антибиотикорезистентности [19].
G.S. Bauldoff и соавт. [20] оценивали эффективность ингаляционного применения Колистина у больных муковисцидозом — кандидатов на трансплантацию легких. Все пациенты были колонизированы множественно-резистентными штаммами P.aeruginosa. Применение Колистина у 20 пациентов привело к исчезновению множественно-устойчивых штаммов и колонизации легких штаммами синегнойной палочки, чувствительными к антибиотикам в течение 45,0 ± 20,2 дня. В контрольной группе только у 3 из 10 пациентов были выделены такие микроорганизмы лишь через 144 ± 48 дней. Авторы заключают, что Колистин может быть использован для содействия появлению чувствительных к препаратам штаммов P.aeruginosa у пациентов, которым планируется трансплантация легких.
В исследовании Markou at al. был достигнут положительный клинический эффект от парентерального CMS в 73 % случаев сепсиса, вызванного МЛР-флорой. Итоговая выживаемость составила 57,7 %. Авторы отмечают, что поражение почек различной степени тяжести наблюдалось у 14,3 % больных. Эти обстоятельства требуют строгого контроля функции почек у всех пациентов, получающих полимиксины.
Berlana и соавторы [21] вводили Колистин (внутривенно, внутримышечно, ингаляционно или интратекально) 80 пациентам с бактериемией, инфицированным МЛР A.baumannii (86 %) или P.aeruginosa (14 %). У 41 пациента (51 %) воспалительный процесс был вызван штаммами A.baumannii, чувствительными исключительно к Колистину. Стерилизация крови была достигнута у 92 % пациентов. Коэффициент госпитальной смертности составил 18 % (14 пациентов). Наиболее распространенным осложнением было раздражение менингеальных оболочек (12 случаев). Прекращение лечения было необходимо в четырех эпизодах и уменьшение дозы — в четырех эпизодах, о необратимых токсических осложнениях не сообщалось [21].
Эффективность применения ингаляционного CMS в сочетании с традиционным внутривенным путем введения у пациентов с критическими заболеваниями, осложненными грамотрицательными мультирезистентными патогенами, бесспорно доказана, однако при присоединении поражения МЛР-флорой менингеальных оболочек возникает необходимость интратекального и интражелудочкового введения антибактериальных препаратов. В литературе указывают на успешное использование в этом случае от 3,75 до 10 мг CMS в день [22] в течение 20 дней без каких-либо побочных эффектов. Однако дискуссия по этому вопросу до сих пор продолжается.
Выводы
В течение последних лет из-за значительной активности МЛР грамотрицательной флоры (P.aeruginosa, A.baumannii и K.pneumoniae), ответственной за эпидемию внутригоспитальной инфекции, Колистин и CMS привлекли большой интерес. В охваченных инфекцией отделениях интенсивной терапии Колистин, вероятно, еще долго останется средством последнего шанса против грамотрицательных полирезистентных бактерий.
Устойчивость к полимиксинам в будущем неизбежно станет серьезной проблемой в мире, поскольку устойчивость к полимиксинам означает, что антибиотики практически не будут доступны для лечения опасных для жизни инфекций, вызванных устойчивыми МЛР-суперинфекциями.
И в заключение следует отметить, что полимиксины — это средства для лечения полирезистентных грамотрицательных «суперинфектов», а НЕ антибиотики для профилактического или необос–нованного эмпирического использования. В этих условиях разумный, рациональный выбор антибактериальных препаратов, способов, режимов дозирования поможет врачам длительно сохранять минимальный паритет в противостоянии «инфекция — макроорганизм».
Конфликт интересов. Не заявлен.
Список литературы
1. Boucher H.W., Talbot G.H., Benjamin D.K. et al. Infectious Diseases Society of, A10 x '20 progress-development of new drugs active against gram-negative bacilli: An update from the IDSA // Cli–nical Infectious Diseases. — 2013. — 56. — Р. 1685-1694.
2. Kumarasamy K.K., Toleman M.A., Walsh T.R. et al. Emergence of a new antibiotic resistance mechanism in India, Pakistan, and the UK: a molecular, biological, and epidemiological study // Lancet Infect. Dis. — 2010. — 10(9). — 597-602. [PubMed: 20705517
3. Queenan A.M., Bush K. Carbapenemases: the Versatile β-Lactamases // Clinical Microbiology Reviews. — 2007. — 20(3). — 440-458. doi: 10.1128/CMR.00001-07.
4. W.H. Organization Tacconelli E.C.E., Savoldi A., Kattula D., Burkert F. (Eds.), Global priority list of antibiotic-resistant bacteria to guide research, discovery, and development of new antibiotics (2017).
5. Shorr A.F. Review of studies of the impact on gram-negative bacterial resistance on outcomes in the intensive care unit // Crit. Care Med. — 2009. — 37. — 1463-9. [PubMed]
6. Velkov T., Roberts K.D., Nation R.L., Thompson P.E., Li J. Pharmacology of polymyxins: New insights into an 'old' class of antibiotics // Future Microbiology. — 2013. — 8. — Р. 711-724.
7. Cheah S.-E., Wang J., Nguyen V.T.T., Turnidge J.D., Li J., Nation R.L. New pharmacokinetic/pharmacodynamic studies of systemically administered colistin against Pseudomonas aeruginosa and Acinetobacter baumannii in mouse thigh and lung infection models: Smaller response in lung infection // Journal of Antimicrobial Chemotherapy. — 2015. — 70. — Р. 3291-3297.
8. Cornaglia G., Giamarellou H., Rossolini G.M. Metallo-beta-lactamases: a last frontier for betalactams? // Lancet Infect. Dis. — 2011. — 11(5). — 381-393. [PubMed: 21530894]
9. Gales A.C., Jones R.N., Sader H.S. Contemporary acti–vity of colistin and polymyxin B against a worldwide collection of Gram-negative pathogens: results from the SENTRY Antimicrobial Surveillance Program (2006–09) // J. Antimicrob. Chemo–ther. — 2011. — 66(9). — 2070-2074. [PubMed: 21715434]
10. Bialvaei A.Z., Samadi Kafil H. Colistin, mechanisms and prevalence of resistance // Curr. Med. Res. Opin. — 2015. — 31(4). — 707-21. Epub 2015 Mar 19.
11. Tran T.B., Velkov T., Nation R. at al. Pharmacokine–tics/pharmacodynamics of colistin and polymyxin B: are we there yet? // Int. J. Antimicrob. Agents. — 2016. — 48(6). — 592-597. Epub 2016 Oct 18.
12. Kumazawa J., Yagisawa M. The history of antibiotics: the Japanese story // J. Infect. Chemother. — 2002. — 8(2). — 125-33.
13. Velkov T., Thompson P.E., Nation R.L., Li J. Structure-activity relationships of polymyxin antibiotics // J. Med. Chem. — 2010. — 53(5). — 1898-1916. [PubMed: 19874036]
14. Sampson T.R., Liu X., Schroeder M.R., Kraft C.S., Burd E.M., Weiss D.S. Rapid killing of Acinetobacter baumannii by polymyxins is mediated by a hydroxyl radical death pathway // Antimicrob. Agents Chemother. — 2012. — 56(11). — 5642-5649. [PubMed: 22908157]
15. Tsimogianni A., Alexandropoulos P., Chantziara V. at al. Intrathecal or intraventricular administration of colistin, vancomycin and amikacin for central nervous system infections in neurosurgical patients in an intensive care unit // International Journal of Antimicrobial Agents. — 2017. — 49, 3. — Р. 389-390.
16. Michalopoulos A.S., Falagas M.E. Colistin: recent data on pharmacodynamics properties and clinical efficacy in critically ill patients // Ann. Intensive Care. — 2011. — 1. — 30.
17. Gurjar Mohan. Colistin for Lung Infection: An Update // Journal of Intensive Care. — 2015. — 3.1. — 3. PMC. Web. 9 Apr. 2018.
18. Daikos G.L., Skiada A., Pavleas J., Vafiadi C., Salatas K., Tofas P. et al. Serum bactericidal activity of three different dosing regimens of colistin with implications for optimum clinical use // J. Chemother. — 2010. — 22. — 175-8.
19. Lin C.C., Liu T.C., Kuo C.F., Liu C.P., Lee C.M. Aerosolized colistin for the treatment of multidrug-resistant Acinetobacter baumannii pneumonia: experience in a tertiary care hospital in northern Taiwan // J. Microbiol. Immunol. Infect. — 2010. — 43(4). — 323-31.
20. Bauldoff G.S., Nunley D.R., Manzetti J. et al. Use of aerosolized colistin sodium in cystic fibrosis patients awaiting lung transplantating // Transplantation. — 1997. — 64. — 748-52.
21. Simsek F., Gedik H., Yildirmak M.T., Iris N.E., Türkmen A., Ersoy A. et al. Colistin against colistin-only-susceptible Acinetobacter baumannii-related infections: monotherapy or combination therapy? // Indian J. Med. Microbiol. — 2012. — 30(4). — 448-52.
22. Petrosillo N., Giannella M., Antonelli M., Antonini M., Barsic B., Belancic L. et al. Clinical experience of colistin-glycopeptide combination in critically ill patients infected with Gram-negative bacteria // Antimicrob. Agents Chemother. — 2014. — 58(2). — 851-859.

/20-1.jpg )
/21-1.jpg )
/22-1.jpg )