Вступ
Консервативне лікування опущення і випадіння внутрішніх статевих органів застосовується на початкових стадіях захворювання та сприяє тільки поступовому розвитку процесу, але не призводить до регресії даної патології.
Радикально вилікувати пролапс внутрішніх статевих органів можливо лише хірургічними методами. На сьогодні запропоновано багато методів оперативного лікування.
Хірургічні операції для лікування генітального пролапсу можно умовно розподілити на декілька груп:
1. Втручання, спрямовані на зміцнення тазового дна — кольпоперинеолеваторопластика.
2. Операції із застосуванням різних модифікацій скорочення та закріплення круглих зв’язок матки та фіксацією матки за допомогою названих утворень.
3. Операції, направлені на укріплення фіксуючого апарату матки (кардинальних, крижово-маткових зв’язок) за рахунок зшивання їх між собою, транспозиції тощо.
4. Операції з жорсткою фіксацією органів, що випали, до стінок таза (до лобкових або крижової кістки, сакроспінальної зв’язки тощо).
5. Операції з використанням алопластичних матеріалів для закріплення зв’язкового апарату матки та її фіксації.
6. Операції, направлені на часткову облітерацію піхви (серединна кольпорафія Лефора — Нейгебауера, піхвово-промежинний клейзис — операція Лабгардта).
7. Радикальний метод хірургічного лікування опущення і випадіння внутрішніх статевих органів — піхвова екстирпація матки.
Сьогодні показаннями для піхвової гістеректомії є: літній вік хворої, патологічне ожиріння, повне випадіння матки, соматичний стан хворої, який дозволяє провести цю операцію. Вивчення найближчих та віддалених результатів і стану життєво важливих органів після операції піхвової екстирпації матки з приводу повного випадіння матки і стінок піхви показує, що дане втручання в пацієнток літнього віку є операцією вибору.
Перевагою піхвового доступу при лікуванні опущення і випадіння внутрішніх статевих органів є можливість одночасного хірургічної корекції з метою лікування нетримання сечі при напруженні, яке зустрічається при цій патології в 40 % спостережень. З метою запобігання інтраопераційних та післяопераційних ускладнень дуже важливо запропонувати хворій найбільш ефективний та безпечний метод знеболювання, що дасть можливість мінімізувати використання анальгетиків під час операції та в ранньому післяопераційному періоді.
Анестезіологічне забезпечення такого типу гінекологічних оперативних втручань у більшості випадків засноване на загальному знеболюванні з використанням ендотрахеальної анестезії з інгаляційними та внутрішньовенними анестетиками. Негативними сторонами загальної анестезії є обов’язкове переведення хворого на кероване дихання, недостатня аналгезія, токсичний вплив загальних анестетиків і більш тяжкий перебіг післяопераційного періоду, недостатня післяопераційна аналгезія, що потребує використання наркотичних анальгетиків.
Застосування при таких оперативних втручаннях методики субарахноїдальної анестезії в чистому вигляді забезпечує ідеальне знеболювання під час операції, але в ранньому післяопераційному періоді після закінчення дії субарахноїдальної анестезії відбувається «прорив» болю, що потребує використання тих же опіатів.
Використання комбінованої спінально-епідуральної анестезії також забезпечує достатню анестезію під час операції за рахунок субарахноїдальної анестезії і післяопераційну аналгезію за рахунок пролонгованої епідуральної аналгезії. Але фінансова складова такого методу знеболювання не завжди дозволяє його застосовувати.
Для розуміння механізмів виникнення больової імпульсації при таких оперативних втручаннях розглянемо іннервацію статевих органів жінки.
В іннервації статевих органів жінки беруть участь симпатична і парасимпатична нервова системи, а також спинномозкові нерви. Симпатичні та парасимпатичні волокна, що відходять від матково-піхвового сплетіння, іннервують піхву, матку, внутрішні відділи маткових труб, сечовий міхур. Тіло матки іннервується головним чином симпатичними волокнами, а шийка матки і піхва — переважно парасимпатичними.
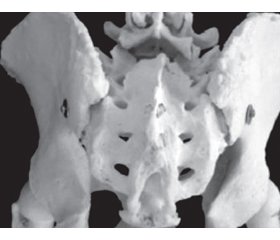
Крижове сплетіння, plexussacralis (рис. 1) — найзначніше з усіх сплетінь, складається з передніх гілок L4 (нижньої частини) і L5 поперекового нерва і гілок чотирьох крижових нервів (S1–4), що виходять із передніх отворів крижової кістки.
/116-1.jpg)
Короткі гілки: 1. Rami musculares для m. piriformis (з S1–2), m. оbturatorius interims із mm. gemelli і quadratus femoris (з L4–5, S1–2), для mm. levator ani et coccygeus. 2. N. gluteus superior (з L4–5, S1) виходить через foramen suprapiriforme з тазу разом з однойменною артерією і потім поширюється в m. gluteus medius, m. gluteus minimus і m. tensor fasciae latae. 3. N. gluteus inferior (з L5, S1–2), вийшовши через foramen infrapiriforme, постачає своїми гілками m. gluteus maximus і капсулу тазо–стегнового суглоба. 4. N. pudendus (з S1–4), вийшовши через foramen infrapiriforme, йде назад у таз через foramen ischiadicum minus. Далі n. pudendus разом з однойменною артерією проходить по боковій стінці fossa ischiorectalis. У межах останньої від нього відходять nn. rectales inferiores, які постачають зовнішній сфінктер (m. sphincter ani externus) і шкіру в найближчій окружності заднього проходу. На рівні сідничного бугра в заднього краю diaphragma urogenital n. pudendus ділиться на nn. perinei і n. dorsalis penis (clitoridis). Перші, йдучи вперед, інервують m. ischiocavernosus, m. bulbospongiosus і m. transversus perinei superficialis, а також шкіру промежини. Кінцеві гілки постачають шкіру задньої сторони мошонки (nn. scrotales posteriores) або великих статевих губ (nn. labiales posteriores). N. dorsalis penis (clitoridis) супроводжує в товщі diaphragma urogenital a. dorsalis penis, дає гілочки до m. transversus perinei profundus і m. sphincter urethrae, проходить на спинку статевого члена (або клітора), де поширюється в шкірі головним чином glans penis. У складі n. pudendus проходить велика кількість вегетативних волокон.
Мета дослідження: оцінити ефективність інтраопераційного і післяопераційного знеболювання комбінації методів регіональної анестезії (субарахноїдальна анестезія + каудальна аналгезія) із застосуванням ультразвукового супроводу при операції черезпіхвової екстирпації матки з пластикою.
Матеріали та методи
Знеболювання проведено в 32 пацієнток, які перебували на лікуванні у відділенні оперативної гінекології з малоінвазивними технологіями Харківського регіонального перинатального центру КЗОЗ «Обласна клінічна лікарня — Центр екстреної медичної допомоги та медицини катастроф».
Пацієнток прооперовано з приводу неповного випадіння внутрішніх статевих органів. Хворим проведено операцію черезпіхвової екстирпації матки з пластикою.
Ступінь операційно-анестезіологічного ризику був 2–3 за АSA. Досліджували коливання середнього артеріального тиску та сатурацію крові під час операції та інтенсивність болю в першу добу після операції (кожні 8 годин) за візуально-аналоговою шкалою (ВАШ). Післяопераційна аналгезія при нашому способі знеболювання тривала близько 1 доби. При зростанні інтенсивності болю, що виникав приблизно через 12 годин після операції, вводили декскетопрофену трометамол через 12 годин в дозі 50 мг внутрішньом’язово.
Результати та обговорення
Очевидно, що післяопераційна больова імпульсація при таких оперативних втручаннях зосереджена в малому тазі, тому в основу нашої моделі знеболювання лягла комбінація методів регіональної анестезії (субарахноїдальна анестезія + каудальна аналгезія).
Каудальна анестезія має низку переваг у використанні: надійний і досить тривалий аналгетичний ефект, відсутність значного фармакологічного навантаження на хвору, мінімальний вплив на гемодинаміку, дихання хворої, однократна ін’єкція.
Для того щоб ефективно провести каудальну блокаду, використовуючи анатомічні орієнтири, потрібно здійснити відбір хворих.
Каудальний епідуральний блок був уперше впроваджений як анатомічно орієнтована сліпа техніка (blind technique). Однак у дорослих він був успішним лише в 68–75 % випадків, навіть у досвідчених руках [1–3].
Анатомічні особливості, а деколи й аномалії будови крижової кістки зумовлюють труднощі в пункції каудального простору, що потребує великого досвіду і тривалого тренінгу щодо інших методів регіональної анестезії.
Частота анатомічних відхилень від 5 до 10 % зробила каудально-епідуральну анестезію непопулярною аж до відродження інтересу в 1940-х роках Хінгсоном та його колегами, які використовували його в акушерській анестезії. Крижово-куприкова мембрана не змогла бути ідентифікована в 10,8 % пацієнтів із використанням МРТ. Анатомічна оцінка 92 крижових кісток виявила, що в 42 % випадків був неправильно сформований вхід (hiatus sacralis) і ріжки (cornua); 4 % випадків показали відсутність входу (hiatus sacralis). Вершина сакрального входу в цьому дослідженні була на рівні S4 в 64 % випадків. У досліджуваній групі при дослідженні анатомії каудального епідурального простору сакральні ріжки не пальпувалися з двох сторін в 14,3 % випадків і пальпувалися з однієї сторони в 24,5 % випадків. Рівень максимальної кривизни крижів був на рівні S3 у 69,4 % випадків.
Ультразвук відіграє все більшу роль в галузі регіональної анестезії та управлінні болем. Ультразвуковий супровід каудального блоку може використовуватися для виявлення сакрального входу, що полегшує входження голки і візуалізацію її проходження на всьому протязі від шкіри до каудального каналу. Це є корисним для підвищення успішності блоку та зниження ризику ускладнень, таких як травма тканини, прокол твердої мозкової оболонки, токсичності місцевих анестетиків та внутрішньосудинного введення.
Каудальний блок з ультразвуковим супроводом вперше був описаний Klock та його колегами у 2003 році [4] і з того часу отримує все більшу популярність. Кілька досліджень різних етнічних груп неодноразово повідомляли про дуже високі успішні показники (96,9–100 %) ультразвукової каудальної ін’єкції [5–9].
Основні досліджувані параметри наведені в табл. 1.
Запропонований спосіб виконується так:
1) каудальний блок проводиться в положенні хворої на животі з підкладанням валика під таз. Після премедикації й обробки операційного поля за допомогою лінійного датчика (8–10 МГц) (в ультразвуковому сканері ми рекомендуємо використовувати перед налаштуванням — скелетно-м’язова система) визначається вхід у сакральній канал у корональному (поперечному) зрізі — це так званий сонографічний орієнтир — frog, тобто силует сидячої жаби (рис. 4);
2) наступний крок: розвертаємо датчик на цьому ж рівні на 90 градусів, тобто в сагітальну площину (аксіальний зріз) і досягаємо оптимальної візуалізації крижово-куприкової зв’язки, епідурального простору та задньої поверхні куприкової кістки (рис. 5). Після інфільтрації місцевим анестетиком розчином 1% лідокаїну епідуральною голкою G18–20 під візуальним контролем та втратою супротиву пунктуємо епідуральний простір. Вводимо 30 мл 0,375% розчину бупівакаїну;
3) субарахноїдальна анестезія проводиться в положенні хворої на боці парамедіанним доступом на рівні L2–4 голкою G26 і введенням 6–10 мг 0,5% гіпербаричного розчину бупівакаїну. При повертанні хворої на спину під коліна підкладається валик (для вирівнювання поперекового лордозу) і нахил столу контролюється електронним кутоміром у межах +2,5–5° для досягнення рівня блокади T9–10;
4) музичний супровід за рахунок навушників із релаксуючою музикою.
Висновки
Переваги запропонованого методу такі.
Каудальна блокада з візуалізацією епідурального простору і визначенням його ширини за допомогою ультразвукового сканера дозволяє застосувати її практично у всіх хворих, яким вона показана. Виняток становлять хворі з анатомічними вадами формування крижової кістки. Підготовка фахівця не займає багато часу і була освоєна всіма без винятку анестезіологами відділення.
Якість знеболювання визначалася самопочуттям самих пацієнтів, які відмічали адекватність знеболювання і комфортність на операційному столі і в післяопераційному періоді. Знеболювання після операції здійснювалось введенням нестероїдних протизапальних засобів 1–2 рази на добу без застосування опіоїдів.
Спонтанне дихання повітрям, що збагачено киснем з потоком 3–4 л/хв, дані пульсоксиметрії (SpO2) були в межах фізіологічної норми.
Гемодинаміка здебільшого була стабільною і не потребувала застосування вазоконстрикторів.
Пиття рідин призначалося через 2 години після операції, а ентеральне харчування — через 4 години.
Активізація пацієнтів: ходіння по палаті через 5 годин.
Даний матеріал показує переваги запропонованого методу над проведенням загального знеболювання та ізольованої субарахноїдальної анестезії в даної категорії хворих.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.

/116-1.jpg)
/117-1.jpg)
/118-1.jpg)
/119-1.jpg)
/120-1.jpg)