Введение
Синдром обструктивного апноэ сна (СОАС) характеризуется периодической, частичной или полной обструкцией верхних дыхательных путей (ВДП) на уровне ротоглотки во время сна. Эпизоды обструкции приводят к ночной гиповентиляции и десатурации, нарастанию гиперкапнии, фрагментации сна, что, в свою очередь, вызывает регулярные пробуждения, дневную сонливость, нарушения функции сердечно-сосудистой системы. В пери–операционном периоде как дети, так и взрослые пациенты с СОАС представляют собой отдельную категорию рисков периоперационных осложнений и летальности [1].
Ряд авторов расценивают наличие СОАС как независимый предиктор трудной вентиляции маской и трудной интубации трахеи [2]. А.П. Зильбер рассматривает СОАС как типичную полиорганную недостаточность [3]. Таким образом, наличие множества невидимых на первый взгляд при первичном контакте анестезиолога с пациентом подводных камней может значимо ухудшить течение периоперационного периода.
Цель: проанализировать и внедрить в практику клиники Practice Guidelines for the Perioperative Management of Patients with Obstructive Sleep Apnea.
Материалы и методы
Был проведен анализ имеющихся литературных источников, 10-летнего опыта проведения полисомнографий у пациентов разных возрастных категорий. Степень тяжести СОАС оценивалась при помощи индекса АГИ (апноэ/гипопноэ) = количество эпизодов апноэ и гипопноэ в час, как представлено в табл. 1.
Был выполнен анализ анестезиологических пособий у пациентов с диагностированным и недиаг–ностированным СОАС, особенно процесса экстубации трахеи у пациентов с ожирением и СОАС. У ряда пациентов были проведены записи полисомнографического исследования в течение 3 часов в раннем послеоперационном периоде. Сформирован протокол периоперационного ведения пациентов с СОАС.
Результаты и обсуждение
Согласно данным литературы, особое внимание в периоперационном периоде анестезиолог должен уделять пациентам с ожирением, беременностью и нарушениями костно-хрящевых или мягких тканей, вызывающими обструкцию верхних дыхательных путей, как пациентам с высоким риском развития СОАС.
Догоспитальный этап — анализ медицинской документации. Наличие у пациентов высокого индекса массы тела, гипертонической болезни, сахарного диабета, инфаркта миокарда в анамнезе может свидетельствовать о риске наличия СОАС.
Беседа с пациентом, как правило, неинформативна, потому что пациент не знает или не обращает внимания на наличие у него признаков СОАС, однако заполнение опросника STOP-Bang является эффективным средством выявления рисков наличия СОАС [4].
Является очевидным, что необходим совместный протокол хирургов и анестезиологов, по которому пациенты с риском СОАС должны обследоваться заранее, чтобы обеспечить безопасное ведение пациента в периоперационном периоде. Тактика ведения основывается на основании или клинических данных, или проведенного исследования сна (полисомнография). При выявлении СОАС необходимо принять решение: или начало лечения СОАС (СРАР-терапия — режим искусственной вентиляции легких постоянным положительным давлением) до операции или отложить оперативное вмешательство. При выборе послеоперационной аналгоседации следует учитывать риск и степень тяжести СОАС и, соответственно, риски гиповентиляции, представленные в табл. 2.
Пациент, родственники, а также хирург должны быть проинформированы о рисках СОАС в после–операционном периоде.
На госпитальном этапе предоперационная подготовка пациента с СОАС включает в себя:
— предоперационную CPAP-терапию. Если неэффективна — неинвазивная вентиляция с положительным давлением (NIV) в режиме Be-level;
— применение каппы;
— предоперационное снижение массы тела.
Следует учитывать потенциальный риск трудной интубации трахеи и быть готовым к обеспечению проходимости дыхательных путей по протоколу DAS [5].
Интраоперационный период — следует учитывать выбор метода анестезии, обеспечение проходимости и безопасности дыхательных путей, мониторинг пациента.
Склонность к обструкции ротоглотки потенцируется во время анестезии, поэтому препараты для анестезии у пациентов с СОАС должны обладать минимальной респираторной депрессией.
Для поверхностных процедур более предпочтительная местная, проводниковая или нейроаксиальная анестезия с умеренной седацией или без нее. При седации обязателен мониторинг пульсоксиметрии/капнометрии. СРАР-пользователь должен пользоваться своим СРАР-прибором в операционной. Общая анестезия с протектированными дыхательными путями более предпочтительна, чем глубокая седация без защиты. Экстубация только после полного пробуждения и полного восстановления нейромышечного проведения на боку, в приподнятом положении [1].
Послеоперационный период — необходимо акцентировать внимание на послеоперационной аналгезии, оксигенации, положении пациента и мониторинге.
Послеоперационная аналгезия — применение опиоидов, седативных препаратов (бензодиазепины, транквилизаторы, барбитураты) потенцирует тяжесть СОАС. Поэтому следует использовать региональные методы обезболивания или нестероидные противовоспалительные препараты (НПВП) для уменьшения или устранения потребности в опиатах. При невозможности отказаться от опиоидов и седативных препаратов — контроль пульсоксиметрии/капнометрии и по показаниям СРАР-терапия.
Оксигенация — при гипопноэ/гиповентиляции дополнительная оксигенация показана до стабилизации показателей пульсоксиметрии на воздухе. При апноэ/гиповентиляции применение СРАР с дополнительной инсуффляцией кислорода или без нее улучшает параметры оксигенации в сравнении с послеоперационной СРАР-терапией или без нее. При выборе параметров СРАР-терапии используется титрация положительного давления конца выдоха (ПДКВ) от 5 до 10–12 см вод.ст; при выборе параметров Be-level ПДКВ титруется в диапазоне от 5 до 10–12 см вод.ст., а давление поддержки (P high) — в диапазоне 15–25 см вод.ст.; время рампы (T ramp) устанавливается на среднюю величину.
Положение пациентов. Отмечается улучшение показателей индекса апноэ-гипопноэ в положении на боку или в приподнятом положении.
Мониторинг. Непрерывный послеоперационный мониторинг с пульсоксиметрией эффективен в выявлении гипоксии. Непрерывный мониторинг следует поддерживать до тех пор, пока сохраняется повышенный риск осложнений СОАС.
Выписка и домашний этап. Пациенты с риском СОАС не должны выписываться до стабилизации состояния, то есть пока не будут способны поддерживать адекватный уровень насыщения кислородом на воздухе во время сна. Если пациент с риском СОАС не использовал СРАР-терапию до оперативного вмешательства, рекомендовано проведение диагностической полисомнографии с титрационной ночью для верификации диагноза и подбора адекватного режима респираторной поддержки.
Клинически значимая десатурация должна рассматриваться в двух аспектах ведения периоперационного периода. Первый — это вопрос комфорта и удовлетворенности пациента, просыпание с грубой фрагментацией сна и клинически значимой десатурацией приводит к грубым, кошмарным сновидениям и, как результат, к неудовлетворенности пациента.
Второе направление — увеличение частоты развития кардиоцеребральных нежелательных событий — гипертензивных кризов, гиповентиляции с нарастанием гиперкапнии, нарушений ритма, вплоть до фатальных пробежек фибрилляции желудочков. Нелеченый СОАС независимо ассоциируется с сердечно-легочными осложнениями, в частности с неплановыми интубациями трахеи и инфарктом миокарда [6]. По данным Kaw et al., СОАС ассоциировался с ростом послеоперационной десатурации, острой дыхательной недостаточности, осложнений сердечно-сосудистой системы и госпитализацией в реанимацию [7]. Однако нет обширных литературных данных об увеличении показателей периоперационной летальности, связанной с наличием СОАС, в том числе недиагностированного.
Несмотря на рекомендации ASA о необходимости разработки протоколов ведения пациентов с СОАС, почти половина респондентов среди канадских анестезиологов либо не знали о наличии протокола СОАС у них в клинике, либо сказали об отсутствии данного протокола вообще [10]. Тем не менее, согласно опросу, за последние 10 лет увеличилась как частота диагностики СОАС, так и количество пациентов с СОАС, хотя неясно — это результат роста осведомленности врачей-анестезиологов или увеличение распространенности СОАС среди населения, или и то и другое.
В продолжение изучения периоперационных рисков интересные данные представили британские анестезиологи в отчете о 60 умерших пациентах с СОАС после ортопедических (12), общехирургических (12), бариатрических (10), лор-операций (10), кардиохирургических (4) и урологических (9). Патогистологическое подозрение о генезе осложнений сформировалось из-за наличия гистологических признаков отека легких, связанного с выраженным отрицательным внутриальвеолярным давлением — сохраняющаяся спонтанная дыхательная активность при коллапсе и обструкции ротоглотки [11].
Из 60 пациентов 26 летальных исходов, 17 пациентов с ишемически-гипоксическим поражением головного мозга, 12 пациентов с острой дыхательной недостаточностью и 5 пациентов с успешной сердечно-легочной реанимацией.
Пятьдесят пациентов (83 %) с диагнозом СОАС до операции. Одиннадцать (31 %) находились на СРАР-терапии до операции, из них четыре (36 %) продолжали СРАР в послеоперационном периоде. Десять пациентов были с недиагностированным диагнозом СОАС до операции. Все получали суточную дозу морфина 10 мг. В первые 24 часа произошли 80 % кардиореспираторных событий.
CPAP-терапия в анализе отчета. Из 60 пациентов с СОАС только 11 (18,3 %) получали СРАР-терапию до операции. Из них 7 (63,6 %) не получали СРАР после операции. Они либо умерли, либо получили аноксическое повреждение головного мозга.
Опиаты. Сравнительный анализ между введением опиатов и наличием СОАС показал, что парентеральный путь введения опиатов вызывал более высокую частоту осложнений в сравнении с эпидуральным (71 против 19 %), а также линейную зависимость дозы опиатов/вероятности смерти (относительный риск 1,0, 1,5 и 3,0 при опиоидных дозах < 10 мг, 10–25 мг и > 25 мг; р < 0,005).
Время и размещение. В первые 24 часа после операции произошло 80 % осложнений. В хирургических отделениях произошли 67 % осложнений, 13 % — в операционных, 18 % — в отделениях АИТ, 2 % — дома после выписки [11].
Таким образом, можно сделать вывод о важности оптимизации периоперационного периода у пациентов с СОАС. Непрерывный послеоперационный мониторинг в течение первых 24 часов и улучшение соблюдения CPAP могут снизить риски смерти.
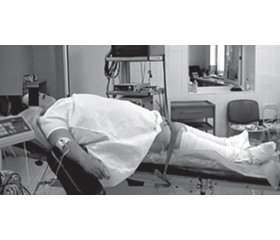
Отражением развития периоперационных дыхательных осложнений является типичный клинический случай — пациентка М., 72 года, после выполненной лапароскопической холецистэктомии, абдоменопластики.
Ранний послеоперационный период, после восстановления сознания, нейромышечной проводимости, мышечного тонуса, адекватных дыхательных движений экстубирована, находится в положении анти-Тренделленбург. При проведении записи полисомнографии в течение 60 минут отмечаются залповые гипопноэ с десатурацией до 79 %, сопровождающиеся выраженным храпом.
Следует отметить, что анестезиологический монитор витальных функций пациента не регистрирует кратковременные десатурации, что создает видимость мнимого благополучия.
Применение режима СРАР с ПДКВ 7 см вод.ст. в данном случае полностью устранило гиповентиляцию и нормализовало показатели сатурации.
Из 22 пациентов, у которых использовалась СРАР-терапия в раннем постэкстубационном периоде, выход из постнаркозной депрессии был гладким. Ритм и глубина дыхания удовлетворительные, не отмечалось ни инструментальных, ни клинических признаков обструкции ротоглотки. Показатели сатурации 94–97 % в режиме СРАР с ПДКВ +7–8 см вод.ст. Пациенты просыпались в состоянии комфорта, без неприятных сновидений, кошмаров, кардиореспираторных осложнений.
Логическим продолжением анализа литературы являются разработка и имплементация в практику клиники Протокола по периоперационному ведению пациента с СОАС, представленного ниже [11].
Протокол периоперационного ведения пациентов с СОАС
Предоперационный этап
1. Анамнез (храп, остановки дыхания во сне, дневная сонливость, ожирение, наличие сахарного диабета).
2. Осмотр (ожирение, лор-врач — арефлексия мягкого неба, объем мягких тканей шеи).
3. Скрининговая шкала STOP-Bang (табл. 3).
При высоком риске наличия СОАС (если время позволяет) — скрининговая полисомнография. Затем при наличии СОАС принятие решения: или отложенная операция, пробная СРАР-терапия, или оперативное вмешательство с соблюдением необходимых предосторожностей: учет рисков трудной интубации трахеи, выбор анестетиков с минимальной депрессией дыхания; активное использование местной/проводниковой или нейроаксиальной анестезии; мониторинг пульсоксиметрии/капнометрии; экстубация только после полного пробуждения и полного восстановления нейромышечного проведения на боку, в приподнятом положении.
Если оперативное вмешательство ургентное — анестезиологическое пособие с соблюдением необходимых предосторожностей (см. выше).
Интраоперационный этап
1. У пациентов с СОАС выбрать минимальный объем вмешательства.
2. Минимальное время операции.
3. Выбор в пользу местной/проводниковой/нейроаксиальной анестезии.
4. Пациенты с СОАС расцениваются как группа риска сложной интубации/экстубации трахеи.
Послеоперационный период
1. Минимизировать использование опиоидов и седативных препаратов.
2. Выбор в пользу парацетамола, НПВП, проводниковой/нейроаксиальных блокад.
3. Постоянно контролировать оксигенацию в послеоперационном периоде.
4. Пациенты с известным диагнозом СОАС должны использовать CPAP после операции.
5. Выписка из больницы после стабильных показателей оксигенации на воздухе в ночное время.
6. Консультация в центре сна после выписки из больницы.
Выводы
В результате анализа литературы, результатов собственных наблюдений клинических случаев мы пришли к выводу, что можно и нужно учитывать риски наличия СОАС у пациента в периоперационном периоде. Регулярное использование протокола по периоперационному ведению пациентов с СОАС позволит открыть новые возможности в практике анестезиолога, связанные:
— с вопросами безопасности в анестезии — отсутствие коллапса ротоглотки и снижение частоты периоперационных осложнений, таких как нарушения ритма, остановки дыхания, остановки сердца, постгипоксические повреждения головного мозга;
— повышением уровня комфорта пациентов в результате улучшения качества дыхания во сне и структуры сна в периоперационном, а особенно в послеоперационном периоде.
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов при подготовке данной статьи.

/132-1.jpg)
/134-1.jpg)
/134-2.jpg)
/135-1.jpg)