Журнал «Медицина неотложных состояний» №3(98), 2019
Вернуться к номеру
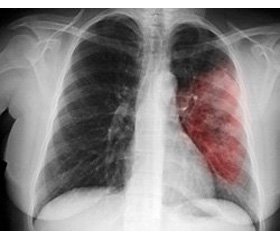
Клинический случай успешного лечения тяжелой внебольничной пневмонии, ассоциированной с вирусом гриппа ВH3N2
Авторы: Клигуненко Е.Н.(1), Корпусенко В.Г.(2), Болтянский С.В.(2), Рудейченко С.В.(2), Матушак А.М.(2), Олейник В.И.(2), Корнеева Е.В.(2), Медведев А.А.(2), Новгородцева Е.П.(2)
(1) — ГУ «Днепропетровская медицинская академия МЗ Украины», г. Днепр, Украина
(2) — КУ «Днепровское клиническое отделение скорой медицинской помощи» ДОС, г. Днепр, Украина
Рубрики: Медицина неотложных состояний
Разделы: Справочник специалиста
Версия для печати
Проблема лікування тяжких пневмоній, у тому числі й вірусних (вірусно-бактеріальних), зберігає свою високу актуальність і вимагає впровадження алгоритму клініко-діагностичних заходів для забезпечення адекватної лікувальної тактики в даній нозологічній групі. У статті розглянуто клінічний випадок інтенсивної терапії пацієнта з позалікарняною двосторонньою полісегментарною пневмонією.
Проблема лечения тяжелых пневмоний, в том числе и вирусных (вирусно-бактериальных), сохраняет свою высокую актуальность и требует внедрения алгоритма клинико-диагностических мероприятий для обеспечения адекватной лечебной тактики в данной нозологической группе. В статье рассмотрен клинический случай интенсивной терапии пациента с внегоспитальной двусторонней полисегментарной пневмонией.
The problem of treating severe pneumonia (including viral, viral-bacterial) is still of high relevance and requires the implementation of an algorithm of clinical diagnostic measures to ensure adequate therapeutic tactics in this nosological group. The article describes a clinical case of intensive care of a patient with community-acquired bilateral multilobar pneumonia.
пневмонія; гострий респіраторний дистрес-синдром; ШВЛ; рекрутмент; пермісивна гіперкапнія; синдром поліорганної недостатності
пневмония; острый респираторный дистресс-синдром; ИВЛ; рекрутмент; пермиссивная гиперкапния; синдром полиорганной недостаточности
pneumonia; аcute respiratory distress syndrome; mechanical ventilation; recruitment; permissive hypercapnia; мultiple organ dysfunction syndrome
Введение
Пневмония — группа различных по этиологии, патогенезу и морфологии острых инфекционно-воспалительных процессов с преимущественным вовлечением паренхимы легких и формированием внутриальвеолярной воспалительной экссудации. Летальность от внебольничной пневмонии (ВП) составляет 47 % от летальности вследствие болезней органов дыхания. В 10 % случаев ВП характеризуется тяжелым течением, требующим госпитализации в отделение реанимации и интенсивной терапии, а летальность в этой группе составляет 15–30 %. Вирусные инфекции — причина 5 % всех тяжелых пневмоний, причем основное значение имеют вирусы гриппа. При неблагоприятном течении гриппа развивается вирус-опосредованное поражение (вплоть до цитолиза) эндотелиоцитов дыхательных путей, в первую очередь бронхиол и альвеол, с массивной экссудацией в интерстиций, нарушением синтеза сурфактанта, микроателектазированием и формированием респираторного дистресс-синдрома. Острая дыхательная недостаточность вследствие респираторного дистресс-синдрома является основной причиной летальности у данных больных на первоначальном этапе лечения в отделении интенсивной терапии (ОИТ), досуточная летальность составляет ≈ 50 % от общей летальности. На последующих этапах лечения летальность обусловлена контаминацией дыхательных путей с присоединением бактериального компонента, прогрессированием полиорганной недостаточности вследствие гипоксического поражения, органоспецифической тропности вирусов, осложнений медикаментозной терапии и искусственной вентиляции легких (ИВЛ).
Таким образом, во всем мире, несмотря на достаточно большой выбор противовирусных и антибактериальных препаратов, а также современные технологии лечения, проблема тяжелых пневмоний, в том числе и вирусных (вирусно-бактериальных), сохраняет свою высокую актуальность.
Клинический случай
Больной Б., 48 лет, 98 кг, переведен в отделение анестезиологии, реанимации и интенсивной терапии (ОАИТ) КУ «Днепровское клиническое отделение скорой медицинской помощи» ДОС на 7-е сутки от начала заболевания из ОИТ инфекционной больницы, где находился в течение двух суток с диагнозом «внегоспитальная двусторонняя полисегментарная пневмония». В течение двух суток нахождения в ОИТ инфекционной больницы динамика отрицательная, несмотря на проводимую терапию, в том числе антибактериальную (клиндамицин + моксифлоксацин), за счет прогрессирования дыхательной недостаточности
На момент поступления в ОАИТ состояние больного тяжелое, уровень сознания — глубокое оглушение. Дыхание спонтанное через естественные дыхательные пути. Оксигенация через маску с резервуаром. При этом частота дыхательных движений — 36/мин, частота сердечных сокращений — 132 уд/мин, артериальное давление — 220/100 мм рт.ст., сатурация кислородом крови (SaO2) — 80 %, температура тела — 37,8 °С. В анализах: лейкоцитоз — 17,0 Г/л, сдвиг формулы влево, абсолютная и относительная лимфоцито- и моноцитопения; азотемия: мочевина — 46,9 ммоль/л, креатинин — 420 мкмоль/л. В анализе газов крови и кислотно-щелочного состояния (КЩС) (FiO2 = 0,5): рНа — 7,305, РаСО2 — 32,2 мм рт.ст., РаО2 — 42 мм рт.ст., ТСО2 — 17,1, НСО3 — 16,1, ВЕ — 10,5, SаО2 — 73,4 %, РаО2/FiО2 — 90 мм рт.ст., PORT — 128 баллов, APACHE II — 23 балла, SOFA — 8 баллов.
Выполнена интубация трахеи, и больной переведен на ИВЛ в протективном режиме аппаратом Maquet (ServoAir), на фоне медикаментозной седации и миоплегии, с паттерном вентиляции VC-SIMV → DC-SIMV, дыхательный объем — 500 мл, Ti : Te — 1 : 2 → Ti : Te — 1 : 1, FiO2 — 1,0, РЕЕР — 10 → 18 см вод.ст., коррекция частоты дыхания по постоянной времени (τ). Несмотря на проводимую ИВЛ с инверсией соотношения Ti : Te до 1 : 1 и поднятие РЕЕР до 18 см вод.ст., относительная нормоксемия (SaO2 — 88–91 %) оставалась достижима только при FiO2 1,0. В связи с сохраняющейся выраженной кислородозависимостью дважды проведен маневр рекрутмента (первый раз — по давлению, второй — по объему) — без выраженного эффекта. Больной переведен в pron-позицию с шинированием плечевого пояса и диафрагмы, повторно выполнен рекрутмент по объему — с положительной динамикой. Удалось добиться относительной нормоксемии при снижении FiO2 до 0,8, а затем и до 0,6 в течение 12 ч. К концу первых суток, на фоне продолжающейся ИВЛ в протективном режиме с использованием концепции driving pressure и снижения FiО2 до 0,6, достигнуто состояние нормоксемии с пермиссивной гиперкапнией: рНа — 7,193, РаСО2 — 51,8 мм рт.ст., РаО2 — 83 мм рт.ст., ТСО2 — 21,5, НСО3 — 19,9, ВЕ — 8,5, SаО2 — 93 %, РаО2/FiО2 — 138 мм рт.ст. Получено лабораторное подтверждение вируса гриппа ВH3N2, установлен диагноз «внегоспитальная двусторонняя полисегментарная пневмония, ассоциированная с вирусом гриппа ВH3N2, острая дыхательная недостаточность 3-й степени паренхиматозного генеза. Сепсис. Синдром полиорганной недостаточности (легкие — недостаточность, почки — недостаточность, печень — дисфункция)». На вторые сутки пребывания в ОАИТ, после стабилизации респираторных показателей, выполнена трахеостомия, проведена санационная бронхоскопия, которая в дальнейшем проводилась ежедневно. В течение трех суток продолжалась протективная ИВЛ на фоне медикаментозной седации и миоплегии с паттерном вентиляции DC-SIMV с ежедневным переводом в pron-позицию на 8 часов.
С третьих суток пребывания в стационаре течение заболевания с отрицательной динамикой за счет нарастания полиорганной недостаточности, в первую очередь почечной, с переходом недостаточности в несостоятельность в виде олигурии > 16 ч, несмотря на стимуляцию диуреза адекватными дозами салуретиков и нормализацию кислородного паттерна и КЩС (при FiO2 0,5): рНа — 7,387, РаСО2 — 51,4 мм рт.ст., РаО2 — 66 мм рт.ст., ТСО2 — 32,5, НСО3 — 30,9, ВЕ — 5,7, SаО2 — 92 %. При этом наблюдался рост азотемии (мочевина — 108 ммоль/л, креатинин — 612 мкмоль/л). Переход в полиурическую стадию на пятые сутки от момента прогрессии острой почечной недостаточности (ОПН). Почечная заместительная терапия не проводилась по техническим причинам. По мере перехода в полиурическую стадию ОПН у больного на фоне постепенного снижения уровня мочевины развился гиперосмолярный синдром с неконтролируемым ростом уровня Na, который носил, по-видимому, компенсаторный (на момент возникновения) характер, направленный на поддержание вне- и внутриклеточной изоосмолярности. Расчетная осмолярность плазмы крови составляла > 400 мосм/л (Na — 177,3 ммоль, мочевина — 43,9 ммоль/л). Учитывая опасность внутриклеточной гипергидратации при быстрой коррекции осмолярности, был выбран ступенчатый подход к ее коррекции в объеме не более 20 % от расчетной потребности в сутки. Коррекция гипер–осмолярности проводилась путем введения через назогастральный зонд дистиллированной воды, а также внутривенной инфузии гипотонического 0,45% раствора NaCl в течение 16 суток — до достижения нормальных расчетных значений осмолярности.
Также у больного на третьи сутки возникли нарушения сердечного ритма по типу пароксизма трепетания предсердий с блоком проведения 2 : 1 и гипотонией, потребовавшие проведения электроимпульсной терапии. Восстановлен синусовый ритм, который и удерживался в дальнейшем.
На 8-е сутки нахождения в ОАИТ (15-е сутки от начала заболевания), одновременно с относительной стабилизацией показателей газообмена и респираторного драйва (FiO2 0,5): рНа — 7,566, РаСО2 — 57,8 мм рт.ст., РаО2 — 81 мм рт.ст., ТСО2 — 54,2, НСО3 — 52,5, ВЕ — 25,7, SаО2 — 96,9 %, статический комплайенс (Cst) — 42 мл/мбар, позволивших прекратить медикаментозную седацию с восстановлением сознания, выявлен неврологический дефицит в виде глубокого тетрапареза и гипоалгезии конечностей. Установлен диагноз «миопатическая квадриплегия критического состояния». В терапию включена патогенетическая медикаментозная терапия (в том числе ингибиторами холинэстеразы), кинезиотерапия. Лечебная тактика эффективна, получен достаточный регресс неврологической симптоматики к 22-м суткам от ее диагностики.
На фоне проводимой терапии состояние больного с положительной динамикой, проявления синдрома полиорганной недостаточности купированы, респираторная поддержка снижена. Проводилась смена режимов вентиляции в следующем порядке: РC-SIMV+PS с постепенным уменьшением количества аппаратных вдохов до 0 → CPAP + PS с постепенным снижением PS и вентиляцией в положении сидя, с постепенно увеличивающимися периодами спонтанного дыхания. Полностью ИВЛ удалось прекратить на 22-е сутки с момента ее начала. Трахеостома деканюлирована на 26-е сутки пребывания в стационаре.
С 12-х суток от начала заболевания на фоне повторного снижения Cst с целью профилактики фибропролиферативного синдрома проведена пульс-терапия метилпреднизолоном.
Во время пребывания больного в ОАИТ с целью поиска возможного возбудителя, коррекции проводимой антибактериальной терапии выполнялись микроскопические и бактериологические исследования бронхоальвеолярных смывов: первый посев (2-е сутки) — роста нет, второй посев (9-е сутки) — Clebsiella pneumoniae 106 КОЕ/мл, третий (21-е сутки) — Enterobacter cloacae 104 КОЕ/мл. Последовательная смена режимов антибактериальной терапии, проводимая по результатам чувствительности: меронем + линезолидин, тазпен + линезолидин, ципрофлоксацин + браксон.
Азотистый баланс поддерживался по результатам метаболического мониторинга (потери белка достигали 435 г/сут, или 4,4 г/кг/сут) с помощью комбинированного парентерально (инфезол)-энтерального (пептамен AF) питания в адекватных потерям дозировках с учетом уровня азотемии.
После стабилизации состояния, на 33-и сутки пребывания в ОАИТ, больной был переведен в терапевтическое отделение, откуда в дальнейшем выписан домой.
Выводы
1. Наличие значительного количества больных с внебольничными (в том числе вирусными и вирусно-бактериальными) пневмониями, требующих лечения в условиях ОАИТ, трудоемкость и непредсказуемость эффекта лечебных действий требуют внедрения алгоритма клинико-диагностических мероприятий для обеспечения адекватной лечебной тактики в данной нозологической группе.
2. Целью стартовой интенсивной терапии у больных с острой дыхательной недостаточностью, обусловленной тяжелой пневмонией (в том числе и постгриппозной), является ранняя респираторная стабилизация, цель которой — достижение относительной нормоксемии: РаО2 ≥ 60 мм рт.ст., SаО2 ≥ 90 % при принудительной ИВЛ с паттерном VC-CMV (PC-CMV, DC-CMV) при Vt ≤ 6 мл/кг, FiO2 ≤ 0,6, при РЕЕР 5–20 см вод.ст., Ppeak ≤ 35 см вод.ст., Pplat ≤ 30 см вод.ст., Pmean ≤ 20 см вод.ст. При этом допустимой является вентиляция в режиме пермиссивной гиперкапнии с рНа ≥ 7,2, инверсия Ti : Te с 1 : 2 в 1 : 1, лимитированная величиной рНа и РаСО2, частота дыханий подбирается индивидуально по постоянной времени (τ). При асинхронии ИВЛ показана медикаментозная седация, в случае неэффективности которой, а также при выполнении определенных лечебных процедур (ИВЛ в pron-позиции, рекрутмент) — мио–релаксация.
3. Для снижения уровня респираторной поддержки и перевода больного на спонтанное дыхание необходимо использование имеющихся протоколов прекращения длительной ИВЛ с учетом имеющегося в конкретном лечебном учреждении оборудования. Оптимальным, по нашему мнению, является следующий алгоритм: VC-CMV (РC-CMV), РC-SIMV+PSV с постепенным уменьшением количества аппаратных вдохов до 0, PSV (BIPAP) с постепенным снижением Ppeak (Phigh) до уровня PEEP (baseline), PC-CSV (CPAP, PS или PV), спонтанное дыхание. Перевод на спонтанное дыхание (эпизодическое, а затем и постоянное) осуществляется при позитивных критериях успешного отлучения от ИВЛ, после оценки работоспособности дыхательной мускулатуры (VC ≥ 30 мл/кг, Vt ≥ 6 мл, f ≤ 26 в 1 мин), оценки дыхательного драйва (P 0,1 ≤ 4,5 см вод.ст.), паттерна дыхания (f/Vt ≤ 100) и при положительном тесте спонтанного дыхания.
4. Позднее начало инвазивной ИВЛ (фатальные нарушения ритма, нестабильность гемодинамики, острый гипоксический психоз) является грубой тактической ошибкой и требует в дальнейшем значительных усилий для стабилизации кислородного режима.
5. При планируемой длительной ИВЛ целесо–образно раннее наложение трахеостомы (сразу после первичной респираторной стабилизации больного).
6. Терапия полиорганной недостаточности требует взвешенного подхода и должна учитывать не только величины отклонения от нормы, но и продолжительность этих изменений, так как некоторые из них могут иметь компенсаторный характер.
7. Выбор стартовой антибиотикотерапии должен учитывать тяжесть состояния больного, особенности микрофлоры (предполагаемые возбудители и чувствительность), сезонность (ОРВИ, грипп), профессии (медработники, лица, контактирующие с антибактериальными средствами), нахождение в стационаре в течение последних трех месяцев, наличие сопутствующей патологии (хроническая обструктивная болезнь легких, нарушения ритма с удлинением периода QT, сахарный диабет), предварительную неэффективную терапию антибактериальными средствами. На последующих этапах лечения возможна модификация антибиотикотерапии в соответствии с изменяющимся микробиологическим профилем.
8. Метаболический мониторинг является обязательной частью интенсивной терапии данной категории больных и осуществляется по определению суточных потерь азота (мочевина мочи). Положительный азотистый баланс поддерживается за счет энтерального (зондового), а при необходимости и комбинированного парентерально-энтерального питания.
1. 10 ведущих причин смерти в мире. Информационный бюллетень № 310. Май, 2014. Availableat: http://www.who.int/mediacentre/factsheets/fs310/ru/.
2. Вирусная пневмония грипп А (H1N1), осложненная ОРДС / Ю.С. Полушин, К.Н. Храпов М.Ю. Майская, К.В. Дикарев // Общая реаниматология. — 2010. — № 3. — С. 15-22.
3. Светлицкая О.И. Острое повреждение легких у пациентов с вирусно-бактериальной пневмонией на фоне избыточной массы тела и ожирения / О.И. Светлицкая, И.И. Канус // Медицинские новости. — 2013. — № 3. — С. 6-10.
4. Mortality Rates for Patients With Acute Lung Injury / ARDS Have Decreased Over Time / M. Zambon, J.-L. Vincent // Chest. — 2008. — Vol. 133. — P. 1120-1127.