Журнал «Медицина неотложных состояний» №4(99), 2019
Вернуться к номеру
Роль сукцинатоксидазного окисления в интенсивной терапии тяжелой черепно-мозговой травмы
Авторы: Черний В.И.(1), Андронова И.А.(2) , Городник Г.А.(2) , Черний Т.В.(1), Андронова М.А.(2)
(1) — Научно-практический центр профилактической и клинической медицины, г. Киев, Украина
(2) — Донецкий национальный медицинский университет
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Мета: вивчення особливостей цереброкардіальних взаємодій у пацієнтів із тяжкою черепно-мозковою травмою (ТЧМТ) і їх змін при використанні в інтенсивній терапії (ІТ) похідних бурштинової кислоти — препаратів цитофлавін і етилметилгідроксипіридину сукцинат. Матеріали та методи. Групу порівняння становили 12 хворих із діагнозом ТЧМТ, які отримували ІТ за стандартним протоколом. Групу дослідження (ГД) становили 74 пацієнтів з ТЧМТ: 43 хворих, які отримували, крім стандартного протоколу, цитофлавін (5 мл у 100 мл фізіологічного розчину внутрішньовенно 1 раз на добу), і 31 хворий, який отримував додатково до стандартного протоколу етилметилгідроксипіридину сукцинат (5 мл у 100 мл фізіологічного розчину внутрішньовенно 1 раз на добу). Тривалість ІТ — від 10 діб до 8 міс. Із пацієнтів ГД 9 осіб померли, у 5 пацієнтів гостра церебральна недостатність трансформувалася у вегетативний стан. Діагноз вегетативного стану в пацієнтів ГД був виставлений у динаміці спостереження на підставі прийнятих міжнародних критеріїв, затверджених Американською академією неврології. У динаміці терапії проводили аналіз рівня свідомості за шкалою коми Глазго, Глазго-Пітсбурзькою шкалою коми й шкалою результатів Глазго, параметрами комп’ютерної томографії (Philips Brilliance CT), показниками кількісної електроенцефалографїї (кЕЕГ) (система Nihon Kohden Corporation EEG-1200K), варіабельності серцевого ритму (ВСР) («Ютас ЮМ 200»). Статистична обробка даних була проведена за допомогою програми MedStat. Результати. В умовах ТЧМТ центральний контур регуляції ВСР зміщувався від вегетативних центрів довгастого мозку в ділянку ретикулярної формації стовбура й середнього мозку й проекцію дна IV шлуночка. Про це свідчать виявлені середні й сильні прямі кореляційні зв’язки між параметрами ВСР і рівнями потужності дельта-діапазону («патологічна» повільнохвильова активність), максимально в проекції окципітальних і лобових відділів кори; активністю нейрогліального пулу ЦНС (спектр-потужність (СП) кЕЕГ у діапазоні 0,5–1 Гц), максимально в зонах проекції стовбурових утворень (С3С4; О1О2); активністю адренергічних нейромедіаторних структур ЦНС (СП кЕЕГ 4–5 Гц), максимально в зонах проекції стовбурових утворень (С3С4; Т3Т4); середні зворотні кореляційні зв’язки між параметрами ВРС і рівнями потужності тета- і альфа-1-діапазонів, максимально в проекції окципітальних і центральних відділів кори; активність холін- (СП кЕЕГ 6–7,5 Гц) і дофамінергічних (СП кЕЕГ 11–12 Гц) систем ЦНС, максимально в зонах проекції стовбурових утворень (С3С4; О1О2). В умовах ТЧМТ з несприятливим результатом (летальний кінець) не існувало єдиного центрального контуру регуляції ВРС, виявлені одночасні конкурентні впливи з боку таламокортикальних, таламогіпоталамічних структур; ретикулярної формації діенцефального рівня. Застосування препаратів — похідних бурштинової кислоти (цитофлавін і етилметилгідроксипіридину сукцинат) у пацієнтів із ТЧМТ приводило до відновлення рівноправних впливів традиційного центрального контуру — центри довгастого мозку, гіпоталамо-гіпофізарна ділянка — на формування ВСР. Цікаво, що ефекти етилметилгідроксипіридину сукцинату були пов’язані більшою мірою з динамікою параметрів кЕЕГ, що відображають зміни на верхньостовбуровому й кірковому рівні ЦНС, а використання цитофлавіну — переважно зі змінами параметрів кЕЕГ, які є нейрофізіологічними предикторами динаміки на рівні середнього мозку, діенцефальної, таламічної й лімбіко-гіпокампальної ділянок ЦНС. Висновки. Параметри цереброкардіальних взаємодій при ТЧМТ і їх зміни є інформативними для оцінки ефективності ІТ і прогнозування результату.
Цель: изучение особенностей цереброкардиальных взаимодействий у пациентов с тяжелой черепно-мозговой травмой (ТЧМТ) и их изменений при использовании в интенсивной терапии (ИТ) производных янтарной кислоты — препаратов цитофлавин и этилметилгидроксипиридина сукцинат. Материалы и методы. Группу сравнения составили 12 больных с диагнозом ТЧМТ, которые получали ИТ по стандартному протоколу. Группу исследования (ГИ) составили 74 пациентов с ТЧМТ: 43 больных, получавших, кроме стандартного протокола, цитофлавин (5 мл в 100 мл физиологического раствора внутривенно 1 раз в сутки), и 31 больной, получавший дополнительно к стандартному протоколу этилметилгидроксипиридина сукцинат (5 мл в 100 мл физиологического раствора внутривенно 1 раз в сутки). Длительность ИТ — от 10 суток до 8 мес. Из пациентов ГИ 9 человек умерли, у 5 пациентов острая церебральная недостаточность трансформировалась в вегетативное состояние. Диагноз вегетативного состояния у пациентов ГИ был выставлен в динамике наблюдения на основании принятых международных критериев, утвержденных Американской академией неврологии. В динамике терапии проводили анализ уровня сознания по шкале комы Глазго, Глазго-Питсбургской шкале комы и шкале исходов Глазго, параметров компьютерной томографии (Philips Brilliance CT), количественной электроэнцефалографии (кЭЭГ) (система Nihon Kohden Corporation EEG-1200K), вариабельности сердечного ритма (ВСР) («Ютас ЮМ 200»). Статистическая обработка данных была проведена с помощью программы MedStat. Результаты. В условиях ТЧМТ центральный контур регуляции ВСР смещался от вегетативных центров продолговатого мозга в область ретикулярной формации ствола и среднего мозга и в проекцию дна IV желудочка. Об этом свидетельствуют выявленные средние и сильные прямые корреляционные связи между параметрами ВСР и уровнями мощности дельта-диапазона («патологическая» медленноволновая активность), максимально в проекции окципитальных и лобных отделов коры; активностью нейроглиального пула центральной нервной системы (ЦНС) (спектр-мощность (СМ) кЭЭГ в диапазоне 0,5–1 Гц), максимально в зонах проецирования стволовых образований (С3С4; О1О2); активностью адренергических нейромедиаторных структур ЦНС (СМ кЭЭГ 4–5 Гц), максимально в зонах проецирования стволовых образований (С3С4, Т3Т4); средние обратные корреляционные связи между параметрами ВСР и уровнями мощности тета- и альфа-1-диапазона, максимально в проекции окципитальных и центральных отделов коры; активностью холин- (СМ кЭЭГ 6–7,5 Гц) и дофаминергических (СМ кЭЭГ 11–12 Гц) систем ЦНС, максимально в зонах проекции стволовых образований (С3С4; О1О2). В условиях ТЧМТ c неблагоприятным исходом не существовало единого центрального контура регуляции ВСР, выявлены одновременные конкурентные влияния со стороны таламокортикальных, таламогипоталамических структур; ретикулярной формации диэнцефального уровня. Применение препаратов — производных янтарной кислоты (цитофлавин и этилметилгидроксипиридина сукцинат) у пациентов с ТЧМТ приводило к восстановлению равноправных влияний традиционного центрального контура — центры продолговатого мозга, гипоталамо-гипофизарная область — на формирование ВСР. Интересно, что эффекты этилметилгидроксипиридина сукцината были связаны в большей мере с динамикой параметров кЭЭГ, отражающих изменения на верхнестволовом и корковом уровне ЦНС, а использования цитофлавина — преимущественно с изменениями параметров кЭЭГ, которые являются нейрофизиологическими предикторами динамики на уровне среднего мозга, диэнцефальной, таламической и лимбико-гиппокампальной областей ЦНС. Выводы. Параметры цереброкардиальных взаимодействий при ТЧМТ и их изменения информативны для оценки эффективности ИТ и прогнозирования исхода.
Background. The objective was to study the features of cerebrocardial interactions in patients with severe traumatic brain injury (STBI) and their changes during the use of succinic acid derivatives — cytoflavin and ethylmethylhydroxypyridine succinate in the intensive care. Materials and methods. The comparison group consisted of 12 patients with the diagnosis with STBI who received all medicines according to the standard protocol. The study group included 74 patients with STBI: 43 persons treated with cytoflavin (5 ml per 100 ml of saline solution intravenously 1 time a day) added to the standard protocol, and 31 individuals who received ethylmethylhydroxypyridine succinate (5 ml per 100 ml of saline solution intravenously 1 time a day) in addition to the standard protocol. Duration of study was from 10 days to 8 months. Nine patients of the study group died, in 5 patients, the acute cerebral insufficiency transformed into vegetative state. The diagnosis of vegetative state in patients of the study group was made in the dynamics of observation on the basis of accepted international criteria approved by the American Academy of Neurology. In the dynamics of therapy, we assessed the level of consciousness using Glasgow Coma Scale, Glasgow-Pittsburgh coma scale and Glasgow Outcome Scale, as well as parameters of computer tomography (Philips Brilliance CT), quantitative electroencephalography (qEEG) (Nihon Kohden Corporation EEG-1200K system) and heart rate variability (Yutas UM 200). The statistical data processing was carried out with MedStat program. Results. In STBI, central contour of heart rate variability regulation is shifted from the vegetative centers of the medulla oblongata to the area of the reticular formation of the brainstem and midbrain and to the projection of the floor of the fourth ventricle. This had been evidenced by the identified medium and strong direct correlations between heart rate variability parameters and: delta-range power levels (“pathological” slow-wave activity), maximal in the projection of the occipital and frontal cortex; activity of the neuroglial pool of the central nervous system (CNS) (qEEG power spectrum in the range of 0.5–1 Hz), maximal in the areas of projection of stem formations (С3С4; О1О2); adrenergic neurotransmitter activity in CNS structures (qEEG power spectrum of 4–5 Hz), maximal in the zones of projection of stem formations (С3С4; Т3Т4); average inverse correlations between the HRV parameters and power levels in theta and alpha-1 bands, maximal in the projection of the occipital and central parts of the cortex; the activity of cholinergic (qEEG power spectrum of 6–7.5 Hz) and dopaminergic (qEEG power spectrum of 11–12 Hz) systems of the CNS, maximal in the zones of projection of stem formations (С3С4; О1О2). In STBI with adverse outcome, there was no single central contour of HRV regulation; simultaneous competitive influences of thalamocortical, thalamohypothalamic structures were revealed; reticular formation of diencephalic level. The use of succinic acid derivatives (cytoflavin and ethylmethylhydroxypyridine succinate) in patients with STBI resulted in the restoration of equal effects of the traditional central contour — centers of the medulla oblongata, pituitary-hypothalamic region — on the formation of heart rate variability. Interestingly that the effects of ethylmethylhydroxypyridine succinate were associated greatly with the dynamics of qEEG parameters reflecting changes in the upper stem and cortical level of the CNS, and the use of cytoflavin — predominantly with qEEG changes that are neurophysiological predictors of the dynamics at the level of the midbrain, diencephalic, thalamic, and limbic-hippocampal regions of the CNS. Conclusions. The parameters of cerebrocardial interactions in STBI and their changes are informative in assessing the effectiveness of intensive care and predicting outcomes.
черепно-мозкова травма; гостра церебральна недостатність; вегетативний стан; бурштинова кислота
черепно-мозговая травма; острая церебральная недостаточность; вегетативное состояние; янтарная кислота
traumatic brain injury; acute cerebral insufficiency; vegetative state; succinic acid
Введение
Черепно-мозговая травма (ЧМТ) характеризуется первичным повреждением мозга, развивающимся в ответ на воздействие механических факторов, которое запускает вторичные множественные деструктивные процессы в центральной нервной системе (ЦНС), обусловленные развитием гипоксии, усугубляющей тяжесть первичного повреждения мозга [1]. Установлено, что как при экспериментальных, так и при клинических формах ЧМТ развивается митохондриальная дисфункция, выражающаяся снижением активности ферментов дыхательной цепи митохондрий (NADH-дегидрогеназа и сукцинатдегидрогеназа) в посттравматический период и уменьшением образования аденозинтрифосфата (АТФ). В работах Л.Д. Лукьяновой [2] показана сигнальная роль митохондрий при адаптации к гипоксии, обосновывается биоэнергетический механизм формирования срочной адаптации к гипоксии. Доказано, что на ранних стадиях гипоксии происходит репрограммирование функционирования субстратного участка дыхательной цепи (переключение окисления НАД-зависимых субстратов на сукцинатоксидазный путь), что позволяет рассматривать сукцинат как сигнальную молекулу, участвующую в регуляции кислородного гомеостаза организма. Наиболее быстрым альтернативным путем коррекции тканевой гипоксии является сукцинатоксидазное окисление, которое достигается путем повышения активности сукцинатдегидрогеназы и улучшения проникновения экзогенного сукцината в митохондрии клетки [3].
С позиций теории систем систему кровообращения (как и любую другую систему организма) можно рассматривать в виде многоуровневой самоуправляемой структуры, состоящей из иерархически связанных элементов: центрального (высшего) и автономного (низшего) контуров управления [4].
В регуляции ритма сердца центральный контур представлен корковыми и подкорковыми образованиями (в частности, гипоталамусом, модуляторным сердечно-сосудистым центром продолговатого мозга).
Автономный контур, представленный синусовым узлом и ядром блуждающего нерва, осуществляет рефлекторную автоподстройку (саморегуляцию) сердечного ритма в связи с дыхательными изменениями кровенаполнения сердечных полостей (в режиме компенсации отклонений).
Диагностический метод, в основу которого положен математический анализ вариабельности сердечного ритма, является наиболее удобным в практическом отношении и теоретически релевантным объектом изучения межсистемных взаимодействий в организме, которые, собственно, и порождают эти колебания [5]. Метод интегрального количественного анализа электроэнцефалограммы (ЭЭГ) [6], амплитудно-когерентный анализ ЭЭГ и математический анализ вариабельности сердечного ритма позволяют дать количественную характеристику центральной нервной и сердечно-сосудистой системам. Поэтому целесообразно провести корреляционный анализ показателей, характеризующих изменение этих систем при тяжелой ЧМТ (ТЧМТ).
Цель: изучение нарушений цереброкардиальных взаимодействий у пациентов с ТЧМТ и их коррекция за счет применения сукцинатсодержащих препаратов.
Материалы и методы
Обследовано 86 пациентов с тяжелой черепно-мозговой травмой, находящихся в отделении нейрохирургической интенсивной терапии (ОНХИТ) ДОКТМО в 2011–2014 гг. Из них группу сравнения (ГС) составили 12 больных с диагнозом ТЧМТ, которые получали интенсивную терапию (ИТ) по стандартному протоколу (СП). Группу исследования (ГИ) составили 74 пациента с ТЧМТ: 43 больных получали дополнительно к СП цитофлавин (5 мл в 100 мл физиологического раствора внутривенно 1 раз в сутки), 31 больной получал дополнительно к СП этилметилгидроксипиридина сукцинат (ЭС) (5 мл в 100 мл физиологического раствора внутривенно 1 раз в сутки). Длительность ИТ — от 10 суток до 8 мес. В качестве контрольной группы (КГ) были обследованы 20 здоровых добровольцев. 54 пациента ГИ были переведены из ОНХИТ на 10–14-е сутки (1-я подгруппа). Из пациентов ГИ 11 человек умерли (2-я подгруппа), у 5 пациентов острая церебральная недостаточность трансформировалась в вегетативное состояние (ВС) (3-я подгруппа) (табл. 1). Диагноз вегетативного состояния у пациентов ГИ был выставлен в динамике наблюдения на основании принятых международных критериев, утвержденных Американской академией неврологии [7]. В ГС 4 пациента умерли. В исследовании выделяли следующие этапы: I — в день поступления в отделение, II — на протяжении ИТ в течение 14 суток, III — перед выпиской из ОНХИТ, IV — после диагностики ВС.
В динамике терапии проводили анализ уровня сознания по шкале комы Глазго (ШКГ) и шкале исходов Глазго, по данным компьютерной томографии (Philips Brilliance CT), количественной ЭЭГ (кЭЭГ) (система Nihon Kohden Corporation EEG-1200K), вариабельности сердечного ритма (ВСР) («Ютас ЮМ 200»). Инструментальные исследования проводили в специально оборудованной лаборатории. ЭЭГ и электрокардиограмму (ЭКГ) регистрировали параллельно у исследуемого на протяжении не менее 30 минут. Наложение ЭЭГ-электродов осуществлялось согласно международной системе «10–20». В качестве аппаратной составляющей диагностического комплекса применяется компьютерный цифровой энцефалограф Nihon Kohden EEG-1200К. Схема коммутации 8-канальная, монополярная, с общими ушными референтными электородами. ЭКГ-отведение регистрируется во II стандартном отведении, синхронно ЭЭГ-каналам. Регистрация биосигналов производилась с частотой квантования 500 Гц. Чувствительность ЭЭГ-каналов — 10 мкВ, ЭКГ — 100 мкВ. Фоновая запись ЭЭГ и ЭКГ производилась длительностью 300 секунд. Использовали фотостимуляционные пробы на частотах 2, 5, 10, 15, 20, 25 Гц. Сохраняли исходные записи биосигналов в цифровом формате, без применения программных средств фильтрации в файл с расширением EDF (European Data Format). Обработка биосигналов производится в программном обеспечении, разработанном в среде графического программирования National Instruments Lab VIEW. Предобработка биосигналов включает процесс программной фильтрации. Применяются сетевые фильтры ЭЭГ- и ЭКГ-каналов с центральной частотой фильтрации 50 Гц. Также для предобработки ЭЭГ-каналов использовали фильтры низких частот с пороговым значением фильтра в 35 Гц и фильтры высоких частот со значением 0,1 Гц.
Спектральный анализ биосигналов производили синхронно в ЭЭГ-отведениях и ЭКГ-канале с помощью математического аппарата быстрого преобразования Фурье. С целью улучшения качества спектрального анализа использовали оконную функцию Ханнинга [8]. Разрешение метода составляет 0,1 Гц. Спектр нативного ЭЭГ-сигнала раскладывается на составляющие диапазоны: дельта — 0,5–3,9 Гц, тета — 4–7,9 Гц, альфа 0 — 8–9 Гц, альфа-1 — 9,5–11 Гц, альфа-2 — 11,5–12,9 Гц, бета-1 — 13–20 Гц, бета-2 — 20,5–35 Гц.
Метод ВСР позволяет судить о степени напряжения регуляторных систем, разобщении процессов центральной и периферической регуляции [9] в соответствии с рекомендациями Североамериканского кардиологического сообщества. Применяли статистические, геометрические методы и анализ частотно-временной области. Из частотных показателей исследовали: TP (мс2) — total power — тотальная мощность спектра. Характеризует только периодические процессы в ритме сердца и не содержит нелинейных и непериодических компонентов. VLF (мс2) — very low frequency — очень низкие частоты, мощность частот в диапазоне 0,003–0,04 Гц, характеризует надсегментарный уровень регуляции симпатического звена автономной нервной системы (АНС) и влияние высших вегетативных центров на сердечно-сосудистую систему. LF (мс2) — low frequency — низкие частоты (НЧ), мощность частот в диапазоне 0,04–0,15 Гц, характеризует влияние симпатического отдела АНС на сердечный ритм, в частности активность вазомоторного центра продолговатого мозга и барорефлекс. HF (мс2) — high frequency — высокие частоты (ВЧ), мощность частот в диапазоне 0,15–0,4 Гц, показатель вагусной активности. LF/HF (НЧ/ВЧ) — симпатовагусный баланс.
Для оценки динамики нейрофизиологических изменений изучали усредненные показатели спектрального анализа ЭЭГ по 8 отведениям, абсолютную и относительную спектральную мощность (ОСМ). Показатели усредняли путем вычисления медианного значения спектральной плотности в каждом диапазоне в 8 отведениях. В качестве интегрального количественного анализа ЭЭГ применяли интегральный коэффициент (ИК), рассчитанный для правой (R) и левой (L) гемисфер соответственно: kfc 1 = (δ + θ + β1)/(α + β2). Интегральный коэффициент отображает соотношение нормальных и патологических ритмов на фоновой ЭЭГ [6]. Реактивность мозга оценивалась по изменению абсолютной спектр-мощности и интегральных коэффициентов на основании классификации типов реакций ЦНС на фармакологическое воздействие [6].
В настоящее время существуют клинико-экспериментальные исследования, связывающие активность определенных диапазонов ЭЭГ с функционированием различных медиаторных систем ЦНС [10, 11].
Медленные биоэлектрические процессы мозга частотой ниже 1 Гц рассматриваются как результат деятельности нейроглиальной популяции с церебральным энергетическим обменом. Коррелят процессов метаболизма: активность 6–7,5 Гц связана с холинергической системой; активность 5–6 Гц — с серотонинергической системой; активность 4–5 Гц — с адренергической активацией; активность 11–12 Гц — с активацией дофаминергической системы; активность 24–25 Гц (бета 2) — с серотонинергической системой.
По данным литературы, основными ЭЭГ-эффектами активации рецепторов глутамата являются усиление ритмов в диапазоне 0,5–3 Гц (то есть в диапазонах дельта-активности) и ослабление — в полосе частот 8–26 Гц (в диапазоне альфа- и бета-ритмов) [11, 12].
Статистическая обработка данных была проведена с помощью программы MedStat [13].
Результаты и обсуждение
При поступлении в отделение у больных ГИ и ГС выраженный неврологический дефицит 4–9 баллов по ШКГ (кома I–III) предопределял резкую дезорганизацию ЭЭГ-паттерна. При визуальной оценке в обеих группах преобладали ЭЭГ кривые IV–V типа (группы 15–20) по классификации Жирмунской — Лосева с преобладанием δ- и θ-активности и минимальным количеством альфа- и бета-ритма [6].
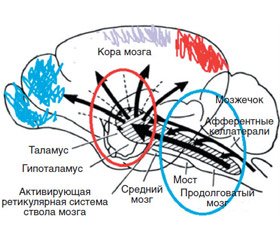
В условиях тяжелой черепно-мозговой травмы c благоприятным исходом (рис. 1) центральный контур регуляции вариабельности сердечного ритма смещается от вегетативных центров продолговатого мозга: в область ретикулярной формации ствола и среднего мозга; в проекцию дна IV желудочка. Об этом свидетельствуют: средние и высокие прямые корреляционные связи (КС) между параметрами ВСР и уровнями мощности дельта-диапазона («патологическая» медленноволновая активность), максимально в проекции окципитальных и лобных отделов коры; активностью нейроглиального пула ЦНС, максимально в зонах проецирования стволовых образований (С3С4; О1О2); активностью адренергических нейромедиаторных структур ЦНС, максимально в зонах проецирования стволовых образований (С3С4; Т3Т4); средние обратные корреляционные связи между параметрами ВРС и уровнями мощности тета- и альфа-1-диапазона, максимально в проекции окципитальных и центральных отделов коры; активностью холин- и дофаминергических систем ЦНС, максимально в зонах проецирования стволовых образований (С3С4; О1О2).
В условиях тяжелой черепно-мозговой травмы c неблагоприятным исходом (рис. 2) не существует единого центрального контура регуляции вариабельности сердечного ритма, есть одновременные конкурентные влияния со стороны: таламокортикальных взаимодействий; таламогипоталамических структур; ретикулярной формации диэнцефального уровня. Об этом свидетельствуют: средние и высокие прямые корреляционные связи между параметрами ВСР и уровнями мощности тета- и бета-диапазонов, максимально в проекции центральных и лобных отделов коры; активностью холинергической нейромедиаторной системы ЦНС, максимально в лобных и центральных отведениях (С3С4; Fp1Fp2); межполушарной когерентностью в диагональных парах переднего (лобно-височная область) и заднего (центрально-окципитальная область) отделов коры больших полушарий; минимальное число средних и высоких обратных корреляционных связей между параметрами ТР, HF, LF, VLF и уровнями нейроглиальной активности ЦНС; межполушарной когерентностью тета- и дельта-диапазонов лобных и височных областей коры.
В отличие от здорового мозга, в условиях острой церебральной недостаточности с последующим исходом в ВС роль центрального контура регуляции ВСР не выполнял единый центр ЦНС (рис. 3).
Выявлено несколько одновременно функционирующих патологических систем, одна из которых включает образования правой гемисферы и структуры диэнцефального уровня (рис. 4), оказывает прямое и реципрокное воздействие на активность парасимпатического кардиоингибиторного центра продолговатого мозга (HF) и функцию центральных эрготропных и гуморально-метаболических механизмов регуляции (VLF) ритма сердца (рис. 3). Показатель VLF и уровни спектральной мощности (СМ) θ-ритма, β2-активности и СМ в узких диапазонах, связанных с активацией серотонинергической нейромедиаторной системы (НС) ЦНС в правой гемисфере — в лобной и височной областях (Fp2T4) — имели высокие прямые корреляционные связи. VLF и СМ δ-диапазона и СМ в диапазоне до 1 Гц, отражающем активность нейроглиального пула ЦНС в правом полушарии, имели высокие обратные корреляционные связи. Показатель HF и правополушарные уровни 1-го интегрального коэффициента (δ + θ + β1)/(α + β2) и СМ в диапазоне до 1 Гц имели высокие прямые корреляционные связи. HF и СМ в диапазонах α-, α1-, β1-ритмов и в диапазонах, отражающих активность серотонин- и дофаминергической НС ЦНС, в проекции правой лобно-височной области (Fp2T4) коры имели высокие обратные КС.
При исследовании динамики изменений цереброкардиальных взаимодействий в ответ на применение сукцинатсодержащих препаратов в интенсивной терапии тяжелой ЧМТ было установлено следующее (табл. 3).
Таким образом, применение препаратов — производных янтарной кислоты (цитофлавин и этилметилгидроксипиридина сукцинат) у пациентов с ТЧМТ приводило к восстановлению равноправных влияний традиционного центрального контура — центры продолговатого мозга, гипоталамо-гипофизарная область — на формирование ВСР. Интересно, что эффекты этилметилгидроксипиридина сукцината были связаны в большей мере с динамикой параметров количественной ЭЭГ, отражающих изменения на верхнестволовом и корковом уровне ЦНС, а использования цитофлавина — преимущественно с изменениями параметров кЭЭГ, которые являются нейрофизиологическими предикторами динамики на уровне среднего мозга, диэнцефальной, таламической и лимбико-гиппокампальной областей ЦНС (табл. 3). Таким образом, сукцинат присутствует в обоих препаратах. Но препарат 2-этил-6-метил-3-оксипиридина сукцинат является структурным аналогом витамина B6 и янтарной кислоты, а цитофлавин — сбалансированным комплексом из двух метаболитов (янтарная кислота, рибоксин) и двух коферментов витаминов (рибофлавин мононуклеотид — витамин В2, никотинамид — витамин РР). Именно компоненты определяют отличие фармакологического действия. Причем на фармацевтическом рынке Украины присутствуют несколько препаратов этилметилгидроксипиридина сукцината: мексикор и аналоги мексидола® (нейротропин, армадин и другие). Принципиальным отличием мексикора, который мы использовали в нашем исследовании, от остальных аналогов является дополнительное количество янтарной кислоты (в мексидоле на 1 молекулу эмоксипина — 1 молекула сукцината, а в мексикоре таких молекул 6) [14].
Необходимо помнить о том, что применение нейрометаболической терапии неэффективно без проведения коррекции вторичных повреждений мозга, восстановления церебрального гомеостаза: коррекции гипоксемии (искусственная вентиляция легких, CPAP), гипотонии (норадреналин, добутамин), гиповолемии (волютенз, гекотон), реологии (реосорбилакт, латрен), гипертермии (инфулган/парацетамол), гипер- и гипогликемии (глюксил, ксилат), гипер- и гипокапнии, внутричерепной гипертензии (сорбилакт в сочетании с L-лизина эсцинатом).
Выводы
1. При тяжелой черепно-мозговой травме с благоприятным исходом центральный контур регуляции вариабельности сердечного ритма смещается от вегетативных центров продолговатого мозга в область ретикулярной формации ствола и среднего мозга, в проекцию дна IV желудочка.
2. При тяжелой черепно-мозговой травме c неблагоприятным исходом не существует единого центрального контура регуляции вариабельности сердечного ритма, развиваются конкурентные влияния со стороны таламокортикальных взаимодействий, таламогипоталамических структур, ретикулярной формации диэнцефального уровня.
3. При тяжелой черепно-мозговой травме с исходом в вегетативное состояние отсутствует единый центральный контур регуляции вариабельности сердечного ритма. В отличие от здорового мозга при развитии вегетативного состояния формируется несколько одновременно функционирующих патологических систем, одна из которых включает образования правой гемисферы и структуры диэнцефального уровня, оказывая прямые и реципрокные воздействия на активность парасимпатического кардиоингибиторного центра продолговатого мозга и функцию центральных эрготропных и гуморально-метаболических механизмов регуляции ритма сердца.
4. Применение препаратов — производных янтарной кислоты (цитофлавин и этилметилгидроксипиридина сукцинат) у пациентов с ТЧМТ приводило к восстановлению равноправных влияний традиционного центрального контура — центры продолговатого мозга, гипоталамо-гипофизарная область — на формирование вариабельности сердечного ритма.
5. Эффекты этилметилгидроксипиридина сукцината связаны преимущественно с изменениями на верхнестволовом и корковом уровне ЦНС. А эффекты цитофлавина связаны преимущественно с изменениями на уровне среднего мозга, диэнцефальной, таламической и лимбико-гиппокампальной областей ЦНС. Таким образом, по фармакологическому действию на ЦНС препараты дополняют друг друга.
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов при подготовке данной статьи.
1. Algattas H., Huanq J.H. Traumatic brain injury pathophysiology and treatments: early, intermediate, and late phases post injury. Int. J. Mol. Sci. 2014. 15(1). 309-341. doi: 10.3390/ijms15010309.
2. Лукьянова Л.Д. Сигнальная роль митохондрий при адаптации к гипоксии. Фізіол. журн. 2013, Т. 59. № 6. С.141-154.
3. Никонов В.В., Чернов А.Л., Феськов А.Э., Соколов А.С., Белецкий А.В. Возможности применения этилметилгидроксипиридина сукцината в комплексной интенсивной терапии острого периода черепно-мозговой травмы. Медицина неотложных состояний. 2018. № 7(94). С. 45-56.
4. Основи теорії систем: навч. посіб. для студ. баз. напрямку 6.050903 «Телекомунікації» / І.В. Демидов; М-во освіти і науки України, Нац. ун-т «Львів. Політехніка», Ін-т телекомунікацій, радіоелектрон. та електрон. техніки, каф. телекомунікацій. Л.: [б. в.], 2013. 210, [1] c.: іл. Бібліогр.: с. 206-210 (64 назви). ISBN 978-966-322-376-6.
5. Баевский P.M., Иванов Г.Г. Вариабельность сердечного ритма: теоретические аспекты и возможности клинического применения. Ультразвуковая и функциональная диагностика. 2001. № 3. С. 106-127.
6. Беленичев И.Ф. и др. Нейропротекция и нейропластичность: монография. К.: Логос, 2015. 512 с.
7. Vegetative State and Minimally Conscious State: A Review of the Therapeutic Interventions. Review Stereotact Funct Neurosurg. 2010. 88. 199-207. DOI: 10.1159/000314354.
8. Дворкович В.П., Дворкович А.В. Оконные функции для гармонического анализа сигналов. М.: Техносфера, 2014. 112 с.
9. Кравченко А.Ю., Зыбайло П.Г., Пушнов В.В., Войнич Ю.В., Барсуков Е.А., Стукачев И.Н. Влияние факторов риска патологии сердечно-сосудистой системы на вариабельность ритма у лиц призывного возраста на фоне артериальной гипертензии. Молодой ученый. 2018. № 16. С. 35-36. URL: https://moluch.ru/archive/202/49598.
10. Андронова И.А., Черний Т.В., Назаренко К.В., Черний В.И., Андронова М.А. Возможности количественной ЭЭГ в исследовании нейромедиаторных систем ЦНС при острой и хронической церебральной недостаточности. Материалы Всероссийской конференции с международным участием «Нейрохимические механизмы формирования адаптивных и патологических состояний мозга», 24–26 июня 2014 г., Санкт-Петербург — Колтуши. С. 17.
11. Шарова Е.В. Современные возможности ЭЭГ в анализе функциональных нарушений при тяжелых повреждениях головного мозга. Нейронауки: теоретичні та клінічні аспекти. 2009. Т. 5. № 1–2. С. 49-58.
12. Черний В.И., Андронова И.А., Городник Г.А., Черний Т.В., Андронова М.А. Нейромедиаторные механизмы восстановления сознания у пациентов с тяжелой черепно-мозговой травмой. Медицина неотложных состояний. 2018. № 1(88). С. 114-121.
13. Лях Ю.Е., Гурьянов В.Г., Хоменко В.Н., Панченко О.А. Основы компьютерной биостатистики: анализ информации в биологии, медицине и фармации статистическим пакетом MedStat. Донецк: Папакица Е.К., 2006. 214 с.
14. Пожилова Е.В., Новиков В.Е., Новикова А.В. Фармакодинамика и клиническое применение препаратов на основе гидроксипиридина. Вестник Смоленской государственной медицинской академии. 2013. № 3. С. 56-66.

/130-1.jpg)
/132-1.jpg)
/133-1.jpg)
/134-1.jpg)
/134-2.jpg)
/131-1.jpg)
/135-2.jpg)