Журнал «Медицина неотложных состояний» №5(100), 2019
Вернуться к номеру
Прогностическая значимость векторкардиографического исследования у больных с острым инфарктом миокарда
Авторы: Белая И.Е., Коломиец В.И., Манищенкова Ю.А.
Государственное учреждение «Луганский государственный медицинский университет»
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Актуальність. Актуальною є оцінка вірогідності векторкардіографічного (ВКГ) дослідження серця хворих із гострим періодом інфаркту міокарда (ІМ) порівняно з електрокардіографічним (ЕКГ) методом. Мета дослідження: визначити передбачувану цінність векторкардіографічного дослідження у хворих із гострим періодом інфаркту міокарда. Матеріали та методи. Обстежено
396 хворих з гострим ІМ лівого шлуночка (180 хворих з ІМ та 216 хворих із поєднаним перебігом ІМ і стеатозу печінки). Вік хворих становив у середньому 61,2 ± 5,1 року. Переважали особи чоловічої статі — 54,55 %. Для отримання більш широкої та глибокої інформації про стан електричної активності серця додатково до ЕКГ використовувалась ЕКГ-методика на удосконаленому кардіодіагностичному багатофункціональному комплексі МТМ-СКМ. Для обчислення співвідношень між результатами даного ВКТ-тесту і стандартом діагностики (ЕКГ) будувалась так звана чотирьохпільна таблиця. Результати. Співвідношення правильно діагностованих пацієнтів за допомогою ВКГ-дослідження дозволяє визначити його чутливість та специфічність. Так, чутливість ВКГ, що визначається відношенням а/(а + с) – 395/(395 + 1), становила 99,7 %, тобто з імовірністю 99,7 % ВКГ покаже позитивний результат у хворих з ІМ. Специфічність ВКГ, що обчислена відношенням d/(d + b) – 30/(30 + 2), дорівнювала 93,8 %, тобто з імовірністю 93,8 % ВКГ дасть негативний результат у хворого, який не має ІМ. Прогностична цінність методу залежить від його чутливості та специфічності. Прогностична цінність позитивного результату, тобто ймовірність наявності ІМ при його ВКГ-ознаках, становила 99,6 % (а/(а + b) – 395/(395 + 2)).
Прогностична цінність негативного результату, тобто ймовірність відсутності ІМ без його ВКГ-ознак, становила 96,8 % (d/(с + d) – 30/(1 + 30)). Висновки. Чутливість ВКГ-методу — 99,7 %, специфічність — 93,8 %. Позитивна прогностична значущість ВКГ — 99,6 %, негативна прогностична значущість ВКГ — 96,8 %.
Актуальность. Актуальной является оценка достоверности векторкардиографического (ВКГ) исследования сердца у больных с острым периодом инфаркта миокарда (ИМ) по сравнению с электрокардиографическим (ЭКГ) методом. Цель исследования: определить предсказательную ценность векторкардиографического исследования у больных с острым периодом инфаркта миокарда. Материалы и методы. Обследованы 396 больных с острым ИМ левого желудочка (180 больных с ИМ и 216 больных с сочетанным течением ИМ и стеатоза печени). Возраст больных составил в среднем 61,2 ± 5,1 года. Преобладали лица мужского пола — 54,55 %. Для получения более обширной и глубокой информации о состоянии электрической активности сердца дополнительно к ЭКГ использовалась ВКГ-методика на усовершенствованном кардиодиагностическом многофункциональном комплексе МТМ-СКМ. Для вычисления соотношений между результатами ВКГ-теста и стандартом диагностики (ЭКГ) строилась так называемая четырехпольная таблица. Результаты. Соотношение правильно диагностированных пациентов с помощью ВКГ-исследования позволяет определять его чувствительность и специфичность. Так, чувствительность ВКГ, определяемая отношением a/(a + c) – 395/(395 + 1), составила 99,7 %, т.е. с вероятностью 99,7 % ВКГ покажет положительный результат у больных с ИМ. Специфичность ВКГ, вычисляемая отношением d/(d + b) – 30/(30 + 2), составила 93,8 %, т.е. с вероятностью 93,8 % ВКГ даст отрицательный результат у больного, не имеющего ИМ. Прогностическая ценность метода зависит от его чувствительности и специфичности. Прогностическая ценность положительного результата, т.е. вероятность наличия ИМ при его ВКГ-признаках, составила 99,6 % (a/(a + b) – 395/(395 + 2)).
Прогностическая ценность отрицательного результата, т.е. вероятность отсутствия ИМ без его ВКГ-признаков, составила 96,8 % (d/(c + d) – 30/(1 + 30)). Выводы. Чувствительность ВКГ-метода — 99,7 %, специфичность — 93,8 %. Положительная прогностическая значимость ВКГ составила 99,6 %, отрицательная прогностическая значимость ВКГ — 96,8 %.
Background. Evaluating the reliability of vectorcardiography (VCG) of the heart in patients with acute myocardial infarction (MI) compared to electrocardiography (ECG) is relevant. The purpose of the research is to determine the prognostic significance of vectorcardiography in patients with acute myocardial infarction. Material and methods. We examined 396 patients with acute left ventricular myocardial infarction (ave-
rage age was 61.2 ± 5.1 years, male patients — 54.55 %). In addition to ECG, we used VCG on the advanced cardiodiagnostic multifunctional complex MTM-SKM. We constructed a so-called four-field table to calculate the correlation between the results of this VCG test and the diagnostic standard (ECG). Results. The sensitivity of VCG, determined by the ratio а/(а + с) – 395/(395 + 1), was 99.7 %. That is, with a proba-bility of 99.7 %, VCG will show a positive result in patients with myocardial infarction. The specificity of VCG, calculated by the ratio d/(d + b) – 30/(30 + 2), was 93.8 %. That is, with a probability of 93.8 %, VCG will give a negative result in a patient who does not have MI. The prognostic value of a method depends on its sensitivity and specificity. The prognostic significance of a positive result, i.e. the probability of having MI with its VCG signs, was 99.6 % (а/(а + b) – 395/(395 + 2)). The prognostic significance of a negative result, that is, the probability of the absence of MI without its VCG signs, was 96.8 % (d/(c + d) – 30/(1 + 30)). Conclusions. The sensitivity of VCG was 99.7 %, specificity — 93.8 %. The positive prognostic significance of VCG was 99.6 %, the negative prognostic significance — 96.8 %.
гострий період інфаркту міокарда; векторкардіограма; чутливість; специфічність; прогностична значущість
острый период инфаркта миокарда; векторкардиограмма; чувствительность; специфичность; прогностическая значимость
acute phase of myocardial infarction; vectorcardiogram; sensitivity; specificity; prognostic significance
Введение
Проблема сочетанной патологии является одной из наиболее актуальных для современной клинической медицины. Особое внимание привлекают полипатии, которые включают инфаркт миокарда (ИМ), в связи с высокой смертностью, составляющей от 10,1 до 32,7 %, и больничной летальностью — 15–16 % [1, 2]. Неблагоприятное течение ИМ могут осложнять хронические патологические процессы в организме, в том числе стеатоз печени, распространенность которого колеблется от 3 до 58 % [3].
Несмотря на то, что электрокардиография (ЭКГ) является основным диагностическим методом при ИМ, его ЭКГ–картина часто неоднозначна, и даже при подтвержденном ИМ, на основании характерной клинической картины и убедительной гиперферментемии, может сразу не проявиться своими классическими признаками, в связи с чем оправдан поиск новых методик электрофизиологического исследования сердца. При этом зарубежными и оте–чественными учеными электрическая активность сердца у больных с ИМ исследована с помощью векторкардиографии (ВКГ) — корригированных ортогональных систем отведений, в том числе по Франку и Мак–Фи — Парунгао, с равноудаленными от геометрического центра сердца электродами. Так, некоторые зарубежные авторы отмечают преимущества векторного анализа ЭКГ перед общепринятым при исследовании ЭДС/С [4, 5], что позволяет изучать величину и направление вектора повреждения ST [6–8], величину максимального вектора QRS и углового расхождения QRS и Т [9], отклонение вектора электрической активности сердца [10] для определения локализации и распространенности ИМ. Российские ученые исследовали особенности распространения возбуждения по миокарду в рубцовой зоне переднеперегородочной локализации [11], состояние «рабочих» кардиомиоцитов при патологии [12, 13], определяли количественные критерии диагностики рубцовых поражений миокарда различной локализации и распространенности [14]. Однако исследователями не применялась система прекардиальных отведений по методике И.Т. Акулиничева в модификации М.Б. Тартаковского, позволяющая снимать потенциалы значительно большей величины, чем при отдаленном расположении электродов, что позволяет уточнять глубину и распространенность некробиотического процесса при различных локализациях ИМ. Поэтому актуальной является оценка достоверности ВКГ–исследования сердца у больных с острым периодом ИМ, в том числе при сочетанной патологии, по сравнению с ЭКГ–методом.
Цель исследования: определить предсказательную ценность векторкардиографического исследования у больных с острым периодом инфаркта миокарда.
Материалы и методы
В инфарктном отделении Луганской городской клинической многопрофильной больницы № 1 обследованы 396 больных с острым периодом ИМ левого желудочка (180 больных с ИМ и 216 больных с сочетанным течением ИМ и стеатоза печени). Возраст больных составил в среднем 61,2 ± 5,1 года. Преобладали лица мужского пола — 216 (54,55 %). Среди обследованных было 180 женщин (45,45 %).
Больные госпитализированы в первые 24 часа от начала развития ИМ. Диагноз ИМ устанавливали в соответствии с рекомендациями Европейского общества кардиологов [15] по клиническим данным, результатам электрокардиографического исследования в динамике и показателям биохимических маркеров некроза миокарда. Для получения более обширной и глубокой информации о состоянии электрической активности сердца дополнительно к ЭКГ использовалась векторкардиографическая (ВКГ) методика. В качестве регистратора применялся современный высокочувствительный кардиодиагностический многофункциональный комплекс МТМ–СКМ Северодонецкого научно–производственного предприятия «Микротерм» (свидетельство о государственной регистрации № 2375/2003, регистрационный № 19081403 от 26 декабря 2003 г., Украина). Векторкардиографически фиксировали петли Р, QRS и Т в системе координат в пяти проекциях (ВА1–5) с последующим анализом величины максимального вектора, площади, скорости распространения импульса по трассе петель Р, QRS и Т. Также были проанализированы данные углового расхождения петель QRS–Т и QRS–Р и наличие размыкания петель QRS и Т. Оценку параметров векторкардиограммы у больных проводили, сравнивая результаты обследования 36 практически здоровых лиц и лиц без признаков перенесенного ИМ. В исследование не включались больные с повторным ИМ и ИМ без зубца Q, более поздними сроками доставки в стационар, органическими поражениями клапанов и острой левожелудочковой недостаточностью III–IV класса по Killip–Kimbal, сахарным диабетом, ожирением и циррозом печени.
Статистическую обработку результатов ВКГ–исследования осуществляли с помощью компьютерной программы Statistica 6.1. При анализе результатов использовали непараметрический U–критерий Манна — Уитни для сравнения двух независимых выборок, критерий Стьюдента — для определения возможных границ ошибок.
Для оценки достоверности примененного в работе диагностического теста (ВКГ) у больных с ИМ использовали наиболее точный (референтный) диагностический метод — ЭКГ. Для вычисления соотношений между результатами данного ВКГ–теста и стандартом диагностики (ЭКГ) строилась так называемая четырехпольная таблица.
Протокол исследования был одобрен этическим комитетом ГУ «Луганский государственный медицинский университет». До включения в исследование у всех участников было получено письменное информированное согласие.
Результаты
Электровекторкардиографически обследованы 396 больных с острым периодом ИМ левого желудочка и 36 человек без признаков ИМ.
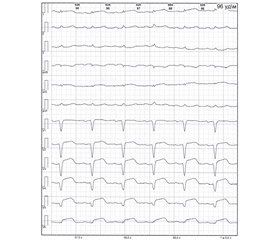
В дополнение к ЭКГ выявлены ВКГ–признаки острого периода Q–ИМ, которые проявлялись: смещением петель QRS в противоположную сторону от области пораженного миокарда; уменьшением их площади в среднем в 6 раз (р < 0,05–0,001); замедлением возбуждения в миокарде в виде локальной внутрижелудочковой блокады; нарушением процессов реполяризации, заключающихся в размыкании петель QRS с появлением вектора повреждения ST и расположением петли Т вне петли QRS, их перекрестом, разнонаправленными изменениями площади петель Т (р < 0,05–0,001), скоростных показателей (р < 0,001) и углового расхождения петель QRS–Т (р < 0,05–0,001) при уменьшении максимального вектора петель Т (р < 0,05–0,01). Кроме того, в периинфарктной зоне векторкардиографически регистрируются разряжение отметок времени по петлям QRS (р < 0,05–0,001) и увеличение площади петель Р в 1,7–3,8 раза (р < 0,05–0,001), отражающие компенсаторную гемодинамическую нагрузку на интактные отделы желудочков и предсердия. Также выявляются нарушения проводимости (сгущение и/или разряжение отметок времени по петлям Р, р < 0,001) и реполяризации в предсердиях в виде разнонаправленных изменений углового расхождения петель QRS–Р (р < 0,05–0,001) [16–18] (рис. 1).
Для определения чувствительности и специфичности ВКГ–метода строилась так называемая четырехпольная таблица (табл. 1).
Согласно данным табл. 1, по результатам ЭКГ–исследования, всего обследованы 396 больных с ИМ (395 больных с ИМ и 1 больной с инфарктоподобной ЭКГ) и 36 больных без признаков ИМ (34 практически здоровых лица и лица без признаков перенесенного ИМ и 2 пациента с полной блокадой левой ножки пучка Гиса). Больные с признаками ИМ на ЭКГ и отрицательным результатом на ВКГ являются ложноотрицательными. Больные без признаков ИМ на ЭКГ и положительным результатом на ВКГ являются ложноположительными. При этом векторкардиографически доказано, что у больного с инфарктоподобной ЭКГ при метаболической кардиомиопатии нет ИМ (ложноотрицательный результат), а у больных с полной блокадой левой ножки пучка Гиса есть признаки ИМ (ложноположительный результат).
Так, у больного с инфарктоподобными изменениями на ЭКГ на фоне спортивного сердца векторкардиографически исключен ИМ и выявлены признаки гипертрофии миокарда левого желудочка (увеличение суммарной площади петель QRS в 1,5 раза) с нарушением процессов реполяризации (угловое расхождение петель QRS–Т увеличено на 35° в 4–й проекции, в ВА1, 4, 5 — сгущение отметок времени по петлям Т) и внутрижелудочковой проводимости (во всех проекциях по петлям QRS — ускорение распространения импульса по миокарду, в ВА1, 4, 5 — почти параллельное расположение начальной и конечной частей петель QRS) в передней стенке левого и, по–видимому, правого желудочков, области верхушки и базальных отделов желудочков, а также нарушение внутрипредсердной проводимости (сгущение отметок времени по петлям Р во всех проекциях) [19] (рис. 2).
Соотношение правильно диагностированных пациентов с помощью ВКГ–исследования позволяет определять его чувствительность и специ–фичность. Так, чувствительность ВКГ, определяемая отношением a/(a + c) – 395/(395 + 1), составила 99,7 %, т.е. с вероятностью 99,7 % ВКГ покажет положительный результат у больных с ИМ. Специфичность ВКГ, вычисляемая отношением d/(d + b) – 30/(30 + 2), составила 93,8 %, т.е. с вероятностью 93,8 % ВКГ даст отрицательный результат у больного, не имеющего ИМ.
Прогностическая ценность метода зависит от его чувствительности и специфичности. Прогностическая ценность положительного результата, т.е. вероятность наличия ИМ при его ВКГ–признаках, составила 99,6 % (a/(a + b) – 395/(395 + 2)).
Прогностическая ценность отрицательного результата, т.е. вероятность отсутствия ИМ без его ВКГ–признаков, составила 96,8 % (d/(c + d) – 30/(1 + 30)).
Обсуждение
Публикации последних лет подтверждают результаты нашего исследования и свидетельствуют о возрастающем интересе к ВКГ–методу. ВКГ начал возрождаться в 90–х годах прошлого столетия, когда стала возможной математическая обработка показателей электрической активности сердца. Это облегчало анализ ВКГ и расширяло диагностическую и прогностическую ценность традиционной 12–канальной ЭКГ [20]. Ряд авторов считают, что компьютеризированная ВКГ может выступать стандартным кардиологическим тестом, в дополнение к ЭКГ, в диагностике кардиоваскулярной патологии [21–23]. Исследования P.D. Cruces и P.D. Arini (2017) показали, что ВКГ позволяет выявлять ишемию миокарда, при этом чувствительность/специфичность метода достигает 98/100 % [24]. Y. Chen и H. Yang доказана информативность пространственно–временного ВКГ–анализа, который выявляет характерные изменения при ИМ с чувствительностью 96,8 % и специфичностью 92,8 % [25]. Американскими учеными с помощью ВКГ–сигнала с ≈ 88% чувствительностью и ≈ 92% специфичностью выявлена взаимосвязь изображения и локализации ИМ [26]. Другие авторы видят перспективным использование ВКГ–показателей для прогноза исхода коронарной патологии. Так, K. Kück и соавторами (2018) показано, что изменение нормативных значений углового расхождения петель QRS–Т является прогностическим маркером общей смертности [27]. C. Panagiotou и соавторами доказана достаточно высокая чувствительность (84,3 %) и специфичность (77,4 %) ВКГ в выявлении рубцовых изменений миокарда, связанных с перенесенным ИМ. Это позволяет прогнозировать развитие фатальных аритмий [28]. Поэтому актуальным является определение прогностической значимости ВКГ–исследования в диагностике нарушений электрической активности сердца у больных с острым периодом ИМ.
Выводы
Установлено, что чувствительность ВКГ–метода составила 99,7 %, т.е. в указанном проценте случаев при наличии ИМ с помощью ВКГ диагностировано данное заболевание. С вероятностью 93,8 % у больного, не имеющего ИМ, ВКГ исключает эту патологию, что соответствует специфичности ВКГ–диагностики.
Положительная прогностическая значимость ВКГ показывает, что с вероятностью 99,6 % пациент с ВКГ–признаками ИМ действительно будет иметь это заболевание. Отрицательная прогностическая значимость ВКГ показывает, что при отсутствии ВКГ–признаков ИМ вероятность того, что нет данного заболевания, составляет 96,8 %.
Конфликт интересов. Авторы заявляют об отсутствии какого–либо конфликта интересов при подготовке данной статьи.
1. Ощепкова Е.В. Заболеваемость и смертность от инфаркта миокарда в Российской Федерации в 2000–2011 гг. Терапевтический архив. 2013. № 4. С. 4–10.
2. Тыць С.Н. Региональная система организации и оказания экстренной медицинской помощи больным с острым коронарным синдромом в Луганской области. Український кардіологічний журнал. 2014. № 6. С. 78–82.
3. Павлов Ч.С. Неалкогольная жировая болезнь печени в клинике внутренних болезней. Русский медицинский журнал. 2010. № 28. С. 1742–1748.
4. Strauss D.G. Vectorcardiogram synthesized from the
12–lead electrocardiogram to image ischemia. J. Electrocardiol. 2009. Mar.–Apr. Vol. 42. Issue 2. P. 190–197. doi: 10.1016/j.jelectrocard. 2008.12.018.
5. Man S. Influence of the vectorcardiogram synthesis matrix on the power of the electrocardiogram–derived spatial QRS–T angle to predict arrhythmias in patients with ischemic heart disease and systolic left ventricular dysfunction. J. Electrocardiol. 2011. July–August. Vol. 44. Issue 4. P. 410–415.
6. Dawson D. Linear affine transformations between 3–lead (Frank XYZ leads) vectorcardiogram and 12–lead electrocardiogram signals. J. Electrocardiol. 2009. Vol. 42. Issue 6. P. 622–630. doi: 10.1016/j.jelectrocard.2009.05.00.
7. Norgaard B.L. Positional changes of spatial QRS– and ST–segment variables in normal subjects: Implications for continuous vectorcardiographymonitoring during myocardial ischemia.
J. Electrocardiol. 2000. Vol. 33. Issue 1. P. 23–30.
8. Yang H. Multiscale recurrence quantification analysis of spatial cardiac vectorcardiogram signals. IEEE Trans. Biomed. Eng. 2011. Vol. 58. Issue 2. Р. 339–347. doi: 10.1109/TBME.2010.2063704.
9. Matveev M. Possibilities of signal–averaged orthogonal and vector electrocardiography for locating and size evaluation of acute myocardial infarction with ST–elevation. Anadolu Kardiyol. Derg. 2007. Jul. Suppl. 1. Р. 193–197.
10. Ghista D.N. Frontal plane vectorcardiograms: theory and graphics visualization of cardiac health status. J. Med. Syst. 2010. Vol. 34. Issue 4. P. 445–458. doi: 10.1007/s10916–009–9257–x.
11. Бакуцкий В.Н. Пространственная векторэлектрокардиография. Кардиология. 2003. № 4. С. 52–54.
12. Головской Б.В. Подход к оценке состояния миокарда по данным векторкардиографии в модифицированном варианте и эхокардиографии. Ультразвуковая и функциональная диагностика. 2008. № 4. С. 48–52.
13. Волобуев А.Н. Совершенствование диагностики сердечных заболеваний с помощью дополнительного анализа электрокардиограммы. Новые Санкт–Петербургские врачебные ведомости. 2006. № 3. С. 37–41.
14. Рябыкина Г.В. Развитие методов исследования электрического поля сердца в Отделе новых методов диагностики [Электронный ресурс]. Кардиологический вестник. 2010. № 1. Режим доступа: http://www.consilium–medicum.com/magazines/magazines/special/cardiology/article/19632.
15. Steg P.G. The Task Force on the management of ST–segment elevation acute myocardial infarction of the European Society of Cardiology (ESC). Eur. Heart J. 2012. Vol. 33. Issue 20. P. 2569–2619. doi: 10.1093/eurheartj/ehs215.
16. Бєлая І.Є. Електрична активність серця у хворих на інфаркт міокарда задньонижньої локалізації у поєднанні з неалкогольною жировою хворобою печінки. Український терапевтичний журнал. 2013. № 2. С. 24–35.
17. Бєлая І.Є. Кількісний просторовий аналіз електрорушійної сили серця і прогноз за гострого інфаркту міокарда у хворих із стеатозом печінки. Український терапевтичний журнал. 2014. № 3–4. С. 78–88.
18. Белая И.Е. Чувствительность и специфичность векторкардиографии в диагностике острого инфаркта миокарда, сочетающегося со стеатозом печени или неалкогольным стеатогепатитом. Российский кардиологический журнал. 2015. № 12(128). С. 27–36. doi: 10.15829/1560–4071–2015–12–169–173.
19. Бєлая І.Є. Застосування нових технологій у дослідженні хворих з інфарктоподібними електрокардіограмами. Медицина невідкладних станів. 2012. № 4(43). С. 60–65.
20. Man S. Vectorcardiographic diagnostic & prognostic information derived from the 12–lead electrocardiogram: Historical review and clinical perspective. J. Electrocardiol. 2015. Jul.–Aug. Vol. 48. Issue 4. P. 463–75. doi: 10.1016/j.jelectrocard.2015.05.002.
21. Maheshwari S. Frank vectorcardiographic system from standard 12 lead ECG: An effort to enhance cardiovascular diagnosis. J. Electrocardiol. 2016. Mar.–Apr. Vol. 49. Issue 2. P. 231–242. doi: 10.1016/j.jelectrocard.2015.12.008.
22. Herman B.J.M. The development and validation of an easy to use automatic QT–interval algorithm. PLoS One. 2017. Sep. 1. Vol. 12. Issue 9. P. e0184352. doi: 10.1371/journal.pone.0184352.
23. Hasan M.A. A review of beat–to–beat vectorcardiographic (VCG) parameters for analyzing repolarization variability in ECG signals. Biomed. Tech. (Berl.). 2016. Feb. Vol. 61. Issue 1.
P. 3–17. doi: 10.1515/bmt–2015–0005.
24. Cruces P.D. Quaternion–based study of angular velocity of the cardiac vector during myocardial ischaemia. Int. J. Cardiol. 2017. Dec. Vol. 248. Issue 1. P. 57–63. doi: 10.1016/j.ijcard.2017.06.095.
25. Chen Y. Wavelet packet analysis of disease–altered recurrence dynamics in the long–term spatiotemporal vectorcardiogram (VCG) signals. Conf. Proc. IEEE Eng. Med. Biol. Soc. 2013. Р. 2595–2598. doi: 10.1109/EMBC.2013.6610071.
26. Le T.Q. Topology and random–walk network representation of cardiac dynamics for localization of myocardial infarction. IEEE Trans. Biomed. Eng. 2013. Aug., Vol. 60. Issue 8. P. 2325–2331. doi: 10.1109/TBME.2013.2255596.
27. Kück K. Spatial QRS–T angle variants for prediction of all–cause mortality. J. Electrocardiol. 2018. Sep.–Oct. Vol. 51. Issue 5. P. 768–775. doi: 10.1016/j.jelectrocard.2018.05.011.
28. Panagiotou C. Detection of myocardial scar from the VCG using a supervised learning approach. Conf. Proc. IEEE Eng. Med. Biol. Soc. 2013. P. 7326–7329. doi: 10.1109/EMBC.2013.6611250.

/103-2.jpg)
/103-1.jpg)
/104-1.jpg)