Международный эндокринологический журнал Том 15, №6, 2019
Вернуться к номеру
Особливості секреції мелатоніну й серотоніну у молодих жінок із різною масою тіла та їх взаємозв’язок з розвитком інсулінорезистентності
Авторы: Місюра К.В., Манська К.Г.
ДУ «Інститут проблем ендокринної патології ім. В.Я. Данилевського НАМН України», м. Харків, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
Актуальність. Актуальність дослідження обумовлена значною поширеністю надлишку маси тіла різного ступеня серед молодого жіночого населення України та необхідністю деталізації підходів до ранньої профілактики у них гормонально-метаболічних ускладнень цих патологічних станів. Мета: деталізувати особливості балансу в системі «мелатонін — серотонін — лептин — чутливість периферичних тканин до інсуліну» у жінок молодого віку — представниць української популяції із різною масою тіла, у тому числі з урахуванням особливостей його складу. Матеріали та методи. Обстежено 130 жінок, середній вік яких становив 28,64 ± 6,91 року, з екзогенно-конституційним надлишком маси тіла різного ступеня. Шляхом анкетування оцінювалась наявність порушень сну. Визначали індекс маси тіла, окружність талії; методом біоімпедансного аналізу — склад тіла (жирову, відносну жирову, безжирову, активну клітинну маси тіла); імуноферментним методом — рівні інсулін- та лептинемії. Розраховувався індекс НОМA. Секреція мелатоніну оцінювалася за вмістом у сечі рівня його метаболіту 6-сульфатоксимелатоніну (6-СОМТ) за методом Друекса в модифікації Г.В. Зубкова; серотоніну — флуориметричним методом В.І. Кулинського та Л.С. Костюковської. Результати. Встановлено, що у молодих жінок — представниць української популяції ступінь накопичення жирової тканини в організмі негативно корелює із рівнем серотонінемії, нічної та середньодобової екскреції 6-СОМТ з сечею; позитивно — із рівнем денної фракції екскреції 6-СОМТ з сечею. Зниження середньодобової екскреції 6-СОМТ та вмісту серотоніну у циркуляції має зв’язок із зростанням значення індексу НОМА та рівня лептинемії. Розвиток абдомінального ожиріння у молодих жінок — представниць української популяції характеризується зниженням рівня серотоніну у циркуляції, нічної фракції екскреції 6-СОМТ з сечею при одночасному зростанні денної. При подальшому збільшенні окружності талії вищезазначені зміни поглиблюються. Висновки. Зниження рівня серотоніну у циркуляції, нічної фракції екскреції мелатоніну при одночасному зростанні денної є значущою відмінністю пацієнток із ожирінням порівняно із жінками з надлишковою масою тіла.
ктуальность. Актуальность исследования обусловлена значительным распространением избытка массы тела разной степени среди молодого женского населения Украины и необходимостью детализации подходов к ранней профилактике у них гормонально-метаболических осложнений этих патологических состояний. Цель: детализировать особенности баланса в системе «мелатонин — серотонин — лептин — чувствительность периферических тканей к инсулину» у женщин молодого возраста — представительниц украинской популяции с разной массой тела, в том числе с учетом особенностей его состава. Материалы и методы. Обследованы 130 женщин, средний возраст которых составил 28,64 ± 6,91 года, с экзогенно-конституциональным избытком массы тела разной степени. Путем анкетирования оценивалось наличие нарушений. Определяли индекс массы тела, окружность талии; методом биоимпедансного анализа — состав тела (жировую, относительную жировую, безжировую, активную клеточную массы тела); иммуноферментным методом — уровни инсулин- и лептинемии. Рассчитывался индекс НOMA. Секреция мелатонина оценивалась по содержанию в моче уровня его метаболита 6-сульфатоксимелатонина (6-СОМТ) по методу Друекса в модификации Г.В. Зубкова; серотонина — флуориметрическим методом В.И. Кулинского и Л. Костюковской. Результаты. Установлено, что у молодых женщин — представительниц украинской популяции степень накопления жировой ткани в организме отрицательно коррелирует с уровнем серотонинемии, ночной и среднесуточной экскреции 6-СОМТ с мочой; положительно — с уровнем дневной фракции экскреции 6-СОМТ с мочой. Снижение среднесуточной экскреции 6-СОМТ и содержания серотонина в циркуляции связано с ростом значения индекса НOMA и уровня лептинемии. Развитие абдоминального ожирения у молодых женщин — представительниц украинской популяции характеризуется снижением уровня серотонина в циркуляции, ночной фракции экскреции 6-СОМТ с мочой при одновременном росте дневной. При последующем увеличении окружности талии вышеуказанные изменения усугубляются. Выводы. Снижение уровня серотонина в циркуляции, ночной фракции экскреции мелатонина при одновременном росте дневной является значимым отличием пациенток с ожирением по сравнению с женщинами с избыточной массой тела.
Background. The relevance of the study is due to the significant prevalence of excess body weight of varying degrees among the young female population of Ukraine and the need for detail approaches to the early prevention of hormonal and metabolic complications of these pathological conditions in them. The purpose was to detail the peculiarities of the balance in the system of melatonin-serotonin-leptin sensitivity of peripheral tissues to insulin in women of reproductive age — representatives of the Ukrainian population with different body weight, including and taking into account the features of body composition. Materials and methods. We examined 130 women, whose average age was 28.64 ± 6.91 years, with exogenously constitutional excess body weight of varying degrees. Questionnaires assessed the presence of sleep disorders. The body mass index and waist circumference were determined. The method of bioimpedance analysis helped evaluate the composition of the body (fatty, relative fatty, lean, active body cell mass), enzyme-linked immunosorbent assay — the level of insulin- and leptinemia. Homeostasis model assessment was calculated. Melatonin secretion was evaluated by the urine content of its metabolite 6-sulfate-oxymelatonin (6-SOMT) according to the Druex method modified by V. Zubkov; serotonin — using fluorimetric method of V.I. Kulynskyi and L. Kostiukovska. Results. In young women — representatives of the Ukrainian population, the degree of adipose tissue accumulation in the body negatively correlates with the level of serotoninemia, night and average daily urine excretion of 6-SOMT; positively — with the level of the daily fraction of 6-SOMT urine excretion. A decrease in the average daily excretion of 6-SOMT and the serotonin content in the circulation are associated with an increase in the homeostasis model assessment and the level of leptinemia. The development of abdominal obesity in young women — representatives of the Ukrainian population is characterized by a decrease in serotonin level in the circulation, a reduction in the urine excretion of nighttime 6-SOMT fraction, while the daily increase is observed. With a subsequent increase in waist circumference, the above changes are exacerbated. Conclusions. Reduced serotonin levels in the circulation, decreased nocturnal melatonin excretion fraction with a simultaneous increase of a daytime one is a significant difference in obese patients compared to overweight women.
ожиріння; надлишкова маса тіла; мелатонін; серотонін; лептин; інсулінорезистентність
ожирение; избыточная масса тела; мелатонин; серотонин; лептин; инсулинорезистентность
obesity; overweight; melatonin; serotonin; leptin; insulin resistance
Вступ
В Україні останніми роками кількість зареєстрованих пацієнтів з ожирінням (ОЖ) становить понад 500 тис. осіб [1]. Але дійсна кількість населення, яка має надлишок маси тіла різного ступеня, в Україні значно більша. Так, згідно з результатами скринінгу надлишкової маси тіла (надлМТ) та ОЖ серед дорослих мешканців м. Харкова — представників української популяції (2014–2015 рр.), визначено, що понад 70 % із них мають надмірну вагу. Значну кількість таких пацієнтів становлять жінки репродуктивного віку [2]. Це підтверджується й іншими дослідниками, за даними яких ОЖ реєструється у третини жіночого населення [3].
Виходячи з того, що жінки репродуктивного віку — категорія, для якої притаманна значна частота надлишку маси тіла різного ступеня, то зрозуміло, що вона потребує особливої уваги при проведенні профілактичних заходів.
На сьогодні у світовій медицині одним із найважливіших завдань профілактичних заходів щодо ОЖ вважається запобігання розвитку гормонально-метаболічних ускладнень надлишкового накопичення жирової тканини. Гормонами, які можуть мати суттєвий вплив на метаболічні характеристики організму, за даними літератури, крім інших, є серотонін, лептин, інсулін [4–6]. Вони є системними координаторами ліпідного та вуглеводного обміну. До того ж, що вкрай важливо для пацієнтів із надлишком маси тіла різного ступеня, їх секреція і ефективність дії залежать від ступеня, особливостей відкладання жиру і стану ендокринної функції жирової тканини [7]. Останнім часом доведено взаємозв’язок між цими гормонами та мелатоніном — регулятором метаболізму, секреція якого залежить від режиму дня, сну та безсоння людини [8]. Багато людей, у тому числі і жінок молодого віку із надлишком маси тіла різного ступеня, не виконують фізіологічного режиму цих процесів, а тому можуть мати порушення дії цього гормону і пов’язані із цим гормонально-метаболічних розлади, в першу чергу інсуліно- та лептинорезистентність, які будуть додатково обумов–лювати розвиток коморбідних первинному ОЖ патологій. Зрозуміло, що при порушенні режиму сну і наявності пов’язаних із цим гормональних розладів патогенез метаболічних порушень буде відрізнятися від такого в осіб із нормальною секрецією цього гормону навіть при однаковій масі тіла. Але деталізація таких відмінностей потребує додаткового дослідження, у тому числі з урахуванням популяційних особливостей населення України.
Невизначеним на сьогодні залишається і питання зв’язку між секрецією гормонів серотоніну та мелатоніну у молодих жінок — представниць української популяції не тільки з їх індексами маси тіла (ІМТ), але й з параметрами складу тіла, зміни яких, за даними літератури [9], є більш інформативними щодо розвитку гормонально-метаболічних порушень, в першу чергу інсулінорезистентності (ІР), що вказує на актуальність дослідження в цьому напрямку.
Мета: деталізувати особливості балансу в системі «мелатонін — серотонін — лептин — чутливість периферичних тканин до інсуліну» у жінок молодого віку — представниць української популяції із різною масою тіла, у тому числі з урахуванням особливостей його складу.
Матеріали та методи
У ДУ «Інститут проблем ендокринної патології ім. В.Я. Данилевського НАМН України» (ДУ «ІПЕП НАМН») у 2011–2019 рр. проведено комплексне дослідження нейрогормональних і метаболічних особливостей перебігу первинного ОЖ у жінок молодого віку — представниць української популяції, одним із завдань якого стало уточнення особливостей балансу в системі «мелатонін — серотонін — лептин — чутливість периферичних тканин до інсуліну».
До етапу роботи, присвяченого цьому питанню, залучались після підписання інформованої згоди 130 жінок — мешканок м. Харкова, середній вік яких становив 28,64 ± 6,91 року, з екзогенно-конституційним надлишком маси тіла різного ступеня без тяжкої супутньої патології, які не отримували медикаментозну терапію на момент обстеження і мали ті чи інші порушення сну.
У всіх обстежених вимірювалася маса тіла, окружність талії (ОТ) і визначався ІМТ.
За величиною ІМТ, згідно з класифікаційними критеріями Всесвітньої організації охорони здоров’я (1997) [9], було сформовано 4 групи обстежених:
— група 1 — жінки з надлМТ (n = 20);
— група 2 — жінки з ОЖ I ступеня (n = 29);
— група 3 — жінки з ОЖ II ступеня (n = 23);
— група 4 — жінки з ОЖ III ступеня (n = 33).
До контрольної групи ввійшли 25 практично здорових жінок з нормальною масою тіла (нМТ).
Наявність абдомінального типу ОЖ (абОЖ) та його вираженість оцінювали згідно з критеріями IDF.
Порушення сну діагностувалось методом анкетування шляхом бальної оцінки суб’єктивних характеристик сну. Клінічне дослідження проводилось у весняно-літній період із дотриманням передбачених у таких випадках заходів безпеки для здоров’я пацієнта, захисту його прав, людської гідності та морально-етичних норм відповідно до принципів Гельсінської декларації прав людини [10], Конвенції Ради Європи про права людини і біомедицини, відповідних законів України; дозволу комісії із біоетики ДУ «ІПЕП НАМНУ» (протокол № 7 від 01.03.2019). Лабораторне дослідження включало визначення концентрації глюкози плазми капілярної крові глюкозооксидазним методом за допомогою експрес-аналізатора Biosen C-line.
Секреція мелатоніну оцінювалася за вмістом у сечі рівня його метаболіту 6-сульфатоксимелатоніну (6-СОМТ) за методом Друекса в модифікації Г.В. Зубкова. Збиралася добова сеча з розподілом на денну та нічну фракції (з 8.00 до 20.00 та з 20.00 до 8.00 відповідно), в окрему ємність кожна фракція. Для аналізу враховувався діурез фракційно (день — ніч) та разом за добу. Безпосередньо для проведення самого аналізу використовувалося не менше 20 мл від кожної фракційної проби.
Збір сечі здійснювався з попередньої підготовкою. До дня її збору з раціону не менше ніж за 3 доби виключалися всі продукти із забарвлювальними речовинами (буряк, помідори, морква, чай чорний, какао, кава, шоколад), а також банани (як додаткове джерело триптофану).
Визначення концентрації серотоніну у цільній крові виконано флуориметричним методом В.І. Кулинського та Л.С. Костюковської.
Імуноферментні обстеження (метод твердофазного імуноферментного аналізу) включали визначення в крові рівнів циркулюючих: інсуліну — із використанням комерційної тест-системи Insulin ELISA Kit виробництва фірми Monobind (США) та лептину — із застосуванням реактивів на апараті ІmmunnoCHEM 2000.
Для визначення ІР проводили розрахунок НОМА-індексу (НОМА-ІR) за формулою HOMA-IR = G0 × Ins0/22,5, де G0 — рівень глюкози в крові натще (ммоль/л); Ins0 — рівень інсуліну крові натще (мкОД/мл). Значення HOMA-IР 2,77 і більше розцінювали як наявність ІР (критерії IDF, 2005) [11].
Усі обстеження проводили відповідно до рекомендацій фірм — виробників діагностичних тест-систем на основі сучасних принципів лабораторних технологій із дотриманням основних положень Конвенції Ради Європи про права людини та біомедицину (від 04.04.1997 р.), Гельсінської декларації Всесвітньої медичної асоціації про етичні принципи проведення наукових медичних досліджень за участю людини (1964–2004 рр.).
Для оцінки структури та рідинних секторів тіла застосовували біоелектричний імпедансний метод за допомогою моніторного комплексу «КМ-АР-01 Діамант» (ЗАО «Діамант»), згідно з інструкцією до експлуатації. Оцінювали такі параметри, як: жирова маса (ЖМ) (кг); відносна жирова маса (ВЖМ) — ЖМ/маса тіла (%); безжирова маса (БЖМ) — маса тіла — ЖМ (кг); співвідношення БЖМ/ЖМ; активна клітинна маса (АКМ) — маса всіх клітин, в яких відбуваються метаболічні процеси (кг); співвідношення АКМ/ЖМ.
При обробці клініко-функціональних результатів використовувалися методи описового статистичного аналізу.
Результати
Було визначено, що у пацієнток із надлМТ, ОЖ I, II і III ст. рівень денної екскреції з сечею 6-СОМТ був статистично значуще (p < 0,001; p < 0,001 та p < 0,001 відповідно) вищим порівняно з особами із нМТ та надлМТ (табл. 1). В обстежених жінок із ОЖ I, II та III ст. не встановлено відмінностей у значеннях цього показника.
Щодо нічної екскреції з сечею 6-СОМТ, то вона перевищувала денну тільки у жінок із нормальною та надлишковою масою тіла. При цьому, якщо у жінок із нМТ нічна екскреція була більшою за денну в середньому майже в 10 разів (що відповідає фізіологічному співвідношенню), то вже у жінок із надлМТ — усього удвічі, що свідчить про порушення циркадних ритмів секреції цього гормону.
За наявності ОЖ відзначалося статистично значуще зниження рівня нічної екскреції з сечею 6-СОМТ, найбільш виражене у жінок із III ступенем. В обстежених цієї категорії його рівень був утричі нижчим за аналогічний показник у жінок із нМТ та у 2,4 раза — при надлМТ. Його рівні в осіб із різним ступенем ОЖ вірогідно не відрізнялися між собою.
Різноспрямовані зміни рівнів нічної та денної екскреції з сечею 6-СОМТ обумовили той факт, що середньодобова секреція цього метаболіту мелатоніну в осіб із різною масою тіла також суттєво не різнилася.
Під час роботи вивчався і взаємозв’язок між рівнями екскреції 6-СОМТ з сечею молодих жінок та основними параметрами складу їх тіла, які, за даними літератури, є більш чутливими маркерами розвитку метаболічних порушень, ніж ІМТ (табл. 2).
Виявлено, що обстежені жінки молодого віку — представниці української популяції із нМТ мали ЖМ на рівні 12,09 ± 2,44 кг, що становить майже 20 % від їх загальної маси тіла, що відповідає, за даними літератури, ступеню накопичення жирової тканини у молодих жінок — представниць інших європеоїдних популяцій [12, 13].
У пацієнток із надлМТ значення ЖМ та ВЖМ вірогідно зростали вже на 194 та на 155 % відповідно.
При розвитку ОЖ I, II та III ст. ЖМ становила 260; 332 та 461 % від аналогічного показника у жінок із нМТ. В обстежених з надлишком маси тіла різного ступеня зареєстровано абсолютне збільшення і БЖМ порівняно з контролем (на 109 % при надлМТ і на 119; 129 та 151 % при первинному ОЖ I, II і III ст. відповідно), і АКМ — при надлМТ на 116 % відносно осіб із нМТ; при ОЖ I, II і III ступеня — на 127; 138 та 160 %. Вірогідність відмінностей усіх середніх за критерієм Краскела — Уолліса реєструвалася на рівні p < 0,001.
При дослідженні залежності між рівнем денної екскреції 6-СОМТ і ЖМ виявлено прямий статистично значущий (p < 0,001) кореляційний зв’язок помірної сили (рівень кореляції r = 0,3771) (рис. 1).
Визначено рівняння регресії, згідно з яким рівень денної екскреції 6-СОМТ (нмоль/день) становить [14,1015 + 0,5786 × ЖМ (кг)].
Щодо нічної екскреції 6-СОМТ з сечею у молодих жінок, то виявлено негативний вірогідний (p < 0,001) корелятивний її зв’язок середньої сили із ЖМ (r = –0,6625) (рис. 2). Рівняння регресії, згідно з яким можливо оцінить нічну екскрецію 6-СОМТ з сечею у молодих жінок (нмоль/ніч), — [101,1794 – – 1,3091 × ЖМ (кг)].
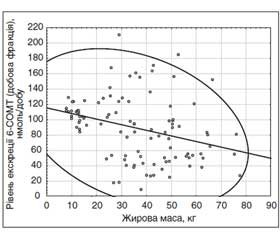
Було також визначено, що середній за добу рівень екскреції 6-СОМТ з сечею у молодих жінок статистично значуще (p = 0,0009) негативно корелював і з ЖМ (рис. 3). Сила кореляції була помірною (r = –0,3201). Рівняння регресії: середній за добу рівень екскреції 6-СОМТ з сечею у молодих жінок (нмоль/добу) = 115,2809 – 0,7305 × × ЖМ (кг).
Провідним фактором, який одночасно обумовлює як зростання ЖМ, так і розвиток метаболічних ускладнень в осіб із надлишком маси тіла, є зниження чутливості периферичних тканин до інсуліну — виникнення ІР. Основний маркер її наявності — збільшення індексу НОМА-IR.
Суттєво впливає на наявність та ступінь ІР гормон епіфіза мелатонін. З метою деталізації особливостей взаємозв’язку між рівнями секреції цього гормону та значенням НОМA-IR у молодих жінок — представниць української популяції в процесі виконання роботи було проведено дослідження і в цьому напрямку (табл. 3).
Було визначено, що між НОМА-IR та рівнем екскреції 6-СОМТ з сечею за добу у молодих жінок виявлено негативний статистично значущий (p = 0,00008) кореляційний зв’язок помірної сили (ступінь кореляції r = –0,3778).
Рівняння регресії: середній за добу рівень екскреції 6-СОМТ з сечею у молодих жінок (нмоль/добу) = 5,9557 – 0,02 × НОМА-IR.
Результати визначення особливостей лептинемії у молодих жінок із різною масою тіла, які були отримані в процесі проведення роботи, надано в табл. 4.
За даними проведеного дослідження встановлено, що у жінок молодого віку із первинним ОЖ ІІ–ІІІ ст. рівень лептину у сироватці крові був відповідно у 2,4 та 2,9 раза вище порівняно з обстеженими з нМТ, а в осіб із ОЖ III ст. — і порівняно із жінками із надлМТ (у 2,1 раза). Встановлено, що рівні лептину статистично значуще зростали зі збільшенням ступеня ОЖ. В осіб із ОЖ I та III ступенів значення цього параметра вірогідно різнилися у 1,7 раза.
При аналізі взаємозв’язків між досліджуваними параметрами зареєстровано, що рівень лептину в сироватці крові статистично значуще негативно корелює із рівнем добової екскреції 6-СОМТ з сечею (r = –0,2163; p = 0,0274). Але сила кореляції була досить слабка (рис. 4).
Пріоритетним результатом даного дослідження стало уточнення рівняння регресії щодо взаємовпливу у системі «добова екскреція 6-СОМТ з сечею — лептинемія», яка характерна для молодих жінок — представниць української популяції. Рівняння регресії: добова екскреція 6-СОМТ з сечею (нмоль/добу) = 49,6699 – 0,0966 × рівень лептину крові (нг/мл).
При її виконанні було зареєстровано вірогідне зниження (майже удвічі) рівня циркуляторного серотоніну у молодих жінок із первинним ОЖ III ст. порівняно з групою жінок аналогічного віку із нМТ (табл. 5).
Наявність негативного взаємозв’язку між рівнем циркуляторного серотоніну та ступенем накопичення жирової тканини підтверджено шляхом оцінки корелятивної взаємозалежності маси жирової тканини в організмі жінок молодого віку із різною масою тіла та вмісту серотоніну у сироватці їх крові (рис. 5). Визначено, що ЖМ має із циркуляторним рівнем даного моноаміну статистично значущий (p = 0,00001) негативний зв’язок помірної сили (r = –0,3799). Залежність відображається таким рівнянням регресії: рівень циркуляторного серотоніну (нг/мл) = 1,2662 – 0,0078 × ЖМ.
Після підтвердження зв’язку між секрецією серотоніну і накопиченням жирової тканини в даному дослідженні було доведено і взаємовплив між рівнем серотонінемії та особливостями її ендокринної функції. Остання оцінювалась за рівнем циркулюючого лептину (рис. 6).
Отримані результати свідчать про наявність статистично значущого (p = 0,0002) негативного зв’язку помірної сили (r = –0,3253) між цими досліджуваними параметрами, який описується таким рівнянням регресії: рівень циркуляторного серотоніну (нг/мл) = 1,2501 – 0,0064 × рівень циркуляторного лептину (нг/мл).
У процесі даного дослідження було показано, що НОМА-ІR у молодих жінок — представниць української популяції знаходиться у негативному кореляційному зв’язку слабкої сили (r = –0,2747). Даний зв’язок є статистично значущим на рівні p = 0,0019. Рівняння регресії: рівень циркуляторного серотоніну (нг/мл) = 49,6699 – 0,0966 × × HOMA.
На сьогодні основним інтегральним антропометричним параметром, що характеризує наявність ІР та, відповідно, ризик метаболічних ускладнень, вважається ОТ — маркер абдомінального (вісцерального) ОЖ. Тому в процесі роботи було досліджено рівень серотонінемії у молодих жінок залежно від наявності останнього та його ступеня, результати якого подано на рис. 7. Встановлено, що в осіб із наявністю вираженого абОЖ рівень циркуляторного серотоніну є статистично значуще нижчим як порівняно з особами із помірним абОЖ (p < 0,004), так і з тими, у кого ОТ не перевищує норму (p < 0,008), — відповідно 0,92 ± 0,35 мкмоль/л проти 1,24 ± 0,43 та 1,13 ± 0,34 нг/мл (за критерієм Краскела — Уолліса p < 0,001).
У процесі роботи було також оцінено характер змін рівнів екскреції з сечею 6-СОМТ залежно від ступеня накопичення жирової тканини на передній черевній стінці. Результати дослідження нічної та денної екскреції метаболіту мелатоніну 6-СОМТ з сечею залежно від значення ОТ, яка характерна для молодих жінок, наведено на рис. 8.
Були зареєстровані різноспрямовані зміни у досліджуваних фракціях. При розвитку абОЖ та зростанні його ступеня спостерігалося вірогідне зростання денної та зменшення нічної фракції порівняно з молодими жінками, без абОЖ.
Так, якщо у жінок останньої категорії вміст 6-СОМТ у сечі, яка збиралась удень, був на рівні 10,12 ± 2,42 нмоль/день, то у жінок із помірним абОЖ — на рівні 36,46 ± 25,19 нмоль/день, із вираженим абОЖ — на рівні 43,37 ± 27,68 нмоль/день (за критерієм Краскела — Уолліса, p < 0,001).
Відносно нічної екскреції з сечею 6-СОМТ, то вона становила у жінок без абОЖ 97,97 ± 11,45 нмоль/ніч, у жінок із помірним абОЖ — 59,69 ± 35,55 нмоль/ніч, із вираженим — 38,92 ± 28,24 нмоль/ніч (за критерієм Краскела — Уолліса, p < 0,001).
Обговорення
Таким чином, при проведенні даного дослідження у молодих жінок із різною масою тіла — представниць української популяції було визначено, що зниження добового рівня секреції мелатоніну та вмісту серотоніну у циркуляції супроводжується підвищенням рівня лептинемії, накопиченням жирової тканини, розвитком інсулінорезистентності та абдомінального ОЖ. Найбільших змін відносно осіб із нМТ щодо секреції цих гормонів зазнають жінки із ОЖ III ст. Отримано дані, що свідчать про вірогідний негативний взаємозв’язок між ступенем накопичення жирової тканини у молодих жінок та рівнем їх нічної секреції мелатоніну. Це може свідчити про протективну роль підвищення добової секреції мелатоніну саме за рахунок її нічної фракції щодо розвитку інсуліно- та лептинорезистентності у молодих жінок, запобігання надлишковому відкладанню у них жирової тканини, у тому числі і на передній черевній стінці.
Визначено, що зниження рівня серотоніну у циркуляції, нічної фракції екскреції мелатоніну при одночасному зростанні денної є значущою відмінністю пацієнток із ОЖ порівняно з особами з надлМТ.
Слід зазначити, що питання взаємозв’язку між ступенем накопичення жирової тканини та змінами секреції мелатоніну і серотоніну і розвитком метаболічних ускладнень є досить дискутабельним. Попри те, що в літературі існує низка повідомлень щодо особливостей секреції гормонів мелатоніну, лептину та серотоніну та їх взаємозв’язку із ступенем чутливості тканин до інсуліну у пацієнтів із ОЖ представників інших популяцій, багато із них досить неоднозначні. Результати більшості не суперечать даним, отриманим у нашому дослідженні [14]. Згідно з ними, дефіцит мелатоніну вірогідно пов’язаний з усіма компонентами метаболічного синдрому. Це пояснюється здатністю мелатоніну активізувати синтетичні процеси, які проходять в мітохондріях; регулювати ген інсулінового рецептора, що обумовлює нормальний метаболізм глюкози; нормалізувати секрецію гонадотропінів у гіпофізі; участь в метаболізмі серотоніну та гормону D, без якого неможливо підтримання нормальної структури тіла.
Але слід зазначити, що А. Malazonia та співавт. [15] отримали більш високий рівень мелатоніну у пацієнтів із ОЖ, ніж в осіб із нМТ. На думку науковців, це можливо розцінити як компенсаторну реакцію, у тому числі і щодо «захисту організму від вільних радикалів». Але існує необхідність експериментального підтвердження цього твердження.
На нашу думку, неоднозначність отриманих результатів пояснюється відмінностями категорій пацієнтів, які були залучені до обстежень, а також, можливо, і їх популяційними особливостями. Це вказує на необхідність проведення подальших досліджень в цьому напрямку для різних категорій представників саме української популяції, у тому числі і з різним терміном виникнення надлишкової ваги та тривалості порушень сну.
Щодо динаміки рівнів серотонінемії, то при обстеженні закордонними науковцями осіб обох статей із морбідним ОЖ у більшості пацієнтів (як і при обстеженні молодих жінок — представниць української популяції) реєструвалося збільшення лептину та зниження серотоніну. Корекція маси тіла дозволяла знизити концентрацію циркулюючих лептину і збільшити — серотоніну, однак все одно їх рівні не досягають нормальних цифр. І ці зміни пояснюють низку питань щодо розвитку ОЖ та його метаболічних ускладнень. Як відомо, основа ОЖ — порушення енергетичної рівноваги, яке призводить до надмірного накопичення жирової тканини. У регуляції енергетичної рівноваги провідну роль відіграє мозок: він впливає на споживання їжі і витрати енергії шляхом модифікації харчової поведінки. Одними з регуляторів харчової поведінки є лептин, який впливає на продукцію нейропептидів з аноректичною дією і на рівень пептидів, що стимулюють споживання їжі на рівні гіпоталамуса, та серотонін — моноамін, який регулює периферичний термогенез.
Але результати деяких повідомлень щодо рівнів серотонінемії в осіб із надлишком маси тіла вказують на збільшення вмісту серотоніну у циркуляції в осіб із ОЖ. Так, дослідники [8] при обстеженні жінок з ОЖ отримали збільшення в 30 разів порівняно зі здоровими рівня серотоніну плазми у жінок з ОЖ. При цьому жінки із суттєвим зростанням рівня серотоніну відрізнялися наявністю і високих рівнів лептину. Автори пояснюють такі результати можливим розвитком лептино- та серотонінорезистентності у частини пацієнтів із ОЖ.
Дослідження щодо питання особливостей секреції мелатоніну у пацієнтів із різною масою тіла проводилися і в Україні, але до нього було залучено підлітків з артеріальною гіпертензією, нМТ, надлМТ та ОЖ. Було встановлено, що у підлітків з артеріальною гіпертензією і надлишком маси тіла вірогідно вищими були показники екскреції 6-СОМТ з сечею, особливо денної його фракції, порівняно з підлітками з артеріальною гіпертензією та нМТ. У підлітків з надмірною вагою відзначено більш виражене зниження порівняно з денною нічної фракції 6-СОМТ. Це підтверджує в цілому дані, отримані в нашому обстеженні молодих жінок. Але у зв’язку із різними категоріями пацієнтів повністю їх порівняти не є можливим.
Все вищенаведене вказує на невизначеність сьогоднішніх поглядів на особливості гормонального ланцюга при різній масі тіла, у тому числі і у молодих жінок — представниць різних популяцій. Про дослідження з урахуванням складу тіла, які, як вже зазначалось, також мають вплив на розвиток інсулінорезистентності, в доступній літературі не повідомляється, що доводить пріоритетність результатів, отриманих під час роботи, результати якої висвітлено у статті. Її результати переконливо доводять, що при наданні медичної допомоги жінкам молодого віку із надлишком маси тіла треба обов’язково уточнювати характер якості та режиму сну кожної з пацієнток. У разі наявності порушень режиму сну та/або його якості, доцільним є визначення у пацієнтки особливостей балансу в системі «мелатонін — серотонін — лептин — чутливість периферичних тканин до інсуліну» з метою оцінки у неї ризику розвитку метаболічних ускладнень — основи інвалідизуючої хронічної неінфекційної патології.
Висновки
1. У молодих жінок — представниць української популяції ступінь накопичення жирової тканини в організмі негативно корелює із рівнем серотонінемії, нічної та середньодобової екскреції 6-сульфатоксимелатоніну з сечею; позитивно — із рівнем денної фракції екскреції 6-сульфатоксимелатоніну з сечею.
2. Зниження середньодобової екскреції 6-сульфатоксимелатоніну та вмісту серотоніну у циркуляції має зв’язок із зростанням значення НОМА-індексу та рівня лептинемії.
3. Розвиток абдомінального ожиріння у молодих жінок — представниць української популяції характеризується зниженням рівня серотоніну у циркуляції, нічної фракції екскреції 6-сульфатоксимелатоніну з сечею при одночасному зростанні денної.
4. Зниження рівня серотоніну у циркуляції, нічної фракції екскреції мелатоніну при одночасному зростанні денної є значущою відмінністю молодих пацієнток із ожирінням порівняно з жінками з надлишковою масою тіла аналогічного віку.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при виконанні роботи та написанні статті.
- Handbook of performance indicators of the endocrinological care of Ukraine for 2014. Endocrinology. 2015;20(Suppl 1):1-38. (in Ukrainian).
- Misiura KV. Some aspects concerning abdominal obesity diagnosis in city population of Ukraine. Mìžnarodnij endokrinologìčnij žurnal. 2017;13(6). doi: 10.22141/2224-0721.13.6.2017.11288.
- WHO. Obesity and overweight. 2016. Available from: https://www.who.int/news-room/fact-sheets/detail/obesity-and-overweight.
- Hall KD. A review of the carbohydrate-insulin model of obesity. Eur J Clin Nutr. 2017 Mar;71(3):323-326. doi: 10.1038/ejcn.2016.260.
- Brown A, Guess N, Dornhorst A, Taheri S, Frost G. Insulin-associated weight gain in obese type 2 diabetes mellitus patients: What can be done? Diabetes Obes Metab. 2017 Dec;19(12):1655-1668. doi: 10.1111/dom.13009.
- Crujeiras AB, Carreira MC, Cabia B, Andrade S, Amil M, Casanueva FF. Leptin resistance in obesity: An epigenetic landscape. Life Sci. 2015 Nov 1;140:57-63. doi: 10.1016/j.lfs.2015.05.003.
- Crane JD, Palanivel R, Mottillo EP, et al. Inhibiting peripheral serotonin synthesis reduces obesity and metabolic dysfunction by promoting brown adipose tissue thermogenesis. Nat Med. 2015 Feb;21(2):166-72. doi: 10.1038/nm.3766.
- McCuen-Wurst C, Ruggieri M, Allison KC. Disordered eating and obesity: associations between binge-eating disorder, night-eating syndrome, and weight-related comorbidities. Ann N Y Acad Sci. 2018 Jan;1411(1):96-105. doi: 10.1111/nyas.13467.
- World Health Organization. Obesity: preventing and managing the global epidemic Report of a WHO Consultation (WHO Technical Report Series 894). Geneva; 2000. 252 p.
- World Medical Association Declaration of Helsinki. Ethical Principles for Medical Research Involving Human Subjects. WMA, 2004. 32 p.
- International Diabetes Federation. The IDF consensus worldwide definition of the metabolic syndrome, 2005. Available from: https://www.idf.org/e-library/consensus-statements/60-idfconsensus-worldwide-definitionof-the-metabolic-syndrome.html.
- De Lorenzo A, Andreoli A, Matthie J, Withers P. Predicting body cell mass with bioimpedance by using theoretical methods: a technological review. J Appl Physiol (1985). 1997 May;82(5):1542-58. doi: 10.1152/jappl.1997.82.5.1542.
- Gudivaka R, Schoeller DA, Kushner RF, Bolt MJ. Single- and multifrequency models for bioelectrical impedance of body water compartments. J Appl Physiol (1985). 1999 Sep;87(3):1087-96. doi: 10.1152/jappl.1999.87.3.1087.
- Taheri S, Lin L, Austin D, Young T, Mignot E. Short sleep duration is associated with reduced leptin, elevated ghrelin, and increased body mass index. PLoS Med. 2004 Dec;1(3):e62. doi: 10.1371/journal.pmed.0010062.
- Malazonia A, Zerekidze T, Giorgadze E, Chkheidze N, Asatiani K. Melatonin Level Variations with Different Behavioural Risk Factors in Obese Female Patients. Open Access Maced J Med Sci. 2017 Aug 12;5(5):613-617. doi: 10.3889/oamjms.2017.063.

/445-1.jpg)
/446-1.jpg)
/446-2.jpg)
/447-1.jpg)
/447-2.jpg)
/448-1.jpg)
/448-2.jpg)
/449-1.jpg)
/449-2.jpg)