Журнал «Медицина неотложных состояний» 3 (66) 2015
Вернуться к номеру
Інтраопераційна динаміка циркуляторних показників при різних методах загальної анестезії під час операцій у положенні на животі
Авторы: Рудь О.А. — ДНУ «Науково-практичний центр профілактичної та клінічної медицини» ДУС, м. Київ
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
У наведеній роботі порівнюються гемодинамічні зміни при використанні двох найбільш поширених методик загальної анестезії — тотальної внутрішньовенної та інгаляційної анестезії — під час виконання ендоскопічних операцій на нирках. Отримані результати свідчать про те, що вибір анестетика для забезпечення даної операції не впливає на рівень артеріального тиску.
В приведенной работе сравнивались изменения гемодинамики при использовании двух наиболее распространенных методик общей анестезии — тотальной внутривенной и ингаляционной анестезии — во время проведения чрескожной нефролитотрипсии. Полученные результаты показали, что выбор анестетика для обеспечения данной операции не влияет на уровень артериального давления.
In this study postural hemodynamic changes were compared during usage of two most common methods of general anesthesia — total intravenous and inhalation anesthesia — as the anaesthesiological management of percutaneous nephrolithotripsy. The study results show that the choice of anesthetic has no effect on blood pressure for this type of surgery.
гемодинаміка, положення на животі, загальна анестезія.
гемодинамика, положение на животе, общая анестезия.
hemodynamics, prone position, general anesthesia.
Статья опубликована на с. 32-34
Вступ
Сечокам’яна хвороба (СКХ) є одним з найбільш частих урологічних захворювань, і в різних країнах від неї страждають від 1,5 до 3 % населення. Поширеність СКХ в Україні посідає друге місце після інфекції сечових шляхів та становить 30–45 % від усієї урологічної патології. У 70 % випадків уролітіаз діагностують у найбільш працездатному віці (30–60 років), а в 11 % випадків це захворювання стає причиною інвалідності. Захворювання перебігає з явищами гострого та хронічного пієлонефриту, частими рецидивами (30–80 %), що, у свою чергу, призводить до виникнення ниркової недостатності, інвалідизації та смерті хворих. У 2010 році смертність від СКХ в Україні становила 0,869 % [8, 14].
До 50 % хворих з уролітіазом мають камені в нирках. У 2010 році в Україні поширеність каменів нирок серед дорослих становила 754 випадки на 100 000 населення [14]. З огляду на значну поширеність захворювання, високу частоту рецидивів, тяжкість ускладнень, ураження в основному людей молодого працездатного віку, питання лікування СКХ є однією з актуальних проблем сучасної медицини.
Останніми роками в клінічну практику широко впроваджують різноманітні малоінвазивні методи лікування каменів нирок — дистанційну літотрипсію та рентген-ендоскопічні методи лікування. Більшість авторів відзначають високу ефективність малоінвазивних методів при лікуванні СКХ, їх малу травматичність та легку переносимість для хворих [2, 3, 11, 12].
Черезшкірні ендоскопічні втручання (черезшкірна нефролітотрипсія — ЧШНЛ) під рентген- або УЗД-контролем є методом вибору при наявності технічних та фізіологічних протипоказань до дистанційної літотрипсії при великих, коралоподібних, множинних каменях та каменях високої щільності [4, 6, 9].
Анестезіологічне забезпечення при ЧШНЛ повинно враховувати такі особливості, як:
— положення пацієнта на животі з можливим виникненням поступальних порушень гемодинаміки та респіраторної функції;
— охолодження пацієнта через використання великих об’ємів іригаційних рідин;
— можливість екстравазації промивної рідини в заочеревинний простір;
— ризик поранення плеври;
— порушення водно-електролітного балансу та кислотно-основного стану;
— високий ризик кровотечі з нирки;
— наявність інфекції сечових шляхів початково.
Серед прогнозованих патофізіологічних змін важливе місце займають постуральні зміни гемодинаміки, до яких відносять зниження серцевого викиду та ударного об’єму після повороту пацієнта на живіт через зменшення венозного повернення й значного збільшення системного та легеневого судинного опору [15].
За кордоном у більшості клінік ЧШНЛ виконують в умовах загальної анестезії. На сьогодні найчастіше використовуються дві основні методики загальної анестезії — тотальна внутрішньовенна анестезія (ТВВА) та інгаляційна анестезія (ІА). Перевагами тотальної внутрішньовенної анестезії пропофолом є мала частота післяопераційної нудоти та блювання, а також відсутність забруднення операційної. Але вартість години анестезії пропофолом значно вища порівняно з інгаляційною анестезією. До переваг інгаляційної анестезії відносять меншу вартість години анестезії та більшу гемодинамічну стабільність. Недоліки — дороговартісне обладнання та забруднення операційної анестетиком [8, 13].
Тому метою нашого дослідження було визначити вплив різних методів загальної анестезії на гемодинамічний профіль при ЧШНЛ.
Матеріали та методи
Після отримання письмової згоди від пацієнтів було відібрано 30 хворих віком 18–64 роки з фізіологічним статусом за ASA І–ІІ, яким планували ЧШНЛ. Були виключені хворі з індексом маси тіла менше 18,5 та більше 34,9 кг/м2, хронічними декомпенсованими та гострими захворюваннями дихальної, серцево-судинної систем, печінки, нирок та ендокринної системи, а також хворі на алкоголізм та наркоманію та пацієнти з фіксованим серцевим викидом (стеноз аортального отвору), вагітні.
Як основний параметр гемодинамічної стабільності ми оцінювали середній артеріальний тиск (АТсер.), що є показником перфузії органів [1].
Для контролю глибини анестезії використовували біспектральний індекс (БІС), оскільки недостатня чи надмірна глибина анестезії може впливати на показники гемодинаміки.
Залежно від методу анестезії, що використовувався, хворі були рандомізовані на дві групи: 1-ша група — тотальна внутрішньовенна анестезія, 2-га — інгаляційна анестезія.
У групі ТВВА анестезія проводилась розчином пропофолу 1% за цільовою концентрацією в плазмі крові без зворотного зв’язку шприцевим дозатором B Braun Space. Індукція: фентаніл 2 мкг/кг, концентрація пропофолу в плазмі 5–6 мкг/дл до досягнення показника БІС 40–45 одиниць. Після міоплегії (рокуроній 0,6 мг/кг) проводилась інтубація трахеї. Штучна вентиляція легень (ШВЛ) проводилась у режимі нормовентиляції за показниками капнометрії апаратом Dräger Fabius Tiro повітряно-кисневою сумішшю низькими потоками (1 л/хв). Підтримка анестезії проводилась розчином пропофолу 1% за цільовою концентрацією в плазмі крові без зворотного зв’язку, показник БІС підтримували в межах 40–60 одиниць.
У групі ІА індукція проводилась пропофолом болюсами по 30 мг до досягнення значень БІС 40–45 одиниць, фентаніл 2 мкг/кг. Після міоплегії (рокуроній 0,6 мг/кг) проводилась інтубація трахеї та ШВЛ за тими ж параметрами, що й у першій групі. Підтримка анестезії проводилась севофлюраном у повітряно-кисневій суміші низькими потоками (1 л/хв). Доза інгаляційного анестетика корегувалась за показником БІС, цільове значення БІС підтримували в межах 40–60 одиниць.
В обох групах з метою анальгезії проводили постійну інфузію розчину фентанілу 0,005% з розрахунку 2 мкг/кг/год.
Інфузія розчинів в обох групах проводилось однаково (до повороту на живіт хворі отримували збалансовані електролітні розчини з розрахунку 10 мл/кг, після повороту на живіт інфузія проводилась із розрахунку 5–6 мл/кг/год). Якщо протягом трьох вимірювань поспіль (з інтервалом 5 хв) АТсер. становив менше 55 мм рт.ст., але не менше 50 мм рт.ст., до інфузії додавався розчин колоїдів (10% розчин гідроксіетилкрохмалю 200/0,5/5). Якщо протягом трьох вимірювань поспіль АТсер. становив менше 50 мм рт.ст., до інфузії додавали симпатоміметики (фенілефрин).
Для полегшення хірургу доступу до нирки перед початком пункції чашково-мискової системи нирки підіймався валик хірургічного стола в проекції нирки.
За вихідні показники гемодинаміки брали значення АТ та ЧСС, отримані при попередньому огляді пацієнта анестезіологом за кілька днів до операції.
Математичну обробку отриманих даних проводили із застосуванням пакета прикладних програм Statistica 6.0 for Microsoft Windows.
Результати
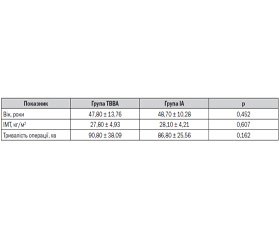
Демографічні дані 30 пацієнтів, які були відібрані для дослідження, та їх розподіл на групи наведені в табл. 1.
Групи порівняння були однорідними й цілком придатними для дослідження.
Зміни параметрів гемодинаміки при повороті хворих на живіт подані в табл. 2.
В обох групах ми спостерігали значне зниження АТсист., але статистично значущої різниці між групами тотальної внутрішньовенної анестезії та інгаляційної анестезії не було (р > 0,05).
Середні показники АТсер. на другому етапі операції (табл. 3) становили 72,10 ± 4,64 мм рт.ст. та 75,10 ± 5,25 мм рт.ст., що свідчить про достатній рівень перфузії органів та тканин, незважаючи на значне зниження АТсист. Mіж групами статистично значущої різниці АТсер.не було (р > 0,05).
У двох пацієнтів (13,3 %) групи тотальної внутрішньовенної анестезії була потреба в додатковій інфузії розчину гідроксіетилкрохмалю (АТсер. < 55 мм рт.ст. протягом трьох вимірів). У групі інгаляційної анестезії додаткову інфузію колоїдного розчину проводили в одного пацієнта (6,7 %). В обох групах у трьох пацієнтів (20 %) після повороту на живіт ми спостерігали брадикардію (ЧСС < 50/хв), що потребувала введення атропіну.
Обговорення результатів
За даними різних авторів, при повороті на живіт ступінь змінення серцевого викиду дуже різниться. Автори пояснюють це різницею розміщення пацієнта на столі та використанням різноманітних підтримуючих пристроїв [1]. Основним механізмом зниження серцевого викиду є зниження венозного повернення до серця внаслідок стискання нижньої порожнистої вени та збільшення постнавантаження. При цьому компенсаторно збільшується системний судинний опір, що дозволяє підтримувати АТсер. на достатньому рівні для забезпечення достатньої перфузії внутрішніх органів.
В отриманих нами даних при положенні хворого на животі з валиком у ділянці проекції нирки вибір анестетика на етапі підтримки загальної анестезії не впливав на постуральні зміни гемодинаміки.
Висновки
Той факт, що вибір анестетика на етапі підтримки загальної анестезії не впливає на постуральні зміни гемодинаміки в положенні хворого на животі, дозволяє лікарю індивідуально підходити до вибору анестезії для пацієнта. А також враховувати, окрім показань та протипоказань, фінансові можливості як пацієнта, так і клініки.
1. Edgcombe H. Anaesthesia in the prone position / H. Edgcombe, K. Carter, S. Yarrow // British Journal of Anaesthesia. — 2008. — 100 (2). — P. 165-183. doi: 10.1093/bja/aem380.
2. Hruza M. Laparoscopic and open stone surgery / Hruza M., Zuazu J., Goezen A., de la Rosette J., Rassweiler J. // Arch. Ital. Urol. Androl. — 2010. — Vol. 82(1). — P. 64-71. doi: 10.1089/end.2009.1539.
3. Istanbulluoglu M.O. Effectiveness of totally tubeles spercutaneous nephrolithotomy inselected patients: a prospective randomized study / Istanbulluoglu M.O., Ozturk B., Gonen M., Cicek T., Ozkardes H. // Int. Urol. Nephrol. — 2009. — Vol. 41, № 3. — P. 541-545. doi: 10.1007/s11255-008-9517-6.
4. Resorlu B. Percutaneous nephrolithotomy for complex caliceal and staghorn stones in patients with solitary kidney / Resorlu B., Kara C., Oguz U., Bayindir M., Unsal A. // Urol. Res. — 2011. — 39(3). — P. 171-176. doi: 10.1007/s00240-010-0321-2.
5. Sudheer P.S. Haemodynamic effects of the prone position: a comparison of propofol total intravenous and inhalation anaesthesia / P.S. Sudheer, S.W. Logan, B. Ateleanu, J.E. Hall // Anaesthesia. — 2006. — 61(2). — Р. 138-41. doi: 10.1111/j.1365-2044.2005.04464.x
6. Yang B. Standard-tract percutaneous nephrolithotomy accessed by two-step dilation for 3052 patients / Yang B., Li J., Hu W.G., Huang X.B., Wang X.F. // Beijing Da Xue Xue Bao. — 2010. — Vol. 42(4). — P. 46-51.
7. Zerrin Ozkose. Inhalation Versus Total Intravenous Anesthesia for Lumbar Disc Herniation: Comparison Of Hemodynamic Effects, Recovery Characteristics, And Cost / Zerrin Ozkose, Bilge Ercan, Yusuf Ünal, Sahin Yardim, Memduh Kaymaz, Fikret Dogulu, Aydn Pasaoglu // Disc. Herniation Journal of Neurosurgical Anesthesiology. — 2001. — Vol. 13, № 4. — Р. 296-302.
8. Акилов Ф.А. Послеоперационные инфекционно-воспалительные осложнения эндоскопических операций по поводу уролитиаза / Акилов Ф.А., Мухтаров Ш.Т., Гиясов Ш.И., Насыров Ф.Р., Мирхамидов Д.Х., Муратова Н.Б. // Урология. — 2013. — № 1. — С. 89-91.
9. Аль-Шукри С.Х. Урология: Учебник / Под ред. С.Х. Аль-Шукри, В.Н. Ткачука / С.Х. Аль-Шукри, В.Н. Ткачук. — 2011. — С. 480.
10. Аполихин О.И. Эпидемиология МКБ в различных регионах РФ по данным официальной статистики. Материалы российской научной конференции с международным участием «Мочекаменная болезнь: фундаментальные исследования, инновации в диагностике и лечении» / Аполихин О.И., Сивков А.В., Солнцева Т.В. и др. // Саратовский научно-медицинский журнал. — 2011. — Т. 7, № 2 (прил.). — С. 120.
11. Мартов А.Г. Трансуретральная пиелокаликолитотрипсия и литоэкстракция — новый метод лечения камней почек / Мартов А.Г., Ергаков Д.В., Москаленко С.А., Лисенок А.А., Степанов В.С., Фатихов Р.Р. // Урология. — 2009. — (1). — C. 26-24.
12. Назаров Т.Х. Современные аспекты патогенеза, диагностики и лечения мочекаменной болезни: Дис… д-ра мед. наук. — СПб., 2009.
13. Перлин Д.В. Малоинвазивные методы лечения мочекаменной болезни / Перлин Д.В., Костромеев С.А. // Вестник ВолГМУ. — 2010. — 4(36). — С. 112-114.
14. Урологія / За редакцією С.П. Пасєчнікова. — Вінниця: Нова Книга, 2013. — С. 218-226.
15. Шевцов Т.П. Тотальная внутривенная анестезия при операциях на позвоночнике / Т.П. Шевцова, В.П. Гаврилюк, С.Н. Гриценко, Т.И. Евченко // Біль, знеболення та інтенсивна терапія. — 2008. — № 4. — С. 38-42.

/33/33.jpg)
/34/34.jpg)